Toàn Bộ Lý Thuyết Và Cách Viết Cấu Hình Electron Nguyên Tử Dễ Nhớ
Cấu hình electron nguyên tử biểu diễn điều gì?
Cấu hình electron (hay còn được gọi là cấu hình điện tử nguyên tử) biểu diễn sự phân bố các electron trong lớp vỏ nguyên tử ở các trạng thái năng lượng khác nhau hay ở các vùng hiện diện của chúng (theo Wikipedia).
Nói một cách khác, cấu hình electron nguyên tử biểu diễn sự phân bố electron trên các phân lớp thuộc các lớp khác nhau.
Ví dụ: Cấu hình e của nguyên tử của một vài nguyên tố thường gặp:
| Nguyên tố | Z | Cấu hình e |
| K | 19 | 1s22s22p63s23p64s1 |
| Ca | 20 | 1s22s22p63s23p64s2 |
| Al | 13 | 1s22s22p63s23p1 |
| Fe | 26 | 1s22s22p63s23p63d64s2 |
| Cu | 29 | 1s22s22p63s23p63d104s1 |
| Cr | 24 | 1s22s22p63s23p63d54s1 |
Cụ thể, cấu hình electron của nguyên tử là chuỗi số đại diện cho các obitan electron. Đây là các khu vực không gian có hình dạng khác nhau bao quanh hạt nhân nguyên tử, trong đó các electron được sắp xếp một cách trật tự. Qua cấu hình electron bạn có thể nhanh chóng xác định số lượng obitan electron trong nguyên tử, và số electron trong từng obitan.
Thứ tự các mức năng lượng trong nguyên tử:
Trong nguyên tử, các electron trên các obitan khác nhau có cùng mức năng lượng như nhau nếu cùng 1 phân lớp. Các mức năng lượng nguyên tử được sắp xếp theo thứ tự tăng dần.

-
Các electron trong nguyên tử lần lượt chiếm các mức năng lượng từ thấp đến cao khi ở trạng thái cơ bản.
-
Từ trong ra ngoài, mức năng lượng của các lớp e tăng theo thứ tự tăng dần từ 1 đến 7 và năng lượng của phân lớp theo thứ tự là s, p, d, f. (1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d 6p 7s 5f 6d 7p)
-
Khi điện tích hạt nhân tăng, có sự chèn mức năng lượng vì vậy mức năng lượng 4s thấp hơn 3d.
Cách viết cấu hình electron nguyên tử: Quy tắc và các bước cần nhớ
Để viết cấu hình e nguyên tử chính xác, bạn cần nắm chắc những quy tắc và các bước cần nhớ sau đây:
Quy tắc viết cấu hình e nguyên tử
Trong quy ước cách viết cấu hình electron nguyên tử:
-
Số thứ tự lớp electron được biểu thị bằng các chữ số: 1, 2, 3
-
Phân lớp được kí hiệu bằng các chữ cái thường: s, p, d, f
-
Số electron trong phân lớp được biểu thị bằng chỉ số ở phía trên bên phải kí hiệu của phân lớp: Ví dụ: s2, p6, d10…

Cấu hình electron nguyên tử được viết theo quy tắc nào?
-
Xác định được số electron của nguyên tử: Các e được phân bố lần lượt vào các phân lớp theo chiều tăng dần của năng lượng trong nguyên tử và tuân theo quy tắc: Phân lớp s chứa tối đa 2 electron; phân lớp p chứa tối đa 6 electron, phân lớp d chứa tối đa 10 electron; phân lớp f chứa tối đa 14 electron.
-
Nguyên lý và quy tắc cần nhớ: Các e được phân bố theo thứ tự tăng dần các mức năng lượng AO (mức năng lượng obitan nguyên tử), tuân theo quy tắc các nguyên lí Pau-li, nguyên lí vững bền và quy tắc Hun.
Nguyên lý Pauli: Trên mỗi obital nguyên tử chỉ có thể chứa tối đa 2 electron. 2 electron này chuyển động tự quay khác chiều nhau xung quanh trục riêng của mỗi electron.
Quy tắc Hund: Trong cùng một phân lớp, các electron sẽ phân bố trên các obital sao cho số electron độc thân là tối đa. Các electron này phải có chiều tự quay giống nhau.
Nguyên lý vững bền: Ở trạng thái cơ bản, trong nguyên tử các electron lần lượt chiếm các obital có mức năng lượng tăng dần từ thấp đến cao.
Viết cấu hình electron
Cấu hình e được viết theo thứ tự các phân lớp trong 1 lớp và theo thứ tự của các lớp electron.
Bên cạnh đó, bạn cần chú ý: Các electron được phân bố vào các AO theo phân mức năng lượng tăng dần và có sự chèn mức năng lượng. Tuy nhiên, khi viết cấu hình e, các phân mức năng lượng cần được sắp xếp lại theo từng lớp.
Ví dụ:
Nguyên tử Fe có Z= 26. Như vậy, trong nguyên tử Fe có:
-
26 electron
-
Các electron được phân bố: 1s2 2s2 2p6 3s2 3p6 4s2 3d6 và có sự chèn mức năng lượng 4s < 3d
-
Sắp xếp lại các phân lớp theo từng lớp, ta được cấu hình electron: 1s2 2s2 2p6 3s2 3p6 3d6 4s2
Hoặc viết gọn là: [Ar] 3d6 4s2 (Trong đó, [Ar] là cấu hình electron nguyên tử của nguyên tố argon - khí hiếm gần nhất đứng trước Fe)
3 bước viết cấu hình e nguyên tử dễ nhớ
Sau khi nắm được đầy đủ lý thuyết của cấu hình electron nguyên tử, sau đây là 3 bước viết cấu hình e đơn giản và dễ nhớ nhất:
-
Bước 1: Xác định số electron của nguyên tử (Z).
-
Bước 2: Sắp xếp các electron theo thứ tự tăng dần mức năng lượng theo quy tắc đã học: 1s 2s 2p 3s 3p 4s 3d 4p 5s…
-
Bước 3: Viết cấu hình e: Sắp xếp theo thứ tự từng lớp (1→7), trong mỗi lớp sắp xếp theo thứ tự từng phân lớp (s→p→d→f). Ví dụ: 1s 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s…

Một số lưu ý khi viết cấu hình electron:
-
Cần xác định đúng số e của nguyên tử hay ion (Số electron(e) = số proton(n) = Z).
-
Nắm vững các nguyên lý và quy tắc, kí hiệu của lớp và phân lớp.
-
Quy tắc bão hòa và bán bão hòa trên d và cấu hình e bền khi các e điền vào phân lớp 4 đạt bão hòa (d, f) hoặc bán bão hòa (d, f).
Ví dụ:
Viết cấu hình e nguyên tử của các nguyên tố sau: Na (Z=11):
- Bước 1: Xác định E=Z=11
- Bước 2: Sắp xếp các e theo thứ tự tăng dần: 1s2 2s2 2p6 3s1
- Bước 3: Viết cấu hình e: 1s2 2s2 2p6 3s1
Tương tự:
- Nguyên tử Hidro có Z = 1, có 1e. Cấu hình electron của nguyên tử H là: 1s1 Nguyên tử Heli có Z = 2, có 2e. Cấu hình electron của nguyên tử H là 1s2, đã bão hòa.
- Nguyên tử Liti có Z = 3, có 3e. Cấu hình electron của nguyên tử H là: 1s22s1. E cuối cùng của nguyên tử liti điền vào phân lớp s. Liti là nguyên tố s.
- Nguyên tử Neon có Z = 10, có 10e. Cấu hình electron của nguyên tử Ne là 1s22s22p6.
- Nguyên tử Clo có Z = 17, có 17e = Cấu hình electron của nguyên tử Cl là 1s22s22p63s23p5. Cấu hình e viết gọn là [Ne]3s23p.
- Electron cuối cùng của Clo điền vào phân lớp p. Clo là nguyên tố p.
- Trong đó, [Ne] là ký hiệu cấu hình e của nguyên tử Neon, là khí hiếm gần nhất đứng trước Clo.
- Nguyên tử sắt Fe có Z = 26, có 26 = Cấu hình electron của nguyên tử Fe là 1s22s22p63s23p64s23d6. Cấu hình e viết gọn là [Ar]3d64s2.
- Electron cuối cùng của Fe điền vào phân lớp d. Sắt (Fe) là nguyên tố d.
Như vậy, các nguyên tố s, p, d, f được xác định như sau:
- Nguyên tố s: Là nguyên tố mà nguyên tử có electron cuối cùng điền vào phân lớp s.
- Nguyên tố p: Là nguyên tố mà nguyên tử có electron cuối cùng điền vào phân lớp p.
- Nguyên tố d: Là nguyên tố mà nguyên tử có electron cuối cùng điền vào phân lớp d.
- Nguyên tố f : Là nguyên tố mà nguyên tử có electron cuối cùng điền vào phân lớp f.
* Lưu ý đối với các nguyên tố có cấu hình nguyên tử bán bão hòa:
- Cr (Z = 24) 1s22s22p63s23p63do4s2 chuyển thành 1s22s22p63s23p63d54s1.
- Cu (Z = 29) 1s22s22p63s23p63d4s2 chuyển thành 1s22s22p63s23p63d104s.
Xem thêm:
- Nhóm halogen là gì? Vị trí, đặc điểm, tính chất, cấu hình electron
- Tinh thể nguyên tử và tinh thể phân tử: Khái niệm, tính chất và bài tập thực hành
Bảng cấu hình electron nguyên tử của 20 nguyên tố đầu tiên
Sau đây là bảng cấu hình electron nguyên tử của 20 nguyên tố đầu tiên bạn cần nhớ để có thể giải thành thạo các bài tập cấu hình electron nguyên tử lớp 10.
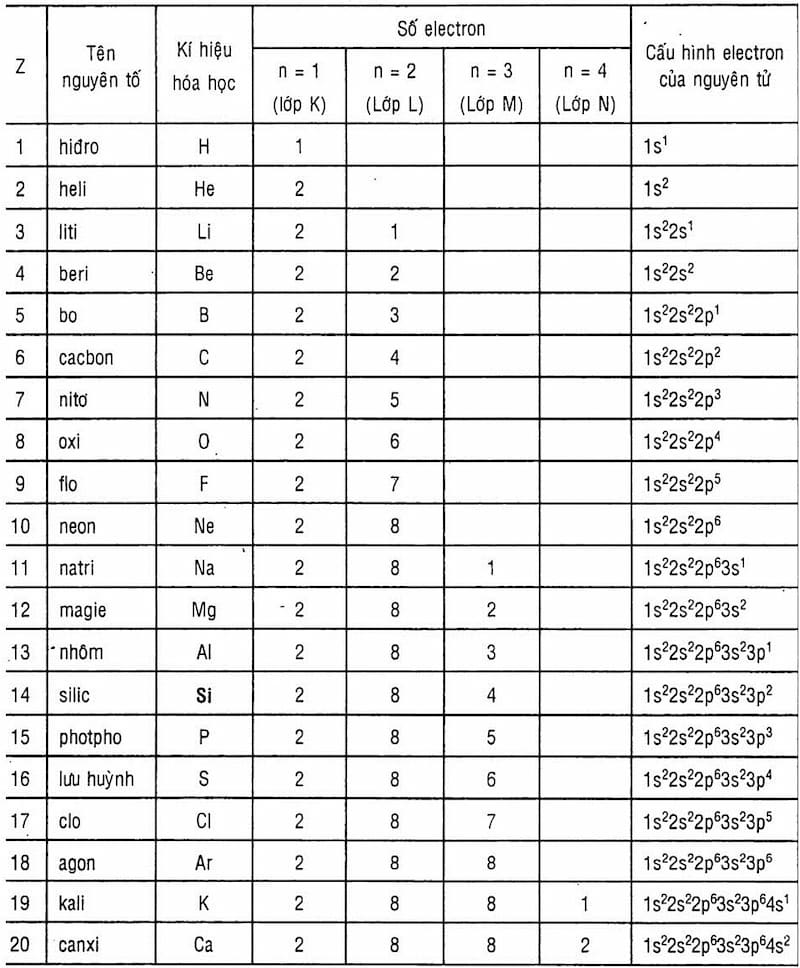
Đặc điểm lớp electron ngoài cùng
Các electron ở lớp ngoài cùng quyết định tính chất hóa học của một nguyên tố. Đối với nguyên tử của tất cả các nguyên tố, lớp electron ngoài cùng có những đặc điểm chung sau đây:
-
Có nhiều nhất là 8 electron.
-
Các nguyên tử có 8e lớp ngoài cùng (ns2np6) và nguyên tử Heli (1s2) đều rất bền và hầu như không tham gia vào các phản ứng hóa học.
-
Các nguyên tử có 1, 2, 3 e lớp ngoài cùng không tham gia vào các phản ứng hóa học (trừ 1 số điều kiện đặc biệt) vì cấu hình electron của các nguyên tử này rất bền. Đó là các nguyên tố khí hiếm chỉ có một nguyên tử.
-
Các nguyên tử có 1, 2, 3 electron ở lớp ngoài cùng dễ nhường electron là nguyên tử của các nguyên tố kim loại, ngoại trừ H, He và B.
-
Các nguyên tử có 5, 6, 7 electron ở lớp ngoài cùng dễ nhận electron thường là nguyên tử của nguyên tố phi kim.
-
Các nguyên tử có 4 electron ngoài cùng có thể là nguyên tử của nguyên tố kim loại hoặc phi kim.
Như vậy, khi biết cấu hình electron của nguyên tử có thể giúp chúng ta dự đoán được loại nguyên tố.
Bài tập về cấu hình e nguyên tử SGK Hóa học 10 kèm lời giải
Sau khi nắm được toàn bộ lý thuyết và cách viết cấu hình e đơn giản nhất, hãy vận dụng chúng để thực hành một số bài tập cấu hình electron nguyên tử dưới đây.

Bài tập 1.(Trang 27 SGK hóa học 10)
Nguyên tố có z = 11 thuộc loại nguyên tố :
A. s B. p C.d D.f
Chọn đáp án đúng.
Gợi ý đáp án: A là đáp án đúng.
Nguyên tố Z=11, ta có cấu hình electron của nguyên tố đó như sau: 1s22s22p63s1. Vậy nguyên tố đã cho là s. Đáp án đúng là A.
Bài tập 2.(Trang 27 SGK hóa học 10)
Cấu hình electron nguyên tử nào sau đây là của lưu huỳnh (Z = 16) :
A. 1s2 2s2 2p5 3s2 3p5 ; B. 1 s2 2s1 2p6 3s2 3p6 ;
C. 1s2 2s2 2p6 3s2 3p4 ; D. 1 s2 2s2 2p6 3s2 3p3.
Chọn đáp án đúng.
Gợi ý đáp án: Đáp án đúng là C
Nguyên tử lưu huỳnh có Z=16 có cấu hình là: 1s22s22p63s23p4
Bài tập 3.(Trang 28 SGK hóa học 10)
Cấu hình electron của nguyên tử nhôm (Z = 13) là 1s22s22p63s23p1. Vậy :
A. Lớp thứ nhất (Lớp K) có 2 electron ;
B. Lớp thứ hai (Lớp L) có 8 electron ;
C. Lớp thứ ba (Lớp M) có 3 electron ;
D. Lớp ngoài cùng có 1 electron.
Tìm câu sai.
Gợi ý đáp án: D là đáp án sai.
Bài tập 4.(Trang 28 SGK hóa học 10)
Tổng số hạt proton, notron và electron trong nguyên tử của một nguyên tố là 13.
a) Xác định nguyên tử khối.
b) Viết cấu hình electron nguyên tử của nguyên tố đó.
(Cho biết : các nguyên tố có số hiệu nguyên tử từ 2 đến 82 trong N bảng tuần hoàn thì 1 ≤ N/Z ≤ 1,5)
Gợi ý đáp án:
a) Tổng số hạt proton, nơtron, electron trong 1 nguyên tử của nguyên tố đã cho là 13. Số proton bằng số electron nên ta có phương trình: 2Z + N =13
Mặt khác từ nguyên tố số 2 đến 82 trong bảng tuần ta có :
Z ≤ N; mà N =13 – 2Z ⇒ Z ≤ 13 – 2Z ⇒ Z ≤ 4,333 (1)
N ≤ 1,5Z ⇒ 13-2Z ≤ 1,5Z ⇒ 3,5Z ≥ 13 ⇒ Z ≥ 3,7 (2)
Từ (1) và (2) và vì Z nguyên dương 3,7 ≤ Z ≤ 4,333 . vậy Z =4
Suy ra số nơtron: N =13 – 2Z = 13 -2.4 = 5
Vậy nguyên tử khối cần tìm theo yêu cầu bài toán là 4+5=9.
b) Viết cấu hình electron: Z=4 có cấu hình là 1s22s2. Đây là nguyên tố s
Bài tập 5.(Trang 28 SGK hóa học 10)
Có bao nhiêu electron ở lớp ngoài cùng trong nguyên tử của các nguyên tố có số hiệu nguyên tử lần lượt bằng 3, 6, 9, 18?
Gợi ý đáp án:
Số electron lớp ngoài cùng trong nguyên tử của các nguyên tố có số hiệu nguyên tử bằng 3, 6, 9, 18 lần lượt là 1, 4, 7, 8. Do các nguyên tử có cấu hình electron như sau :
z = 3: 1s2 2s1 ; z = 6: 1s2 2s2 2p2 ;
z = 9: 1s2 2s2 2p5 ; z = 18: 1s2 2s2 2p6 3s2 3p6.
Như vậy, bài viết này của Monkey đã cung cấp cho bạn toàn bộ lý thuyết về cấu hình electron nguyên tử cùng 3 bước viết cấu hình e đơn giản và dễ nhớ nhất. Hy vọng qua những thông tin trên, bạn có thể vận dụng giải thành thạo các bài tập như viết cấu hình e, xác định số lớp e, v.v... và đạt điểm cao trong các bài thi.
Chia sẻ bài viết và đừng quên truy cập chuyên mục Kiến thức cơ bản trên website của Monkeymỗi ngày để có thêm nhiều kiến thức Hóa học bổ ích khác!
Từ khóa » E Cuối Cùng Là Gì
-
Chuyên đề Vai Trò Và ý Nghĩa Của Electron (ngoài Cùng, Cuối Cùng ...
-
Cấu Hình Electron Nguyên Tử - Thầy Phạm Ngọc Dũng Dạy HÓA
-
Cấu Hình Electron – Wikipedia Tiếng Việt
-
Cấu Hình Electron - Hóa
-
Electron Cuối Cùng Của Nguyên Tử Nguyên Tố X Phân Bố Vào Phân ...
-
Electron Cuối Cùng Phân Bố Trong Nguyên Tử X Là 3d8. Số ... - Hoc247
-
Viết Cấu Hình E Của D( Số Electron Cuối Cùng điền Vào Phân Lớp 4s1?
-
Chất Nhận Electron Cuối Cùng Của Quá Trình Quang Hợp Là Gì?
-
Chương 1. Nguyên Tử - Hoc24
-
Bài 5. Cấu Hình Electron Nguyên Tử - Củng Cố Kiến Thức
-
Giá Trị Cuối Cùng Là Gì? Phân Loại, Cách Tính Terminal Value?
-
Người Tiêu Thụ Cuối Cùng Là Gì? Mô Hình Giải Thích Hành Vi Mua Sắm
-
Lý Thuyết, Cách Viết Cấu Hình Electron Nguyên Tử Và Bài Tập Vận ...