40 Bài Tập Về Axit Phophoric Tác Dụng Với Dung Dịch Kiềm Có Lời Giải ...
Có thể bạn quan tâm

- Lớp 12
-
 Ngữ văn 12
Ngữ văn 12 - Soạn văn - Kết nối tri thức
- Soạn văn - Cánh diều
- Soạn văn - Chân trời sáng tạo
- Tác giả tác phẩm
- Tóm tắt, bố cục Văn - Kết nối tri thức
- Tóm tắt, bố cục Văn - Cánh diều
- Tóm tắt, bố cục Văn - Chân trời sáng tạo
- SBT Văn - Kết nối tri thức
- >> Xem thêm
-
 Toán học 12
Toán học 12 - SGK Toán - Kết nối tri thức
- SGK Toán - Cánh diều
- SGK Toán - Chân trời sáng tạo
- SGK Toán - Cùng khám phá
- SBT Toán - Kết nối tri thức
- SBT Toán - Cánh diều
- SBT Toán - Chân trời sáng tạo
- Chuyên đề học tập Toán - Kết nối tri thức
- >> Xem thêm
-
 Tiếng Anh 12
Tiếng Anh 12 - Tiếng Anh - Global Success
- Tiếng Anh - Friends Global
- Tiếng Anh - iLearn Smart World
- Tiếng Anh - Bright
- Tiếng Anh - English Discovery
- SBT Global Success
- SBT Friends Global
- SBT iLearn Smart World
- >> Xem thêm
-
 Vật lí 12
Vật lí 12 - SGK Vật Lí - Kết nối tri thức
- SGK Vật Lí - Cánh diều
- SGK Vật Lí - Chân trời sáng tạo
- SBT Vật lí - Kết nối tri thức
- SBT Vật lí - Cánh diều
- SBT Vật lí - Chân trời sáng tạo
- Chuyên đề học tập Lí - Kết nối tri thức
- Chuyên đề học tập Lí - Cánh diều
- >> Xem thêm
-
 Hóa học 12
Hóa học 12 - SGK Hóa - Kết nối tri thức
- SGK Hóa - Cánh diều
- SGK Hóa - Chân trời sáng tạo
- SBT Hóa - Kết nối tri thức
- SBT Hóa - Cánh diều
- SBT Hóa - Chân trời sáng tạo
- Chuyên đề học tập Hóa - Kết nối tri thức
- Chuyên đề học tập Hóa - Cánh diều
- >> Xem thêm
-
 Sinh học 12
Sinh học 12 - SGK Sinh - Kết nối tri thức
- SGK Sinh - Cánh diều
- SGK Sinh - Chân trời sáng tạo
- Trắc nghiệm Sinh - Kết nối tri thức
- Trắc nghiệm Sinh - Cánh diều
- Trắc nghiệm Sinh - Chân trời sáng tạo
- Chuyên đề học tập Sinh - Kết nối tri thức
- Chuyên đề học tập Sinh - Cánh diều
- >> Xem thêm
-
 Lịch sử 12
Lịch sử 12 - SGK Lịch sử - Kết nối tri thức
- SGK Lịch sử - Chân trời sáng tạo
- SGK Lịch sử - Cánh diều
- SBT Lịch sử - Cánh diều
- Đề thi, đề kiểm tra Lịch sử - Kết nối tri thức
- Đề thi, đề kiểm tra Lịch sử - Chân trời sáng tạo
- Đề thi, đề kiểm tra Lịch sử - Cánh diều
- Chuyên đề học tập Lịch sử - Kết nối tri thức
- >> Xem thêm
-
 Địa lí 12
Địa lí 12 - SGK Địa lí - Kết nối tri thức
- SGK Địa lí - Chân trời sáng tạo
- SGK Địa lí - Cánh diều
- SBT Địa lí - Cánh diều
- Đề thi, đề kiểm tra Địa lí - Kết nối tri thức
- Đề thi, đề kiểm tra Địa lí - Chân trời sáng tạo
- Đề thi, đề kiểm tra Địa lí - Cánh diều
- SBT Địa lí - Chân trời sáng tạo
- >> Xem thêm
- GD kinh tế và pháp luật 12
- SGK Giáo dục kinh tế và pháp luật - Kết nối tri thức
- SGK Giáo dục kinh tế và pháp luật - Chân trời sáng tạo
- SGK Giáo dục kinh tế và pháp luật - Cánh diều
- SBT Giáo dục kinh tế và pháp luật - Cánh diều
- SBT Giáo dục kinh tế và pháp luật - Chân trời sáng tạo
- Chuyên đề học tập Giáo dục kinh tế pháp luật - Kết nối tri thức
- Chuyên đề học tập Giáo dục kinh tế pháp luật - Cánh diều
- Chuyên đề học tập Giáo dục kinh tế pháp luật - Chân trời sáng tạo
-
 Công nghệ 12
Công nghệ 12 - SGK Công nghệ - Kết nối tri thức
- SGK Công nghệ - Cánh diều
- Chuyên đề học tập Công nghệ - Kết nối tri thức
- Chuyên đề học tập Công nghệ - Cánh diều
-
 Tin học 12
Tin học 12 - SGK Tin học - Cánh diều
- SGK Tin học - Chân trời sáng tạo
- SGK Tin học - Kết nối tri thức
- SBT Tin học - Kết nối tri thức
- SBT Tin học - Cánh diều
- SBT Tin học - Chân trời sáng tạo
- Chuyên đề học tập Tin - Kết nối tri thức
- Chuyên đề học tập Tin - Chân trời sáng tạo
- >> Xem thêm
-
 HĐ trải nghiệm, hướng nghiệp 12
HĐ trải nghiệm, hướng nghiệp 12 - SGK Hoạt động trải nghiệm, hướng nghiệp - Kết nối tri thức
- SGK Hoạt động trải nghiệm, hướng nghiệp - Cánh diều
- SGK Hoạt động trải nghiệm, hướng nghiệp - Chân trời sáng tạo Bản 1
- SGK Hoạt động trải nghiệm, hướng nghiệp - Chân trời sáng tạo Bản 2
- GD Quốc phòng và An ninh 12
- SGK Giáo dục quốc phòng và an ninh - Kết nối tri thức
- SGK Giáo dục quốc phòng và an ninh - Cánh diều
- Giáo dục thể chất 12
- SGK Giáo dục thể chất - Kết nối tri thức
- SGK Giáo dục thể chất - Cánh diều
- Giáo dục địa phương 12
- Tài liệu Giáo dục địa phương
- Đề thi, đề kiểm tra 12
- Tổng hợp đề thi, đề kiểm tra
-
- Lớp 11
-
 Ngữ văn 11
Ngữ văn 11 - Soạn văn - Kết nối tri thức - chi tiết
- Soạn văn - Kết nối tri thức - siêu ngắn
- Soạn văn - Cánh Diều - chi tiết
- Soạn văn - Cánh Diều - siêu ngắn
- Soạn văn - Chân trời sáng tạo - chi tiết
- Soạn văn - Chân trời sáng tạo - siêu ngắn
- Tác giả tác phẩm
- Tóm tắt, bố cục Văn - Kết nối tri thức
- >> Xem thêm
-
 Toán học 11
Toán học 11 - SGK Toán - Kết nối tri thức
- SGK Toán - Cánh diều
- SGK Toán - Chân trời sáng tạo
- SGK Toán - Cùng khám phá
- Chuyên đề học tập Toán - Kết nối tri thức
- Chuyên đề học tập Toán - Cánh diều
- Chuyên đề học tập Toán - Chân trời sáng tạo
- SBT Toán - Kết nối tri thức
- >> Xem thêm
-
 Tiếng Anh 11
Tiếng Anh 11 - Tiếng Anh - Global Success
- Tiếng Anh - Friends Global
- Tiếng Anh - iLearn Smart Wolrd
- Tiếng Anh - Bright
- Tiếng Anh - English Discovery
- SBT Global Success
- SBT Friends Global
- SBT iLearn Smart World
- >> Xem thêm
-
 Vật lí 11
Vật lí 11 - SGK Vật Lí - Kết nối tri thức
- SGK Vật Lí - Cánh diều
- SGK Vật Lí - Chân trời sáng tạo
- Chuyên đề học tập Lí - Kết nối tri thức
- Chuyên đề học tập Lí - Cánh diều
- Chuyên đề học tập Lí - Chân trời sáng tạo
- SBT Vật lí - Kết nối tri thức
- SBT Vật lí - Cánh diều
- >> Xem thêm
-
 Hóa học 11
Hóa học 11 - SGK Hóa học - Kết nối tri thức
- SGK Hóa học - Cánh diều
- SGK Hóa học - Chân trời sáng tạo
- Chuyên đề học tập Hóa - Kết nối tri thức
- Chuyên đề học tập Hóa - Cánh diều
- Chuyên đề học tập Hóa - Chân trời sáng tạo
- SBT Hóa - Kết nối tri thức
- SBT Hóa - Cánh diều
- >> Xem thêm
-
 Sinh học 11
Sinh học 11 - SGK Sinh - Kết nối tri thức
- SGK Sinh - Cánh diều
- SGK Sinh - Chân trời sáng tạo
- Chuyên đề học tập Sinh - Kết nối tri thức
- Chuyên đề học tập Sinh - Cánh diều
- Chuyên đề học tập Sinh - Chân trời sáng tạo
- SBT Sinh - Kết nối tri thức
- SBT Sinh - Cánh diều
- >> Xem thêm
-
 HĐ trải nghiệm, hướng nghiệp 11
HĐ trải nghiệm, hướng nghiệp 11 - SBT Hoạt động trải nghiệm - Kết nối tri thức
- SGK Hoạt động trải nghiệm, hướng nghiệp - Kết nối tri thức
- SGK Hoạt động trải nghiệm, hướng nghiệp - Cánh diều
- SGK Hoạt động trải nghiệm, hướng nghiệp - Chân trời sáng tạo Bản 1
- SGK Hoạt động trải nghiệm, hướng nghiệp - Chân trời sáng tạo Bản 2
- SBT Hoạt động trải nghiệm - Cánh diều
- SBT Hoạt động trải nghiệm - Chân trời sáng tạo (Bản 1)
- SBT Hoạt động trải nghiệm - Chân trời sáng tạo (Bản 2)
-
 Lịch sử 11
Lịch sử 11 - SGK Lịch sử - Kết nối tri thức
- SGK Lịch sử - Chân trời sáng tạo
- SGK Lịch sử - Cánh diều
- SBT Lịch sử - Kết nối tri thức
- SBT Lịch sử - Chân trời sáng tạo
- SBT Lịch sử - Cánh diều
- Đề thi, đề kiểm tra Lịch sử - Kết nối tri thức
- Đề thi, đề kiểm tra Lịch sử - Chân trời sáng tạo
- >> Xem thêm
-
 Địa lí 11
Địa lí 11 - SGK Địa lí - Kết nối tri thức
- SGK Địa lí - Chân trời sáng tạo
- SGK Địa lí - Cánh diều
- SBT Địa lí - Kết nối tri thức
- SBT Địa lí - Chân trời sáng tạo
- SBT Địa lí - Cánh diều
- Đề thi, đề kiểm tra Địa lí - Kết nối tri thức
- Đề thi, đề kiểm tra Địa lí - Chân trời sáng tạo
- >> Xem thêm
- GD kinh tế và pháp luật 11
- SGK Giáo dục kinh tế và pháp luật - Kết nối tri thức
- SGK Giáo dục kinh tế và pháp luật - Chân trời sáng tạo
- SGK Giáo dục kinh tế và pháp luật - Cánh diều
- SBT Giáo dục kinh tế và pháp luật - Kết nối tri thức
- SBT Giáo dục kinh tế và pháp luật - Chân trời sáng tạo
- SBT Giáo dục kinh tế và pháp luật - Cánh diều
- Chuyên đề học tập Giáo dục kinh tế pháp luật - Kết nối tri thức
- Chuyên đề học tập Giáo dục kinh tế pháp luật - Chân trời sáng tạo
- >> Xem thêm
-
 Công nghệ 11
Công nghệ 11 - SGK Công nghệ - Kết nối tri thức
- SGK Công nghệ - Cánh diều
-
 Tin học 11
Tin học 11 - SGK Tin học - Kết nối tri thức
- SGK Tin học - Cánh diều
- SBT Tin học - Kết nối tri thức
- SBT Tin học - Cánh diều
- Chuyên đề học tập Tin - Kết nối tri thức
- Chuyên đề học tập Tin - Cánh diều
- Giáo dục thể chất 11
- SGK Giáo dục thể chất - Kết nối tri thức
- SGK Giáo dục thể chất - Cánh diều
- GD Quốc phòng và An ninh 11
- SGK Giáo dục quốc phòng và an ninh - Kết nối tri thức
- SGK Giáo dục quốc phòng và an ninh - Cánh diều
- Giáo dục địa phương 11
- Tài liệu Giáo dục địa phương
- Đề thi, đề kiểm tra 11
- Tổng hợp đề thi, đề kiểm tra
-
- Lớp 10
-
 Ngữ văn 10
Ngữ văn 10 - Soạn văn - Kết nối tri thức - siêu ngắn
- Soạn văn - Kết nối tri thức - chi tiết
- Soạn văn - Chân trời sáng tạo - siêu ngắn
- Soạn văn - Chân trời sáng tạo - chi tiết
- Soạn văn - Cánh Diều - siêu ngắn
- Soạn văn - Cánh Diều - chi tiết
- Tác giả tác phẩm
- Tóm tắt, bố cục Văn - Kết nối tri thức
- >> Xem thêm
-
 Toán học 10
Toán học 10 - SGK Toán - Kết nối tri thức
- SGK Toán - Chân trời sáng tạo
- SGK Toán - Cánh diều
- SBT Toán - Kết nối tri thức
- SBT Toán - Chân trời sáng tạo
- SBT Toán - Cánh diều
- Chuyên đề học tập Toán - Kết nối tri thức
- Chuyên đề học tập Toán - Chân trời sáng tạo
- >> Xem thêm
-
 Tiếng Anh 10
Tiếng Anh 10 - Tiếng Anh - Global Success
- Tiếng Anh - Friends Global
- Tiếng Anh - iLearn Smart World
- Tiếng Anh - English Discovery
- Tiếng Anh - Bright
- Tiếng Anh - Explore New Worlds
- SBT Global Success
- SBT Friends Global
- >> Xem thêm
-
 Vật lí 10
Vật lí 10 - SGK Vật Lí - Kết nối tri thức
- SGK Vật Lí - Chân trời sáng tạo
- SGK Vật Lí - Cánh diều
- SBT Vật lí - Kết nối tri thức
- SBT Vật lí - Chân trời sáng tạo
- SBT Vật lí - Cánh diều
- Trắc nghiệm Lí - Kết nối tri thức
- Bài tập trắc nghiệm Lí - Kết nối tri thức
- >> Xem thêm
-
 Hóa học 10
Hóa học 10 - SGK Hóa - Kết nối tri thức
- SGK Hóa - Chân trời sáng tạo
- SGK Hóa - Cánh diều
- SBT Hóa - Kết nối tri thức
- SBT Hóa - Chân trời sáng tạo
- SBT Hóa 10 - Cánh diều
- Chuyên đề học tập Hóa - Kết nối tri thức
- Chuyên đề học tập Hóa 10 – Chân trời sáng tạo
- >> Xem thêm
-
 Sinh học 10
Sinh học 10 - SGK Sinh - Kết nối tri thức
- SGK Sinh - Chân trời sáng tạo
- SGK Sinh - Cánh diều
- SBT Sinh - Kết nối tri thức
- SBT Sinh - Chân trời sáng tạo
- SBT Sinh - Cánh diều
- Chuyên đề học tập Sinh - Kết nối tri thức
- Chuyên đề học tập Sinh - Chân trời sáng tạo
- >> Xem thêm
-
 Lịch sử 10
Lịch sử 10 - SGK Lịch sử - Kết nối tri thức
- SGK Lịch sử - Chân trời sáng tạo
- SGK Lịch sử - Cánh Diều
- SBT Lịch sử - Kết nối tri thức
- SBT Lịch sử - Chân trời sáng tạo
- SBT Lịch sử - Cánh Diều
- Chuyên đề học tập Lịch sử - Kết nối tri thức
- Trắc nghiệm Sử - kết nối tri thức
- >> Xem thêm
-
 Địa lí 10
Địa lí 10 - SGK Địa lí - Kết nối tri thức
- SGK Địa lí - Cánh Diều
- SGK Địa lí - Chân trời sáng tạo
- SBT Địa lí - Kết nối tri thức
- SBT Địa lí - Chân trời sáng tạo
- Trắc nghiệm Địa lí - Kết nối tri thức
- Trắc nghiệm Địa lí - Chân trời sáng tạo
- Trắc nghiệm Địa lí - Cánh Diều
- >> Xem thêm
-
 Tin học 10
Tin học 10 - SGK Tin học - Kết nối tri thức
- SGK Tin học - Cánh Diều
- SBT Tin học - Kết nối tri thức
- SBT Tin học 10 - Cánh diều
-
 Công nghệ 10
Công nghệ 10 - SGK Công nghệ - Kết nối tri thức
- SGK Công nghệ - Cánh diều
- Chuyên đề học tập Công nghệ - Kết nối tri thức
- Chuyên đề học tập Công nghệ - Cánh diều
- GD kinh tế và pháp luật 10
- SGK Giáo dục kinh tế và pháp luật - KNTT
- SGK Giáo dục kinh tế và pháp luật - CTST
- SGK Giáo dục kinh tế và pháp luật - Cánh diều
- SBT Giáo dục kinh tế và pháp luật - Kết nối tri thức
- SBT Giáo dục kinh tế và pháp luật - Chân trời sáng tạo
- SBT Giáo dục kinh tế và pháp luật - Cánh diều
- Chuyên đề học tập Giáo dục kinh tế pháp luật - Kết nối tri thức
- Chuyên đề học tập Giáo dục kinh tế pháp luật - Chân trời sáng tạo
- >> Xem thêm
-
 HĐ trải nghiệm, hướng nghiệp 10
HĐ trải nghiệm, hướng nghiệp 10 - SGK Hoạt động trải nghiệm, hướng nghiệp - Kết nối tri thức
- SGK Hoạt động trải nghiệm, hướng nghiệp - Chân trời sáng tạo
- SGK Hoạt động trải nghiệm, hướng nghiệp - Cánh Diều
- SBT Hoạt động trải nghiệm - Kết nối tri thức
- SBT Hoạt động trải nghiệm - Cánh diều
- SBT Hoạt động trải nghiệm - Chân trời sáng tạo (Bản 1)
- SBT Hoạt động trải nghiệm - Chân trời sáng tạo (Bản 2)
- Giáo dục thể chất 10
- SGK Giáo dục thể chất - Kết nối tri thức
- SGK Giáo dục thể chất - Cánh diều
- GD Quốc phòng và An ninh 10
- SGK Giáo dục quốc phòng và an ninh - Kết nối tri thức
- SGK Giáo dục quốc phòng và an ninh - Cánh diều
- Giáo dục địa phương 10
- Tài liệu Giáo dục địa phương
- Đề thi, đề kiểm tra 10
- Tổng hợp đề thi, đề kiểm tra
-
- Lớp 9
-
 Toán học 9
Toán học 9 - SGK Toán - Kết nối tri thức
- SGK Toán - Chân trời sáng tạo
- SGK Toán - Cánh diều
- SGK Toán - Cùng khám phá
- SBT Toán - Kết nối tri thức
- SBT Toán - Chân trời sáng tạo
- SBT Toán - Cánh diều
- Vở thực hành Toán
- >> Xem thêm
-
 Ngữ văn 9
Ngữ văn 9 - Soạn văn - Kết nối tri thức
- Soạn văn - Chân trời sáng tạo
- Soạn văn - Cánh diều
- Tác giả - Tác phẩm văn
- Tóm tắt, bố cục Văn - Kết nối tri thức
- Tóm tắt, bố cục Văn - Chân trời sáng tạo
- Tóm tắt, bố cục Văn - Cánh diều
- SBT Văn - Kết nối tri thức
- >> Xem thêm
-
 Tiếng Anh 9
Tiếng Anh 9 - Tiếng Anh - Global Success
- Tiếng Anh - Friends Plus
- Tiếng Anh - iLearn Smart World
- Tiếng Anh - Right on!
- Tiếng Anh - English Discovery
- SBT Global Success
- SBT Friends Plus
- SBT iLearn Smart World
- >> Xem thêm
-
 Khoa học tự nhiên 9
Khoa học tự nhiên 9 - SGK Khoa học tự nhiên - Kết nối tri thức
- SGK Khoa học tự nhiên - Cánh diều
- SGK Khoa học tự nhiên 9 Chân trời sáng tạo
- SBT KHTN - Kết nối tri thức
- SBT KHTN - Cánh diều
- SBT KHTN - Chân trời sáng tạo
- Trắc nghiệm KHTN - Kết nối tri thức
- Trắc nghiệm KHTN - Cánh diều
- >> Xem thêm
-
 Lịch sử và Địa lí 9
Lịch sử và Địa lí 9 - SGK Lịch sử và Địa lí - Kết nối tri thức
- SGK Lịch sử và Địa lí - Cánh diều
- SGK Lịch sử và Địa lí - Chân trời sáng tạo
- SBT Lịch sử - Cánh diều
- SBT Địa lí - Kết nối tri thức
- SBT Địa lí - Chân trời sáng tạo
- SBT Đia lí - Cánh diều
- Đề thi, kiểm tra Lịch Sử và Địa lí - Kết nối tri thức
- >> Xem thêm
-
 GDCD 9
GDCD 9 - Giáo dục công dân - Kết nối tri thức
- Giáo dục công dân - Chân trời sáng tạo
- Giáo dục công dân - Cánh diều
- SBT GDCD - Chân trời sáng tạo
- SBT GDCD - Cánh diều
-
 Tin học 9
Tin học 9 - SGK Tin học - Kết nối tri thức
- SGK Tin học - Cánh diều
- SGK Tin học - Chân trời sáng tạo
- SBT Tin học - Kết nối tri thức
- SBT Tin học - Chân trời sáng tạo
- SBT Tin học - Cánh diều
-
 Công nghệ 9
Công nghệ 9 - SGK Công nghệ - Kết nối tri thức
- SGK Công nghệ - Chân trời sáng tạo
- SGK Công nghệ - Cánh diều
- SBT Công nghệ - Cánh diều
-
 HĐ trải nghiệm, hướng nghiệp 9
HĐ trải nghiệm, hướng nghiệp 9 - SGK Hoạt động trải nghiệm, hướng nghiệp - Kết nối tri thức
- SGK Hoạt động trải nghiệm, hướng nghiệp - Cánh diều
- SGK Hoạt động trải nghiệm, hướng nghiệp - Chân trời sáng tạo Bản 1
- SGK Hoạt động trải nghiệm, hướng nghiệp - Chân trời sáng tạo Bản 2
- Giáo dục địa phương 9
- Tài liệu Giáo dục địa phương
- Đề thi, đề kiểm tra 9
- Tổng hợp đề thi, đề kiểm tra
- Tổng hợp đề thi vào 10
-
- Lớp 8
-
 Ngữ văn 8
Ngữ văn 8 - Soạn văn chi tiết - KNTT
- Soạn văn siêu ngắn - KNTT
- Soạn văn chi tiết - CTST
- Soạn văn siêu ngắn - CTST
- Soạn văn chi tiết - Cánh diều
- Soạn văn siêu ngắn - Cánh diều
- Tác giả - Tác phẩm văn
- Tóm tắt, bố cục Văn - Kết nối tri thức
- >> Xem thêm
-
 Toán học 8
Toán học 8 - SGK Toán - Kết nối tri thức
- SGK Toán - Chân trời sáng tạo
- SGK Toán - Cánh diều
- SGK Toán - Cùng khám phá
- SBT Toán - Kết nối tri thức
- SBT Toán - Chân trời sáng tạo
- SBT Toán - Cánh diều
- Vở thực hành Toán
- >> Xem thêm
-
 Tiếng Anh 8
Tiếng Anh 8 - Tiếng Anh - Global Success
- Tiếng Anh - Friends Plus
- Tiếng Anh - iLearn Smart World
- Tiếng Anh - Right on!
- Tiếng Anh - English Discovery
- SBT Global Success
- SBT Friends Plus
- SBT iLearn Smart World
- >> Xem thêm
-
 Khoa học tự nhiên 8
Khoa học tự nhiên 8 - SGK Khoa học tự nhiên - Kết nối tri thức
- SGK Khoa học tự nhiên - Chân trời sáng tạo
- SGK Khoa học tự nhiên - Cánh diều
- SBT KHTN - Kết nối tri thức
- SBT KHTN - Cánh diều
- Vở thực hành Khoa học tự nhiên
- Đề thi, đề kiểm tra KHTN - Kết nối tri thức
- Đề thi, đề kiểm tra KHTN - Cánh diều
- >> Xem thêm
-
 Lịch sử và Địa lí 8
Lịch sử và Địa lí 8 - SGK Lịch sử và Địa lí - Kết nối tri thức
- SGK Lịch sử và Địa lí - Cánh diều
- SGK Lịch sử và Địa lí - Chân trời sáng tạo
- SBT Lịch sử - Kết nối tri thức
- SBT Địa lí - Kết nối tri thức
- SBT Lịch sử - Chân trời sáng tạo
- SBT Địa lí - Chân trời sáng tạo
- SBT Lịch sử - Cánh diều
- >> Xem thêm
-
 GDCD 8
GDCD 8 - Giáo dục công dân - Kết nối tri thức
- Giáo dục công dân - Chân trời sáng tạo
- Giáo dục công dân - Cánh diều
- SBT GDCD - Kết nối tri thức
- SBT GDCD - Chân trời sáng tạo
- SBT GDCD - Cánh diều
-
 Công nghệ 8
Công nghệ 8 - SGK Công nghệ - Kết nối tri thức
- SGK Công nghệ - Chân trời sáng tạo
- SGK Công nghệ - Cánh diều
- SBT Công nghệ - Kết nối tri thức
- SBT Công nghệ - Chân trời sáng tạo
- SBT Công nghệ - Cánh diều
-
 Tin học 8
Tin học 8 - SGK Tin học - Kết nối tri thức
- SGK Tin học - Chân trời sáng tạo
- SGK Tin học - Cánh diều
- SBT Tin học - Kết nối tri thức
- SBT Tin học - Chân trời sáng tạo
- SBT Tin học - Cánh diều
-
 HĐ trải nghiệm, hướng nghiệp 8
HĐ trải nghiệm, hướng nghiệp 8 - SGK Hoạt động trải nghiệm, hướng nghiệp - Kết nối tri thức
- SGK Hoạt động trải nghiệm, hướng nghiệp - Cánh diều
- SGK Hoạt động trải nghiệm, hướng nghiệp - Chân trời sáng tạo Bản 1
- SGK Hoạt động trải nghiệm, hướng nghiệp - Chân trời sáng tạo Bản 2
- SBT Hoạt động trải nghiệm - Kết nối tri thức
- SBT Hoạt động trải nghiệm - Cánh diều
- SBT Hoạt động trải nghiệm - Chân trời sáng tạo (Bản 1)
- SBT Hoạt động trải nghiệm - Chân trời sáng tạo (Bản 2)
-
 Âm nhạc 8
Âm nhạc 8 - SGK Âm nhạc - Kết nối tri thức
- SGK Âm nhạc - Chân trời sáng tạo
- SGK Âm nhạc - Cánh diều
-
 Mỹ thuật 8
Mỹ thuật 8 - SGK Mĩ thuật - Kết nối tri thức
- SGK Mĩ thuật - Chân trời sáng tạo bản 1
- SGK Mĩ thuật - Cánh diều
- SGK Mĩ thuật - Chân trời sáng tạo bản 2
- Giáo dục thể chất 8
- SGK Giáo dục thể chất - Kết nối tri thức
- SGK Giáo dục thể chất - Cánh diều
- SGK Giáo dục thể chất - Chân trời sáng tạo
- Giáo dục địa phương 8
- Đề thi, đề kiểm tra Giáo dục địa phương
- Tài liệu Giáo dục địa phương
- Đề thi, đề kiểm tra 8
- Tổng hợp đề thi, đề kiểm tra
-
- Lớp 7
-
 Ngữ văn 7
Ngữ văn 7 - Soạn văn siêu ngắn - KNTT
- Soạn văn chi tiết - KNTT
- Soạn văn siêu ngắn - CTST
- Soạn văn chi tiết - CTST
- Soạn văn siêu ngắn - Cánh diều
- Soạn văn chi tiết - Cánh diều
- Tác giả - Tác phẩm văn
- Tóm tắt, bố cục Văn - Kết nối tri thức
- >> Xem thêm
-
 Toán học 7
Toán học 7 - SGK Toán - Kết nối tri thức
- SGK Toán - Chân trời sáng tạo
- SGK Toán - Cánh diều
- SBT Toán - Kết nối tri thức
- SBT Toán - Chân trời sáng tạo
- SBT Toán - Cánh diều
- Trắc nghiệm Toán - Kết nối tri thức
- Trắc nghiệm Toán- Chân trời sáng tạo
- >> Xem thêm
-
 Tiếng Anh 7
Tiếng Anh 7 - Tiếng Anh - Global Success
- Tiếng Anh - Friends Plus
- Tiếng Anh - iLearn Smart World
- Tiếng Anh - English Discovery
- Tiếng Anh - Right on!
- SBT Global Success
- SBT Friends Plus
- SBT iLearn Smart World
- >> Xem thêm
-
 Khoa học tự nhiên 7
Khoa học tự nhiên 7 - SGK Khoa học tự nhiên - Kết nối tri thức
- SGK Khoa học tự nhiên - Chân trời sáng tạo
- SGK Khoa học tự nhiên - Cánh diều
- SBT KHTN - Kết nối tri thức
- SBT KHTN - Chân trời sáng tạo
- SBT KHTN - Cánh diều
- Trắc nghiệm KHTN - Kết nối tri thức
- Bài tập trắc nghiệm Khoa học tự nhiên - Kết nối tri thức
- >> Xem thêm
-
 Lịch sử và Địa lí 7
Lịch sử và Địa lí 7 - SGK Lịch sử và Địa lí - Kết nối tri thức
- SGK Lịch sử và Địa lí - Chân trời sáng tạo
- SGK Lịch sử và Địa lí - Cánh Diều
- SBT Lịch sử và Địa lí - Kết nối tri thức
- SBT Lịch sử và Địa lí - Chân trời sáng tạo
- SBT Lịch sử và Địa lí - Cánh diều
- Trắc nghiệm Lịch sử và Địa lí - Kết nối tri thức
- Trắc nghiệm Lịch sử và Địa lí - Chân trời sáng tạo
- >> Xem thêm
-
 Tin học 7
Tin học 7 - SGK Tin học - Kết nối tri thức
- SGK Tin học - Cánh Diều
- SGK Tin học - Chân trời sáng tạo
- SBT Tin học - Kết nối tri thức
- SBT Tin học - Chân trời sáng tạo
- SBT Tin học - Cánh diều
-
 Công nghệ 7
Công nghệ 7 - SGK Công nghệ - Kết nối tri thức
- SGK Công nghệ - Chân trời sáng tạo
- SGK Công nghệ - Cánh diều
- SBT Công nghệ - Kết nối tri thức
- SBT Công nghệ - Chân trời sáng tạo
- SBT Công nghệ - Cánh diều
-
 GDCD 7
GDCD 7 - SGK GDCD - KNTT
- SGK GDCD - CTST
- SGK GDCD - Cánh diều
- Bài tập tình huống GDCD
- SBT GDCD - Kết nối tri thức
- SBT GDCD - Chân trời sáng tạo
- SBT GDCD - Cánh diều
-
 HĐ trải nghiệm, hướng nghiệp 7
HĐ trải nghiệm, hướng nghiệp 7 - SBT Hoạt động trải nghiệm - Chân trời sáng tạo (Bản 1)
- SGK Hoạt động trải nghiệm, hướng nghiệp - Kết nối tri thức
- SGK Hoạt động trải nghiệm, hướng nghiệp - Cánh Diều
- SGK Hoạt động trải nghiệm, hướng nghiệp - Chân trời sáng tạo
- SBT Hoạt động trải nghiệm - Cánh diều
- SBT Hoạt động trải nghiệm - Kết nối tri thức
- SBT Hoạt động trải nghiệm - Chân trời sáng tạo (Bản 2)
-
 Âm nhạc 7
Âm nhạc 7 - Âm nhạc - Kết nối tri thức
- Âm nhạc - Chân trời sáng tạo
- Âm nhạc - Cánh diều
- Giáo dục địa phương 7
- Đề thi, đề kiểm tra Giáo dục địa phương 7
- Tài liệu Giáo dục địa phương
- Đề thi, đề kiểm tra 7
- Tổng hợp đề thi, đề kiểm tra
-
- Lớp 6
-
 Ngữ văn 6
Ngữ văn 6 - Soạn văn siêu ngắn - KNTT
- Soạn văn chi tiết - KNTT
- Soạn văn siêu ngắn - CTST
- Soạn văn chi tiết - CTST
- Soạn văn siêu ngắn - Cánh diều
- Soạn văn chi tiết - Cánh diều
- Tác giả - Tác phẩm văn
- Tóm tắt, bố cục Văn - Kết nối tri thức
- >> Xem thêm
-
 Toán học 6
Toán học 6 - SGK Toán - Kết nối tri thức
- SGK Toán - Chân trời sáng tạo
- SGK Toán - Cánh diều
- SBT Toán - Kết nối tri thức
- SBT Toán - Chân trời sáng tạo
- SBT Toán - Cánh diều
- Trắc nghiệm Toán - Kết nối tri thức
- Trắc nghiệm Toán - Chân trời sáng tạo
- >> Xem thêm
-
 Tiếng Anh 6
Tiếng Anh 6 - Global Success (Pearson)
- Tiếng Anh - Friends plus
- Tiếng Anh - iLearn Smart World
- Tiếng Anh - Right on
- Tiếng Anh - English Discovery
- Tiếng Anh - Explore English
- SBT Global Success
- SBT Friends Plus
- >> Xem thêm
-
 Khoa học tự nhiên 6
Khoa học tự nhiên 6 - SGK KHTN - Kết nối tri thức
- SGK KHTN - Chân trời sáng tạo
- SGK KHTN - Cánh Diều
- SBT KHTN - Kết nối tri thức
- SBT KHTN - Chân trời sáng tạo
- SBT KHTN - Cánh Diều
- Trắc nghiệm KHTN - Kết nối tri thức
- Trắc nghiệm KHTN - Chân trời sáng tạo
- >> Xem thêm
-
 Lịch sử và Địa lí 6
Lịch sử và Địa lí 6 - SGK Lịch sử và Địa lí - KNTT
- SGK Lịch sử và Địa lí - CTST
- SGK Lịch sử và Địa lí - Cánh Diều
- SBT Lịch sử và Địa lí - KNTT
- SBT Lịch sử và Địa lí - CTST
- SBT Lịch sử và Địa lí - Cánh diều
- Trắc nghiệm Lịch sử và Địa Lí - KNTT
- Trắc nghiệm Lịch Sử và Địa Lí - CTST
- >> Xem thêm
-
 GDCD 6
GDCD 6 - SGK GDCD - KNTT
- SGK GDCD - CTST
- SGK GDCD - Cánh Diều
- SBT GDCD - Kết nối tri thức
- SBT GDCD - Chân trời sáng tạo
- SBT GDCD - Cánh diều
-
 Công nghệ 6
Công nghệ 6 - Công nghệ - Kết nối tri thức
- Công nghệ - Cánh Diều
- Công nghệ - Chân trời sáng tạo
- SBT Công nghệ - Kết nối tri thức
- SBT Công nghệ - Cánh diều
- SBT Công nghệ - Chân trời sáng tạo
-
 Tin học 6
Tin học 6 - Tin học - Kết nối tri thức + chân trời sáng tạo
- Tin học - Cánh Diều
- SBT Tin học - Kết nối tri thức
- SBT Tin học - Cánh Diều
-
 HĐ trải nghiệm, hướng nghiệp 6
HĐ trải nghiệm, hướng nghiệp 6 - SGK Trải nghiệm, hướng nghiệp - Kết nối tri thức
- SGK Trải nghiệm, hướng nghiệp - Chân trời sáng tạo
- SGK Trải nghiệm, hướng nghiệp - Cánh diều
- SBT Trải nghiệm, hướng nghiệp - Kết nối tri thức
- SBT Trải nghiệm, hướng nghiệp - Chân trời sáng tạo
- Thực hành Trải nghiệm, hướng nghiệp - Cánh diều
-
 Âm nhạc 6
Âm nhạc 6 - Âm nhạc - Kết nối tri thức
- Âm nhạc - Cánh Diều
- Âm nhạc: Chân trời sáng tạo
-
 Mỹ thuật 6
Mỹ thuật 6 - Mĩ thuật - Kết nối tri thức
- Mĩ thuật - Chân trời sáng tạo
- Mĩ thuật - Cánh diều
- Giáo dục địa phương 6
- Đề thi, đề kiểm tra Giáo dục địa phương
- Tài liệu Giáo dục địa phương
- Đề thi, đề kiểm tra 6
- Tổng hợp đề thi, đề kiểm tra
-
- Lớp 5
-
 Toán học 5
Toán học 5 - SGK Toán - Kết nối tri thức
- SGK Toán - Chân trời sáng tạo
- SGK Toán - Cánh diều
- SGK Toán - Bình Minh
- VBT Toán - Kết nối tri thức
- VBT Toán - Cánh diều
- Trắc nghiệm Toán - Kết nối tri thức
- Trắc nghiệm Toán - Chân trời sáng tạo
- >> Xem thêm
-
 Tiếng việt 5
Tiếng việt 5 - Tiếng Việt - Kết nối tri thức
- Tiếng Việt - Chân trời sáng tạo
- Tiếng Việt - Cánh diều
- VBT Tiếng Việt - Kết nối tri thức
- VBT Tiếng Việt - Chân trời sáng tạo
- VBT Tiếng Việt - Cánh diều
- Văn mẫu lớp 5
- Đề thi, đề kiểm tra Tiếng Việt - Kết nối tri thức
- >> Xem thêm
-
 Tiếng Anh 5
Tiếng Anh 5 - Tiếng Anh - Global Success
- Tiếng Anh - Family and Friends
- Tiếng Anh - iLearn Smart Start
- Tiếng Anh - Explore Our World
- Tiếng Anh - Phonics Smart
- SBT Tiếng Anh - Global Success
- SBT Tiếng Anh - Family and Friends
- SBT Tiếng Anh - iLearn Smart Start
- >> Xem thêm
-
 Lịch sử và Địa lí 5
Lịch sử và Địa lí 5 - SGK Lịch sử và Địa lí - Kết nối tri thức
- SGK Lịch sử và Địa lí - Cánh diều
- SGK Lịch sử và Địa lí - Chân trời sáng tạo
- VBT Lịch sử và Địa lí - Kết nối tri thức
- VBT Lịch sử và Địa lí - Cánh diều
- Đề thi, đề kiểm tra Lịch sử và Địa lí - Kết nối tri thức
- Đề thi, đề kiểm tra Lịch sử và Địa lí - Chân trời sáng tạo
- Đề thi, đề kiểm tra Lịch sử và Địa lí - Cánh diều
-
 Khoa học 5
Khoa học 5 - SGK Khoa học - Kết nối tri thức
- SGK Khoa học - Chân trời sáng tạo
- SGK Khoa học - Cánh diều
- VBT Khoa học - Kết nối tri thức
- VBT Khoa học - Chân trời sáng tạo
- VBT Khoa học - Cánh diều
-
 Đạo đức 5
Đạo đức 5 - SGK Đạo đức - Kết nối tri thức
- SGK Đạo đức - Chân trời sáng tạo
- SGK Đạo đức - Cánh diều
- VBT Đạo đức - Kết nối tri thức
- VBT Đạo đức - Chân trời sáng tạo
- VBT Đạo đức - Cánh diều
-
 Tin học 5
Tin học 5 - SGK Tin học - Cánh diều
- SGK Tin học - Kết nối tri thức
- SGK Tin học - Chân trời sáng tạo
- VBT Tin học - Kết nối tri thức
- VBT Tin học - Chân trời sáng tạo
- VBT Tin học - Cánh diều
-
 HĐ trải nghiệm, hướng nghiệp 5
HĐ trải nghiệm, hướng nghiệp 5 - SGK Hoạt động trải nghiệm - Kết nối tri thức
- SGK Hoạt động trải nghiệm - Cánh diều
- SGK Hoạt động trải nghiệm - Chân trời sáng tạo Bản 1
- SGK Hoạt động trải nghiệm - Chân trời sáng tạo Bản 2
- VBT Hoạt động trải nghiệm - Kết nối tri thức
- VBT Hoạt động trải nghiệm - Cánh diều
- VBT Hoạt động trải nghiệm - Chân trời sáng tạo (Bản 1)
- VBT Hoạt động trải nghiệm - Chân trời sáng tạo (Bản 2)
-
 Công nghệ 5
Công nghệ 5 - SGK Công nghệ - Kết nối tri thức
- SGK Công nghệ - Chân trời sáng tạo
- SGK Công nghệ - Cánh diều
- VBT Công nghệ - Kết nối tri thức
- Đề thi, đề kiểm tra 5
- Đề thi vào lớp 6
- Tổng hợp đề thi, đề kiểm tra
-
- Lớp 4
-
 Toán học 4
Toán học 4 - SGK Toán - Kết nối tri thức
- SGK Toán - Chân trời sáng tạo
- SGK Toán - Cánh diều
- SGK Toán - Bình Minh
- VBT Toán - Kết nối tri thức
- Vở thực hành Toán
- Trắc nghiệm Toán - Kết nối tri thức
- Trắc nghiệm Toán - Cánh diều
- >> Xem thêm
-
 Tiếng việt 4
Tiếng việt 4 - Tiếng Việt - Kết nối tri thức
- Tiếng Việt - Chân trời sáng tạo
- Tiếng Việt - Cánh diều
- VBT Tiếng Việt - Kết nối tri thức
- Đề thi, đề kiểm tra Tiếng Việt - Kết nối tri thức
- Đề thi, đề kiểm tra Tiếng Việt - Chân trời sáng tạo
- Đề thi, đề kiểm tra Tiếng Việt - Cánh diều
- Ôn hè Tiếng Việt
- >> Xem thêm
-
 Tiếng Anh 4
Tiếng Anh 4 - Tiếng Anh - Global Sucess
- Tiếng Anh - Family and Friends
- Tiếng Anh - iLearn Smart Start
- Tiếng Anh - Phonics Smart
- Tiếng Anh - Explore Our World
- SBT Tiếng Anh - Global Success
- SBT Tiếng Anh - Family and Friends
- SBT Tiếng Anh - iLearn Smart Start
- >> Xem thêm
-
 Lịch sử và Địa lí 4
Lịch sử và Địa lí 4 - SGK Lịch sử và Địa lí - Kết nối tri thức
- SGK Lịch sử và Địa lí - Chân trời sáng tạo
- SGK Lịch sử và Địa lí - Cánh diều
- VBT Lịch sử và Địa lí - Kết nối tri thức
- VBT Lịch sử và Địa lí - Chân trời sáng tạo
- VBT Lịch sử và Địa lí - Cánh diều
- Đề thi, đề kiểm tra Lịch sử và Địa lí - Kết nối tri thức
- Đề thi, đề kiểm tra Lịch sử và Địa lí - Chân trời sáng tạo
- >> Xem thêm
-
 Khoa học 4
Khoa học 4 - SGK Khoa học - Kết nối tri thức
- SGK Khoa học - Chân trời sáng tạo
- SGK Khoa học - Cánh diều
- VBT Khoa học - Kết nối tri thức
- VBT Khoa học - Chân trời sáng tạo
- VBT Khoa học - Cánh diều
-
 Đạo đức 4
Đạo đức 4 - SGK Đạo đức - Kết nối tri thức
- SGK Đạo đức - Chân trời sáng tạo
- SGK Đạo đức - Cánh diều
- VBT Đạo đức - Kết nối tri thức
- VBT Đạo đức 4 - Chân trời sáng tạo
- VBT Đạo đức - Cánh diều
-
 Tin học 4
Tin học 4 - SGK Tin học - Kết nối tri thức
- SGK Tin học - Chân trời sáng tạo
- SGK Tin học - Cánh diều
- VBT Tin học - Kết nối tri thức
- VBT Tin học - Chân trời sáng tạo
- VBT Tin học - Cánh diều
-
 Công nghệ 4
Công nghệ 4 - SGK Công nghệ - Kết nối tri thức
- SGK Công nghệ - Chân trời sáng tạo
- SGK Công nghệ - Cánh diều
- VBT Công nghệ - Kết nối tri thức
- VBT Công nghệ - Chân trời sáng tạo
- VBT Công nghệ - Cánh diều
-
 HĐ trải nghiệm, hướng nghiệp 4
HĐ trải nghiệm, hướng nghiệp 4 - SGK Hoạt động trải nghiệm - Kết nối tri thức
- SGK Hoạt động trải nghiệm - Cánh diều
- SGK Hoạt động trải nghiệm - Chân trời sáng tạo Bản 1
- SGK Hoạt động trải nghiệm - Chân trời sáng tạo Bản 2
- VBT Hoạt động trải nghiệm - Kết nối tri thức
- VBT Hoạt động trải nghiệm - Cánh diều
- VBT Hoạt động trải nghiệm - Chân trời sáng tạo (Bản 1)
- VBT Hoạt động trải nghiệm - Chân trời sáng tạo (Bản 2)
-
 Âm nhạc 4
Âm nhạc 4 - SGK Âm nhạc - Kết nối tri thức
- SGK Âm nhạc - Chân trời sáng tạo
- SGK Âm nhạc - Cánh diều
-
 Mỹ thuật 4
Mỹ thuật 4 - SGK Mĩ thuật - Kết nối tri thức
- SGK Mĩ thuật - Cánh diều
- SGK Mĩ thuật - Chân trời sáng tạo bản 1
- SGK Mĩ thuật - Chân trời sáng tạo bản 2
- Giáo dục thể chất 4
- SGK Giáo dục thể chất - Kết nối tri thức
- SGK Giáo dục thể chất - Cánh diều
- SGK Giáo dục thể chất - Chân trời sáng tạo
- Giáo dục địa phương 4
- Tài liệu Giáo dục địa phương
- Đề thi, đề kiểm tra 4
- Tổng hợp đề thi, đề kiểm tra
-
- Lớp 3
-
 Toán học 3
Toán học 3 - SGK Toán - Kết nối tri thức
- SGK Toán - Chân trời sáng tạo
- SGK Toán - Cánh diều
- VBT Toán - Kết nối tri thức
- Trắc nghiệm Toán - Kết nối tri thức
- Trắc nghiệm Toán - Cánh diều
- Trắc nghiệm Toán - Chân trời sáng tạo
- Đề thi, đề kiểm tra Toán - Kết nối tri thức
- >> Xem thêm
-
 Tiếng việt 3
Tiếng việt 3 - Tiếng Việt - Kết nối tri thức
- Tiếng Việt - Chân trời sáng tạo
- Tiếng Việt - Cánh diều
- VBT Tiếng Việt - Kết nối tri thức
- VBT Tiếng Việt - Chân trời sáng tạo
- VBT Tiếng Việt - Cánh diều
- Đề thi, đề kiểm tra Tiếng Việt - Kết nối tri thức
- Đề thi, đề kiểm tra Tiếng Việt - Chân trời sáng tạo
- >> Xem thêm
-
 Tiếng Anh 3
Tiếng Anh 3 - Tiếng Anh - Global Success
- Tiếng Anh - Family and Friends
- Tiếng Anh - iLearn Smart Start
- Tiếng Anh - Explore Our World
- Tiếng Anh - Phonics Smart
- SBT Tiếng Anh - Global Success
- SBT Tiếng Anh - Family and Friends
- SBT Tiếng Anh - iLearn Smart Start
- >> Xem thêm
-
 Tự nhiên và xã hội 3
Tự nhiên và xã hội 3 - VBT Tự nhiên và xã hội - Cánh diều
- Tự nhiên và xã hội - Kết nối tri thức
- Tự nhiên và xã hội - Chân trời sáng tạo
- Tự nhiên và xã hội - Cánh diều
- VBT Tự nhiên và xã hội - Kết nối tri thức
- VBT Tự nhiên và xã hội - Chân trời sáng tạo
-
 Đạo đức 3
Đạo đức 3 - SGK Đạo đức - Kết nối tri thức
- SGK Đạo đức - Chân trời sáng tạo
- SGK Đạo đức - Cánh diều
- VBT Đạo đức - Kết nối tri thức
- VBT Đạo đức - Cánh diều
- VBT Đạo đức - Chân trời sáng tạo
-
 Tin học 3
Tin học 3 - SGK Tin học - Kết nối tri thức
- SGK Tin học - Chân trời sáng tạo
- SGK Tin học - Cánh diều
- VBT Tin học - Kết nối tri thức
- VBT Tin học - Chân trời sáng tạo
-
 HĐ trải nghiệm, hướng nghiệp 3
HĐ trải nghiệm, hướng nghiệp 3 - SGK Hoạt động trải nghiệm- Kết nối tri thức
- SGK Hoạt động trải nghiệm- Chân trời sáng tạo
- SGK Hoạt động trải nghiệm - Cánh diều
- VBT Hoạt động trải nghệm - Kết nối tri thức
- VBT Hoạt động trải nghiệm - Chân trời sáng tạo
- VBT Hoạt động trải nghiệm - Cánh diều
-
 Công nghệ 3
Công nghệ 3 - SGK Công nghệ - Kết nối tri thức
- SGK Công nghệ - Chân trời sáng tạo
- SGK Công nghệ - Cánh diều
- VBT Công nghệ - Kết nối tri thức
- VBT Công nghệ - Chân trời sáng tạo
- VBT Công nghệ - Cánh diều
-
 Âm nhạc 3
Âm nhạc 3 - Âm nhạc - Kết nối tri thức
- Âm nhạc - Chân trời sáng tạo
- Âm nhạc - Cánh diều
- Giáo dục thể chất 3
- SGK Giáo dục thể chất - Kết nối tri thức
- SGK Giáo dục thể chất - Chân trời sáng tạo
- SGK Giáo dục thể chất - Cánh diều
- Giáo dục địa phương 3
- Tài liệu Giáo dục địa phương
-
- Lớp 2
-
 Toán học 2
Toán học 2 - SGK Toán - Kết nối tri thức
- SGK Toán - Chân trời sáng tạo
- SGK Toán - Cánh Diều
- VBT Toán - KNTT
- VBT Toán - CTST
- Trắc nghiệm Toán - Kết nối tri thức
- Trắc nghiệm Toán - Chân trời sáng tạo
- Trắc nghiệm Toán - Cánh Diều
- >> Xem thêm
-
 Tiếng việt 2
Tiếng việt 2 - Tiếng Việt - Kết nối tri thức
- Tiếng Việt - Chân trời sáng tạo
- Tiếng Việt - Cánh Diều
- Văn mẫu - Kết nối tri thức
- Văn mẫu - Chân trời sáng tạo
- Văn mẫu - Cánh diều
- VBT Tiếng Việt - Kết nối tri thức
- VBT Tiếng Việt - Chân trời sáng tạo
- >> Xem thêm
-
 Tiếng Anh 2
Tiếng Anh 2 - Tiếng Anh - Kết nối tri thức
- Tiếng Anh - Family and Friends
- Tiếng Anh - iLearn Smart Start
- Tiếng Anh - Phonics Smart
- Tiếng Anh - English Discovery
- Tiếng Anh - Explore Our World
- Family & Friends Special
- SBT Kết nối tri thức
- >> Xem thêm
-
 Tự nhiên và xã hội 2
Tự nhiên và xã hội 2 - Tự nhiên và xã hội - Kết nối tri thức
- Tự nhiên và xã hội - Chân trời sáng tạo
- Tự nhiên và xã hội - Cánh diều
- VBT Tự nhiên và xã hội - Kết nối tri thức
- VBT Tự nhiên và xã hội - Cánh diều
- VBT Tự nhiên và xã hội - Chân trời sáng tạo
-
 Đạo đức 2
Đạo đức 2 - SGK Đạo đức - Kết nối tri thức
- SGK Đạo đức - Chân trời sáng tạo
- SGK Đạo đức - Cánh Diều
- VBT Đạo đức - Kết nối tri thức
- VBT Đạo đức - Chân trời sáng tạo
- VBT Đạo đức - Cánh Diều
-
 Âm nhạc 2
Âm nhạc 2 - Âm nhạc 2 - Kết nối tri thức
- Âm nhạc 2 - Chân trời sáng tạo
- Âm nhạc 2 - Cánh diều
- VBT Âm nhạc - Kết nối tri thức
- VBT Âm nhạc - Chân trời sáng tạo
- VBT Âm nhạc - Cánh diều
-
 Mỹ thuật 2
Mỹ thuật 2 - Mĩ thuật- Kết nối tri thức
- Mĩ thuật- Chân trời sáng tạo
- Mĩ thuật - Cánh Diều
-
 HĐ trải nghiệm, hướng nghiệp 2
HĐ trải nghiệm, hướng nghiệp 2 - VBT Hoạt động trải nghiệm - Chân trời sáng tạo
- VTH Hoạt động trải nghiệm - Cánh Diều
- VBT Hoạt động trải nghiệm - Kết nối tri thức
- Giáo dục địa phương 2
- Tài liệu Giáo dục địa phương
-
- Lớp 1
-
 Tiếng việt 1
Tiếng việt 1 - Đề thi, kiểm tra Tiếng Việt
- SGK Tiếng Việt - Kết nối tri thức
- SGK Tiếng Việt - Chân trời sáng tạo
- SGK Tiếng Việt - Cánh diều
-
 Toán học 1
Toán học 1 - SGK Toán - Kết nối tri thức
- SGK Toán - Cánh diều
- SGK Toán - Chân trời sáng tạo
- Trắc nghiệm Toán
-
 Tiếng Anh 1
Tiếng Anh 1 - Chứng chỉ Cambridge Pre A1 Starters
-
 Truyện cổ tích 1
Truyện cổ tích 1 - Truyện cổ tích
-
 Tự nhiên và xã hội 1
Tự nhiên và xã hội 1 - Tự nhiên & xã hội
- VBT Tự nhiên & xã hội
-
 Đạo đức 1
Đạo đức 1 - VBT Đạo Đức
- Giáo dục địa phương 1
- Tài liệu Giáo dục địa phương
-
- Công cụ
-
 Ngữ văn
Ngữ văn - Từ điển tiếng Việt
- Từ đồng nghĩa, trái nghĩa
- Thành ngữ Việt Nam
- Dẫn chứng nghị luận xã hội
- Ca dao, tục ngữ
- Chính tả tiếng Việt
- Từ láy
- Kho truyện
- >> Xem thêm
-
 Tiếng Anh
Tiếng Anh - Động từ bất quy tắc
- Cụm động từ (Phrasal verbs)
-

- Chương 1 : Sự điện li

-

 100 bài tập về sự điện li có đáp án và lời giải chi tiết
100 bài tập về sự điện li có đáp án và lời giải chi tiết -

 300 bài tập về axit - bazo - muối có đáp án và lời giải chi tiết
300 bài tập về axit - bazo - muối có đáp án và lời giải chi tiết -

 300 bài tập về sự điện li của nước, pH, chất chỉ thị axit - bazo có đáp án và lời giải chi tiết
300 bài tập về sự điện li của nước, pH, chất chỉ thị axit - bazo có đáp án và lời giải chi tiết -

 300 câu hỏi về phản ứng trao đổi ion trong dung dịch các chất điện li có lời giải chi tiết
300 câu hỏi về phản ứng trao đổi ion trong dung dịch các chất điện li có lời giải chi tiết
-
- Chương 2: Nito - Photpho

-

 100 bài tập về nitơ có đáp án và lời giải chi tiết
100 bài tập về nitơ có đáp án và lời giải chi tiết -

 150 bài tập về aminiac và muối amoni có đáp án và lời giải chi tiết
150 bài tập về aminiac và muối amoni có đáp án và lời giải chi tiết -

 300 bài tập về axit nitric và muối nitrat có đáp án và lời giải chi tiết
300 bài tập về axit nitric và muối nitrat có đáp án và lời giải chi tiết -

 100 bài tập về photpho có đáp án và lời giải chi tiết
100 bài tập về photpho có đáp án và lời giải chi tiết -

 150 bài tập về axit photphoric và muối photphat có đáp án và lời giải chi tiết
150 bài tập về axit photphoric và muối photphat có đáp án và lời giải chi tiết -

 100 bài tập về phân bón hóa học có đáp án và lời giải chi tiết
100 bài tập về phân bón hóa học có đáp án và lời giải chi tiết
-
- Chương 3: Cacbon - Silic

-

 200 bài tập về cacbon có đáp án và lời giải chi tiết
200 bài tập về cacbon có đáp án và lời giải chi tiết -

 200 bài tập về silic và hợp chất của silic có đáp án và lời giải chi tiết
200 bài tập về silic và hợp chất của silic có đáp án và lời giải chi tiết
-
- Chương 4: Đại cương về hóa học hữu cơ

-

 200 bài tập về mở đầu hợp chất hữu cơ có đáp án và lời giải chi tiết
200 bài tập về mở đầu hợp chất hữu cơ có đáp án và lời giải chi tiết -

 200 bài tập về cấu trúc phân tử hợp chất hữu cơ có đáp án và lời giải chi tiết
200 bài tập về cấu trúc phân tử hợp chất hữu cơ có đáp án và lời giải chi tiết -

 100 bài tập về phản ứng hữu cơ có đáp án và lời giải chi tiết
100 bài tập về phản ứng hữu cơ có đáp án và lời giải chi tiết
-

40 bài tập về axit phophoric tác dụng với dung dịch kiềm có lời giải (phần 1)
Làm đề thiCâu hỏi 1 :
Thêm 0,15 mol NaOH vào dung dịch chứa 0,1 mol H3PO4. Sau phản ứng, trong dung dịch có các muối:
- A NaH2PO4 và Na2HPO4.
- B NaH2PO4 và Na3HPO4.
- C Na2HPO4 và Na3PO4.
- D NaH2PO4, Na2HPO4 và Na3PO4.
Đáp án: A
Phương pháp giải:
Các muối có thể tạo ra:
NaH2PO4 (tỉ lệ Na : P = 1)
Na2HPO4 (tỉ lệ Na : P = 2)
Na3PO4 (tỉ lệ Na : P = 3)
Từ đề bài tính được nNa : nP. Từ đó suy ra các muối được tạo thành.
Lời giải chi tiết:
Các muối có thể tạo ra:
NaH2PO4 (tỉ lệ Na : P = 1)
Na2HPO4 (tỉ lệ Na : P = 2)
Na3PO4 (tỉ lệ Na : P = 3)
Theo đề bài:
nNa = nNaOH = 0,15 mol
nP = nH3PO4 = 0,1 mol
=> 1 < nNa : nP = 0,15 : 0,1 = 1,5 < 2
=> Tạo 2 muối NaH2PO4 và Na2HPO4.
Đáp án A
Đáp án - Lời giảiCâu hỏi 2 :
Cho H3PO4 tác dụng hết với dung dịch chứa m gam NaOH, sau phản ứng thu được dung dịch X có chứa 2,51m gam chất tan. Các chất tan trong dung dịch X là
- A Na2HPO4, Na3PO4.
- B NaH2PO4, Na2HPO4.
- C Na3PO4, NaOH.
- D NaH2PO4, Na3PO4.
Đáp án: B
Phương pháp giải:
Lời giải chi tiết:
Các phản ứng có thể xảy ra :
(1) 3NaOH + H3PO4 -> Na3PO4 + 3H2O
(2) 2NaOH + H3PO4 -> Na2HPO4 + 2H2O
(3) NaOH + H3PO4 -> NaH2PO4 + H2O
Ta thấy : nNaOH = nH2O = 0,025m (mol)
BTKL: mH3PO4 = m chất tan + mH2O - mNaOH = 2,51m + 0,025m.18 - 0,025m.40 = 1,96m (gam) => nH3PO4 = 0,02m (mol) Tỉ lệ: nNaOH:nH3PO4 = 0,025m:0,02m = 1,25 (1<1,25<2) => Xảy ra phản ứng (2) và (3)
Chất tan là Na2HPO4 và NaH2PO4
Đáp án B
Đáp án - Lời giảiCâu hỏi 3 :
Để thu được muối trung hòa, cần bao nhiêu ml dung dịch NaOH 1M cho tác dụng với 50 ml dung dịch H3PO4 0,5M
- A 35 ml.
- B 45 ml.
- C 25 ml.
- D 75 ml.
Đáp án: D
Phương pháp giải:
Tính theo PTHH: H3PO4 + 3NaOH → Na3PO4 + 3H2O
Lời giải chi tiết:
nH3PO4 = 0,05.0,5 = 0,025 mol
H3PO4 + 3NaOH → Na3PO4 + 3H2O
0,025 → 0,075 mol
=> V dd NaOH = 0,075 : 1 = 0,075 lít = 75 ml
Đáp án D
Đáp án - Lời giảiCâu hỏi 4 :
Đổ dung dịch chứa 1,8 mol NaOH vào dung dịch chứa 1 mol H3PO4 thì muối thu được có số mol là :
- A 0,2 mol NaH2PO4 ; 0,8 mol Na2HPO4
- B 1 mol NaH2PO4
- C 0,6 mol Na3PO4
- D 0,8 mol NaH2PO4 ; 0,2 mol Na2HPO4
Đáp án: A
Phương pháp giải:
Lời giải chi tiết:
Vì nNaOH : nH3PO4 = 1,8 : 1 = 1,8
=> Phản ứng tạo x mol muối NaH2PO4 và y mol Na2HPO4
=> nNaOH = x + 2y = 1,8 và nH3PO4 = x + y = 1
=> x = 0,2 mol ; y = 0,8 mol
Đáp án A
Đáp án - Lời giảiCâu hỏi 5 :
Cho m gam NaOH vào dung dịch chứa 0,04 mol H3PO4, sau phản ứng hoàn toàn thu được dung dịch Y. Cô cạn dung dịch Y thu được 1,22m gam chất rắn khan. Giá trị m là
- A 2,0.
- B 4,0.
- C 6,0.
- D 8,0.
Đáp án: D
Phương pháp giải:
NaOH + H3PO4 → NaH2PO4 + H2O
2NaOH + H3PO4 → Na2HPO4 + 2H2O
3NaOH + H3PO4 → Na3PO4 + 3H2O
Nếu chỉ có NaH2PO4 => mmuối = 3m
Nếu chỉ có Na2HPO4 => mmuối = 1,775m
Nếu chỉ có Na3PO4 => mmuối = 1,37m
Theo đề bài: mchất rắn (=1,22m) < 1,37m
=> chất rắn gồm NaOH và Na3PO4
Lời giải chi tiết:
NaOH + H3PO4 -> NaH2PO4 + H2O
2NaOH + H3PO4 -> Na2HPO4 + 2H2O
3NaOH + H3PO4 -> Na3PO4 + 3H2O
nNaOH = m/40 = 0,025m (mol)
- Nếu chỉ có NaH2PO4 => nNaH2PO4 = nNaOH = 0,025m (mol) => mmuối = 0,025m.120 = 3m (g)
- Nếu chỉ có Na2HPO4 => nNa2HPO4 = 0,5nNaOH = 0,0125m (mol) => mmuối = 0,0125m.142 = 1,775m (g)
- Nếu chỉ có Na3PO4 => nNa3PO4 = nNaOH/3 = m/120 (mol) => mmuối = m/120.164 ≈ 1,37m (g)
Theo đề bài: mchất rắn (=1,22m) < 1,37m
=> chất rắn gồm NaOH và Na3PO4
=> nNa3PO4 = 0,04 mol=> nNaOH pứ = 0,12 mol
m rắn = mNa3PO4 + mNaOH dư => m rắn = mNa3PO4 + (mNaOH bđ - mNaOH pư) => 1,22m = 0,04.164 + (m - 0,12.40) => m = 8 gam
Đáp án D
Đáp án - Lời giảiCâu hỏi 6 :
Cho dd chứa 19,6 g H3PO4 vào tác dụng với dd chứa 22g NaOH. Muối gì tạo thành và khối lượng là bao nhiêu?
- A Na2HPO4 và Na3PO4; 7,1g và 24,6g.
- B Na2HPO4 và Na3PO4; 1,7g và 14,6g.
- C NaH2PO4 và Na3PO4; 5,7g và 15,8g.
- D NaH2PO4 và Na3PO4; 7,5g và16,4g.
Đáp án: A
Phương pháp giải:
Lời giải chi tiết:
nNaOH = 0,55 mol ; nH3PO4 = 0,2 mol
=> 2 < nNaOH / nH3PO4 < 3
Các phản ứng :
2NaOH + H3PO4 -> Na2HPO4 + 2H2O
2x x
3NaOH + H3PO4 -> Na3PO4 + 3H2O
3y y
=> 2x + 3y = 0,55 ; x + y = 0,2
=> x = 0,05 ; y = 0,15 mol
=> Na2HPO4 và Na3PO4; 7,1g và 24,6g.
Đáp án A
Đáp án - Lời giảiCâu hỏi 7 :
Cho dung dịch NaOH vào axit H3PO4 phản ứng xảy ra theo tỉ lệ 2 : 1. Hỏi muối nào thu được sau phản ứng?
- A Na2HPO4.
- B NaH2PO4.
- C Na3PO4.
- D Không xác định được.
Đáp án: A
Lời giải chi tiết:
PTHH: 2NaOH + H3PO4 → Na2HPO4 + 2H2O
Đáp án A
Đáp án - Lời giảiCâu hỏi 8 :
Để thu được muối photphat trung hòa, cần lấy bao nhiêu ml dung dịch NaOH 2,00M cho tác dụng với 200 ml dung dịch H3PO4 1,00M?
- A 100 ml
- B 200 ml
- C 300 ml
- D 350 ml
Đáp án: C
Phương pháp giải:
Tính theo PTHH.
Lời giải chi tiết:
nH3PO4 = 0,2.1 = 0,2 mol
PTHH: 3NaOH + H3PO4 → Na3PO4 + 3H2O
0,6 ← 0,2 (mol)
=> VNaOH = 0,6 : 2 = 0,3 lít = 300 ml
Đáp án C
Đáp án - Lời giảiCâu hỏi 9 :
Thêm 0,15 mol NaOH vào dung dịch chứa 0,1 mol H3PO4. Sau phản ứng, trong dung dịch có các muối:
- A NaH2PO4 và Na2HPO4.
- B NaH2PO4, Na2HPO4 và Na3PO4.
- C Na2HPO4 và Na3PO4.
- D NaH2PO4 và Na3PO4.
Đáp án: A
Phương pháp giải:
Lời giải chi tiết:
Ta có: nNaOH : nH3PO4 = 0,15 : 0,1 = 1,5
=> Hỗn hợp muối gồm có NaH2PO4 và Na2HPO4.
Đáp án A
Đáp án - Lời giảiCâu hỏi 10 :
Đổ dung dịch chứa 1,8 mol NaOH vào dung dịch chứa 1 mol H3PO4 thì muối thu được có số mol là :
- A
0,2 mol NaH2PO4 ; 0,8 mol Na2HPO4
- B
1 mol NaH2PO4
- C 0,6 mol Na3PO4
- D 0,8 mol NaH2PO4 ; 0,2 mol Na2HPO4
Đáp án: A
Lời giải chi tiết:
Vì nNaOH : nH3PO4 = 1,8 : 1 = 1,8
=> Phản ứng tạo x mol muối NaH2PO4 và y mol Na2HPO4
=> nNaOH = x + 2y = 1,8 và nH3PO4 = x + y = 1
=> x = 0,2 mol ; y = 0,8 mol
Đáp án A
Đáp án - Lời giảiCâu hỏi 11 :
Thêm 0,25 mol NaOH vào dung dịch chứa 0,1 mol H3PO4. Sau phản ứng, trog dung dịch có các muối:
- A NaH2PO4 và Na2HPO4.
- B NaH2PO4 và Na3PO4.
- C Na2HPO4 và Na3PO4.
- D NaH2PO4, Na2HPO4 và Na3PO4.
Đáp án: C
Phương pháp giải:
Các muối có thể tạo ra:
NaH2PO4 (tỉ lệ Na : P = 1)
Na2HPO4 (tỉ lệ Na : P = 2)
Na3PO4 (tỉ lệ Na : P = 3)
Từ đề bài tính được nNa : nP. Từ đó suy ra các muối được tạo thành.
Lời giải chi tiết:
Các muối có thể tạo ra:
NaH2PO4 (tỉ lệ Na : P = 1)
Na2HPO4 (tỉ lệ Na : P = 2)
Na3PO4 (tỉ lệ Na : P = 3)
Theo đề bài:
nNa = nNaOH = 0,25 mol
nP = nH3PO4 = 0,1 mol
=> 2 < nNa : nP = 0,25 : 0,1 = 2,5 < 3
=> Tạo 2 muối Na2HPO4 và Na3PO4.
Đáp án C
Đáp án - Lời giảiCâu hỏi 12 :
Cho 200 ml dung dịch NaOH 1M tác dụng với 200 ml dung dịch H3PO4 0,5M, muối thu được có khối lượng là
- A 11,9 gam.
- B 14,2 gam.
- C 15,8 gam.
- D 16,4 gam.
Đáp án: B
Phương pháp giải:
Phương pháp giải :
Xét NaOH : H3PO4 = T
+ Nếu T 1 thì tạo muối: NaH2PO4
+ Nếu 1 < T < 2 thì tạo 2 muối: NaH2PO4 và Na2HPO4
+ Nếu T = 2 thì tạo muối: Na2HPO4
+ Nếu 2 < T < 3 thì tạo 2 muối: Na2HPO4 và Na3PO4
+ Nếu T 3 thì tạo muối Na3PO4
Lời giải chi tiết:
Hướng dẫn giải:
n NaOH= 0,2 mol
n H3PO4= 0,1 mol
n NaOH : nH3PO4= 2 : 1 nên chỉ xảy tạo muối Na2HPO4
=> n Na2PO4 = 0,1 mol => m =14,2
Đáp án B
Đáp án - Lời giảiCâu hỏi 13 :
Cho 0,1 mol NaOH và 200 ml dung dịch H3PO4 1M. Phản ứng xảy ra hoàn toàn, sản phẩm thu được sau phản ứng là
- A Na2HPO4.
- B NaH2PO4.
- C Na3PO4.
- D NaH2PO4 và H3PO4 dư.
Đáp án: D
Phương pháp giải:
Lời giải chi tiết:
Các phản ứng có thể xảy ra:
3NaOH + H3PO4 → Na3PO4 + 3H2O
2NaOH + H3PO4 → Na2HPO4 + 2H2O
NaOH + H3PO4 → NaH2PO4 + H2O
Ta thấy: nNaOH : nH3PO4 = 0,1 : 0,2 = 0,5 < 1 => H3PO4 dư
Đáp án D
Đáp án - Lời giảiCâu hỏi 14 :
Cho 44 gam NaOH vào dung dịch chứa 39,2 gam H3PO4. Sau khi phản ứng xảy ra hoàn toàn, đem cô cạn dung dịch thu được đến cạn khô. Hỏi những muối nào được tạo nên và khối lượng muối khan thu được là bao nhiêu?
- A Na3PO4 và 50 gam.
- B NaH2PO4 và 42,9 gam; Na2HPO4 và 14,2 gam.
- C Na2HPO4 và 15 gam.
- D Na2HPO4 và 14,2 gam; Na3PO4 và 49,2 gam.
Đáp án: D
Phương pháp giải:
Lời giải chi tiết:
Các phản ứng có thể xảy ra :
(1) 3NaOH + H3PO4 → Na3PO4 + 3H2O
(2) 2NaOH + H3PO4 → Na2HPO4 + 2H2O
(3) NaOH + H3PO4 → NaH2PO4 + H2O
Ta có: nNaOH : nH3PO4 = 1,1 : 0,4 = 2,75
=> Xảy ra 2 phản ứng (1) và (2)
BTNT "Na": nNaOH = 3nNa3PO4 + 2nNa2HPO4 = 1,1 (*)
BTNT "P": nH3PO4 = nNa3PO4 + nNa2HPO4 = 0,4 (**)
Giải hệ (*) và (**) được nNa3PO4 = 0,3 mol và nNa2HPO4 = 0,1 mol
=> mNa3PO4 = 0,3.164 = 49,2 gam ; mNa2HPO4 = 0,1.142 = 14,2 gam
Đáp án D
Đáp án - Lời giảiCâu hỏi 15 :
Đốt cháy hoàn toàn 6,2 gam photpho bằng oxi dư rồi cho sản phẩm tạo thành tác dụng vừa đủ với m gam dung dịch NaOH 32% thu được muối Na2HPO4. Giá trị của m là:
- A
75.
- B
50.
- C
100.
- D
25.
Đáp án: B
Lời giải chi tiết:
Do phản ứng là vừa đủ nên :
2nP = 2nNa2HPO4 = nNaOH ( bảo toàn nguyên tố )
=> nNaOH = 2.6,2 : 31 = 0,4 mol
=> m = \(\frac{{0,4.40.100}}{{32}} = 50g\)
Đáp án B
Đáp án - Lời giảiCâu hỏi 16 :
Lấy 240 ml dung dịch gồm NaOH 1,6M và KOH 1M tác dụng hết với dung dịch H3PO4 thu được dung dich X. Chia X thành 2 phần bằng nhau:
- Phần 1: Cô cạn thu được 20,544 gam hỗn hợp muối khan.
- Phần 2: Cho tác dụng với dung dịch CaCl2 (dư) thu được m gam kết tủa.
Giá trị của m là
- A 11,160.
- B 17,688.
- C 17,640.
- D 24,288.
Đáp án: B
Phương pháp giải:
Quy đổi hỗn hợp kiềm về MOH với M=(23.0,384+39.0,24)/0,624=379/13.
Lời giải chi tiết:
nNaOH=0,384 mol; nKOH=0,24 mol.
Gọi CT chung của kiềm là MOH (với M=(23.0,384+39.0,24)/0,624=379/13)
Giả sử chỉ tạo một trong các muối sau:
MH2PO4: m muối=0,624.(1640/13)=78,72 g.
M2HPO4: m muối=(0,624/2).(2006/13)=48,144 g.
M3PO4: m muối=(0,624/3).(2372/13)=37,952 g.
37,952 gmuối=20,544.2=41,088<48,144 g
=> Tạo 2 muối M2HPO4 (x mol); M3PO4 (y mol).
Ta có:
(2006/13)x+(2372/13)y=20,544(1)
2x+3y=0,024/2(2)
=>x=0,048; y=0,072
=>m↓=mCa3(PO4)2+mCaHPO4=0,036.310+0,048.136=17,688 gam.
Đáp án B
Đáp án - Lời giảiCâu hỏi 17 :
Cho dung dịch NaOH tác dụng với dung dịch H3PO4 tạo 2 muối Na2HPO4,
Na3PO4. Cho 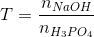
Xác định khoảng giá trị của T để tạo 2 muối trên.
- A T ≤ 1
- B 1<T<2
- C 2<T<3
- D T ≥ 3
Đáp án: C
Phương pháp giải:
Phương pháp:
+ T ≤ 1: NaH2PO4
+ 1<T<2: NaH2PO4, Na2HPO4
+ 2<T<3: Na2HPO4 ,Na3PO4
+ T ≥ 3: Na3PO4
Lời giải chi tiết:
Hướng dẫn giải
=> tạo 2 muối Na2HPO4,Na3PO4 => 2<T<3
=> chọn C
Đáp án C
Đáp án - Lời giảiCâu hỏi 18 :
Cho 0,3 mol dung dịch Ba(OH)2 tác dụng với 0,5 mol H3PO4 thu được dung dịch X. Dung dịch X chứa
- A Ba(H2PO4)2 và BaHPO4
- B BaHPO4 và Ba3(PO4)2
- C Ba3(PO4)2
- D Ba(H2PO4)2
Đáp án: A
Lời giải chi tiết:
Hướng dẫn giải
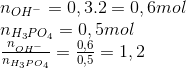
=> tạo 2 muối Ba(H2PO4)2, BaHPO4
=> chọn A
Đáp án A
Đáp án - Lời giảiCâu hỏi 19 :
Cho 0,5 mol dung dịch Ca(OH)2 tác dụng với 0,4 mol H3PO4 thu được dung dịch X. Dung dịch X chứa
- A Ca(H2PO4)2 và CaHPO4
- B CaHPO4 và Ca3(PO4)2
- C Ca3(PO4)2
- D Ca(H2PO4)2
Đáp án: B
Lời giải chi tiết:
nOH- = 2nCa(OH)2 = 1 mol
nH3PO4 = 0,4 mol
\( \to \frac{{{n_{O{H^ - }}}}}{{{n_{{H_3}P{O_4}}}}} = \frac{1}{{0,4}} = 2,5\)
=> Tạo muối CaHPO4 và Ca3(PO4)2
Đáp án B
Đáp án - Lời giảiCâu hỏi 20 :
Cho dung dịch NaOH tác dụng với dung dịch H3PO4 tạo 2 muối NaH2PO4, Na2HPO4. 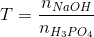
Xác định khoảng giá trị của T để tạo 2 muối trên
- A T≤ 1
- B 1<T<2
- C 2<T<3
- D T≥ 3
Đáp án: B
Phương pháp giải:
Phương pháp:
+ T ≤ 1: NaH2PO4
+ 1<T<2: NaH2PO4, Na2HPO4
+ 2<T<3: Na2HPO4 ,Na3PO4
+ T ≥ 3: Na3PO4
Lời giải chi tiết:
Hướng dẫn giải:
=> tạo 2 muối NaH2PO4, Na2HPO4 => 1<T<2
=> chọn B
Đáp án B
Đáp án - Lời giảiCâu hỏi 21 :
Cho 200 ml dung dịch KOH 1,5 M vào 200 ml dung dịch H3PO4 1 M thu được dung dịch X. dung dịch X chứa các chất là
- A K3PO4 , K2HPO4
- B KH2PO4, K2HPO4
- C KH2PO4, KOH
- D KH2PO4, H3PO4
Đáp án: B
Phương pháp giải:
Phương pháp:
Xét tỉ lệ
=> dd
Lời giải chi tiết:
Hướng dẫn giải
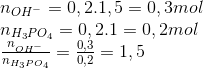
=> dd chứa KH2PO4, K2HPO4
=> chọn B
Đáp án B
Đáp án - Lời giảiCâu hỏi 22 :
Cho 19,6gam H3PO4 vào 100 ml dung dịch Ca(OH)2 1,5M thu được dung dịch X. Dung dịch X chứa các chất
- A Ca3(PO4)2 và CaHPO4
- B Ca(H2PO4)2 và CaHPO4
- C Ca3(PO4)2 và Ca(OH)2
- D Ca(H2PO4)2 và H3PO4
Đáp án: B
Phương pháp giải:
Phương pháp:
Xét tỉ lệ
=> dd
Lời giải chi tiết:
Hướng dẫn giải
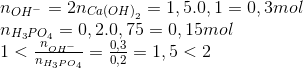
=> dd chứa Ca(H2PO4)2 và CaHPO4
=> chọn B
Đáp án B
Đáp án - Lời giảiCâu hỏi 23 :
Cần lấy bao nhiêu gam NaOH cho vào dd H3PO4 để thu được dung dịch có chứa 2,84 gam Na2HPO4 và 6,56 gam Na3PO4.
- A 4 gam
- B 6,4 gam
- C 7,68 gam
- D đáp án khác.
Đáp án: B
Phương pháp giải:
Phương pháp:
2NaOH+ H3PO4 -> Na2HPO4 + 2H2O
3Na OH + H3PO4 -> Na3PO4 + 3H2O
=> mNaOH
Lời giải chi tiết:
Hướng dẫn giải:
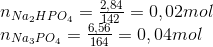
2NaOH+ H3PO4 -> Na2HPO4 + 2H2O
0,04 0,02
3Na OH + H3PO4 -> Na3PO4 + 3H2O
0,12 0,04
=> mNaOH= 40.0,16=6,4 gam
=> chọn B
Đáp án B
Đáp án - Lời giảiCâu hỏi 24 :
Trộn 100 ml dd NaOH 2,5M với 100 ml dd H3PO4 1,6M thu được dung dịch X. Xác định các chất tan có trong dung dịch X.
- A Na3PO4 và NaOH
- B Na3PO4 và Na2HPO4
- C Na2HPO4 và NaH2PO4
- D NaH2PO4 và H3PO4
Đáp án: C
Phương pháp giải:
Phương pháp:
Xét tỉ lệ
Lời giải chi tiết:
Hướng dẫn giải
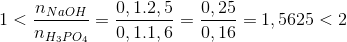
=> dung dịch X: NaH2PO4 ,Na2HPO4
=> chọn C
Đáp án C
Đáp án - Lời giảiCâu hỏi 25 :
Trộn lẫn dd có chứa 100 gam H3PO4 14,7% với dung dịch 16,8 gam KOH. Khối lượng muối thu được trong dung dịch.
- A 14,7 gam
- B 31,5 gam
- C 26,1 gam
- D 28,8 gam
Đáp án: C
Phương pháp giải:
Phương pháp:
Xét tỉ lệ
Lời giải chi tiết:
Hướng dẫn giải:
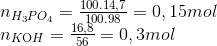
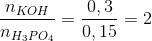
2KOH+ H3PO4 K2HPO4 + 2H2O
0,3 0,15 0,15
mmuối = 0,15.174=26,1 g
Đáp án C
Đáp án - Lời giảiCâu hỏi 26 :
Cho 200 ml dung dịch Ba(OH)2 1M vào 100 ml dung dịch H3PO4 1,5 M thu được dung dịch X. Dung dịch X chứa các chất
- A Ba3(PO4)2 và BaHPO4
- B Ba(H2PO4)2 và BaHPO4
- C Ba3(PO4)2 và Ba(OH)2
- D Ba(H2PO4)2 và H3PO4
Đáp án: A
Phương pháp giải:
Phương pháp:
Tìm tỉ lệ
=> dd
Lời giải chi tiết:
Hướng dẫn giải
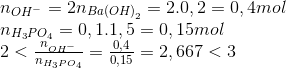
=> dd chứa Ba3(PO4)2 và BaHPO4
=> chọn A
Đáp án A
Đáp án - Lời giảiCâu hỏi 27 :
Cho 0,15 mol NaOH tác dụng với 0,1 mol H3PO4 thu được dung dịch X. Khối lượng các muối trong dung dịch X.
- A 6 gam NaH2PO4 và 7,1 gam Na2HPO4
- B 12 gam NaH2PO4 và 3,65 gam Na2HPO4
- C 9 gam NaH2PO4 và 7,1 gam Na2HPO4
- D 12 gam NaH2PO4 và 7,1 gam Na2HPO4.
Đáp án: A
Phương pháp giải:
Phương pháp:
=> X: NaH2PO4 (x mol), Na2HPO4 (y mol)
NaOH + H3PO4 -> NaH2PO4+ H2O (1)
x x x
2NaOH+ H3PO4 -> Na2HPO4 + 2H2O (2)
2y y y
Lời giải chi tiết:
Hướng dẫn giải
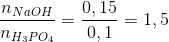
=> X: NaH2PO4 (x mol), Na2HPO4 (y mol)
NaOH + H3PO4 -> NaH2PO4+ H2O (1)
x x x
2NaOH+ H3PO4 -> Na2HPO4 + 2H2O (2)
2y y y
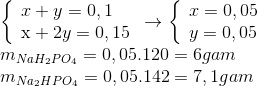
=> chọn A
Đáp án A
Đáp án - Lời giảiCâu hỏi 28 :
Lấy V(ml) dung dịch H3PO4 35% ( d = 1,25gam/ml ) đem trộn với 100 ml dung dịch KOH 2M thu được dung dịch X có chứa 14,95 gam hỗn hợp 2 muối K3PO4 và K2HPO4. Tính V1
- A 15,12 ml
- B 16,8 ml
- C 18,48 ml
- D 18,6 ml.
Đáp án: B
Phương pháp giải:
Phương pháp:
2KOH+ H3PO4 -> K2HPO4 + 2H2O
2x x x
3KOH + H3PO4 -> K3PO4 + 3H2O
3y y y
Lời giải chi tiết:
Hướng dẫn giải
2KOH+ H3PO4 -> K2HPO4 + 2H2O
2x x x
3KOH + H3PO4 -> K3PO4 + 3H2O
3y y y
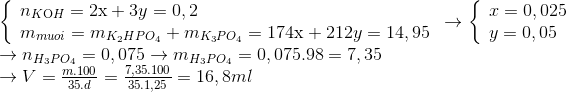
=> chọn B
Đáp án B
Đáp án - Lời giảiCâu hỏi 29 :
Cho 44g NaOH vào dung dịch chứa 39,2g H3PO4. Sau khi phản ứng xảy ra hoàn toàn , đem cô dung dịch thu được đến cạn khô. Hỏi những muối nào được tạo nên và khối lượng muối khan thu được là bao nhiêu ?
- A Na3PO4 và 50,0g
- B Na2HPO4 và 15,0g
- C NaH2PO4 và 49,2g ; Na2HPO4 và 14,2g
- D Na2HPO4 và 14,2g ; Na3PO4 và 49,2g
Đáp án: D
Phương pháp giải:
Phương pháp:
NaOH: 1,1 mol, H3PO4: 0,4 mol
Lời giải chi tiết:
Hướng dẫn giải
NaOH: 1,1 mol, H3PO4: 0,4 mol
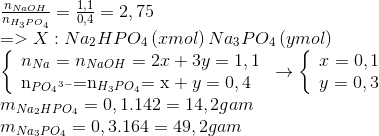
=> chọn D
Đáp án D
Đáp án - Lời giảiCâu hỏi 30 :
Cho 200 mol dung dịch KOH 2 M vào 200 ml dung dịch H3PO4 1,5 M. Khối lượng các chất có trong dung dịch X là?
- A 21,2 gam KH2PO4 và 13,65 gam K2HPO4
- B 27,2 gam KH2PO4 và 17,4 gam K2HPO4
- C 29 gam NaH2PO4 và 17,1 gam K2HPO4
- D 24 gam NaH2PO4 và 14,2 gam K2HPO4
Đáp án: B
Phương pháp giải:
Phương pháp:
KH2PO4, K2HPO4
x y
Lập hệ PT = > x,y
Lời giải chi tiết:
Hướng dẫn giải
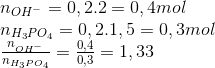
KH2PO4, K2HPO4
x y
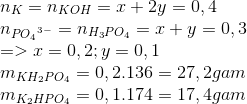
=> chọn B
Đáp án B
Đáp án - Lời giảiCâu hỏi 31 :
Cho 44g NaOH vào dung dịch chứa 39,2g H3PO4. Sau khi phản ứng xảy ra hoàn toàn , đem cô dung dịch thu được đến cạn khô. Hỏi những muối nào được tạo nên và khối lượng muối khan thu được là bao nhiêu ?
- A Na3PO4 và 50,0g
- B Na2HPO4 và 15,0g
- C NaH2PO4 và 49,2g ; Na2HPO4 và 14,2g
- D Na2HPO4 và 14,2g ; Na3PO4 và 49,2g
Đáp án: D
Phương pháp giải:
Phương pháp:
nNaOH = 44:40=1,1 mol
2<T<3 tạo 2 muối Na2HPO4 ,Na3PO4
2NaOH+ H3PO4 Na2HPO4 + 2H2O
2x.................x
3Na OH + H3PO4 Na3PO4 + 3H2O
3y...............y
Lời giải chi tiết:
Hướng dẫn giải
nNaOH = 44/40=1,1 mol
nH3PO4=39,2/98=0,4 mol.
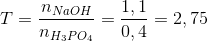
2<T<3 tạo 2 muối Na2HPO4 ,Na3PO4
2NaOH+ H3PO4 Na2HPO4 + 2H2O
2x.................x
3Na OH + H3PO4 Na3PO4 + 3H2O
3y...............y
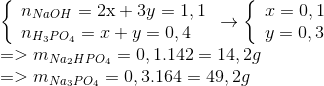
=> chọn D
Đáp án D
Đáp án - Lời giải
Câu hỏi 32 :
Cho 200 ml dung dịch H3PO4 1M vào 250 ml dung dịch hỗn hợp NaOH 0,5M và KOH 1,5M. Sau khi phản ứng hoàn toàn thu được dung dịch X. Khối lượng muối có trong dung dịch X là :
- A 32,6g
- B 36,6g
- C 38,4g
- D 40,2g
Đáp án: B
Phương pháp giải:
Phương pháp :
- Bài toán Kiềm + Axit nhiều nấc
Các phản ứng có thể xảy ra :
MOH + H3PO4 -> NaH2PO4 + H2O (1)
2MOH + H3PO4 -> Na2HPO4 + 2H2O (2)
3MOH + H3PO4 -> Na3PO4 + 3H2O (3)
Dựa vào tỉ lệ nOH : nH3PO4 = a => dự đoán sản phẩm phản ứng
+) a ≤ 1 => Chỉ có phản ứng (1)
+) 1 < a < 2 => (1) và (2)
+) a = 2 => (2)
+) 2 < a < 3 => (2) và (3)
+) a ≥ 3 => (3)
Lời giải chi tiết:
Hướng dẫn giải :
nH3PO4 = 0,2 mol ; nOH = nNaOH + nKOH = 0,5 mol
Các phản ứng có thể xảy ra :
MOH + H3PO4 -> NaH2PO4 + H2O (1)
2MOH + H3PO4 -> Na2HPO4 + 2H2O (2)
3MOH + H3PO4 -> Na3PO4 + 3H2O (3)
Vì nOH : nH3PO4 = 0,5 : 0,2 = 2,5
=> Xảy ra 2 phản ứng (2) và (3)
2MOH + H3PO4 -> Na2HPO4 + 2H2O (2)
2x <- x
3MOH + H3PO4 -> Na3PO4 + 3H2O (3)
3y <- y
=> x + y = 0,2 và 2x + 3y = 0,5
=> x = y = 0,1 mol
Muối sau phản ứng gồm : 0,1 mol HPO42- ; 0,1 mol PO43- ; 0,125 mol Na+ ; 0,375 mol K+
=> m = mion = 36,6g
Đáp án B
Đáp án - Lời giảiCâu hỏi 33 :
Cho 400 mol dung dịch Ba(OH)2 0,5 M vào 200 ml dung dịch H3PO4 1,5 M. Khối lượng các chất có trong dung dịch X là?
- A 33,1 gam Ba(H2PO4)2 và 23,3 gam BaHPO4
- B 2,34 gam Ba(H2PO4)2 và 2,54 gam BaHPO4
- C 33,1 gam Ba(H2PO4)2 và 23,1 gam BaHPO4
- D 33,1 gam Ba(H2PO4)2 và 9,8 gam H3PO4
Đáp án: A
Phương pháp giải:
Phương pháp:
=> dd chứa Ba(H2PO4)2 và BaHPO4
x y
Lập hệ PT => x,y
Lời giải chi tiết:
Hướng dẫn giải
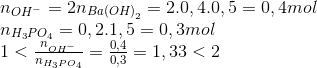
=> dd chứa Ba(H2PO4)2 và BaHPO4
x y
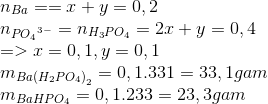
=> chọn A
Đáp án A
Đáp án - Lời giảiCâu hỏi 34 :
Cho 20 gam NaOH vào dung dịch chứa 39,2 gam H3PO4. Hỏi muối nào được tạo thành? Khối lượng là bao nhiêu ?
- A Na3PO4: 50 gam.
- B Na2HPO4: 14,2 gam và Na3PO4: 49,2 gam.
- C Na3PO4: 50 gam và Na2HPO4: 22,5 gam.
- D NaH2PO4: 36 gam và Na2HPO4: 14,2 gam.
Đáp án: D
Phương pháp giải:
a = nOH- : nH3PO4
+ a > 3 => Bazo dư, sau phản ứng thu được muối PO43- và OH-
+ a = 3 => thu được muối PO43-
+ 2< a < 3 => thu được HPO42- và PO43-
+ a = 2 => thu được HPO42-
+ 1 < a < 2 => thu được HPO42- và H2PO4-
+ a = 1 => thu được H2PO4-
+ a < 1 => axit dư, sau phản ứng thu được H2PO4-và H+
Lời giải chi tiết:
nNaOH = 0,5 mol
nH3PO4 = 0,4 mol
1 < nNaOH : nH3PO4 = 0,5:0,4 = 1,25 < 2
=> Tạo thành 2 muối: NaH2PO4 (x mol) và Na2HPO4 (y mol)
BT “Na”: x + 2y = nNaOH = 0,5
BT “P”: x + y = nH3PO4 = 0,4
=> x = 0,3 và y = 0,1
mNaH2PO4 = 0,3.120 = 36 (g)
mNa2HPO4 = 0,1.142 = 14,2 (g)
Đáp án D
Đáp án - Lời giảiCâu hỏi 35 :
Cho 300 ml dung dịch NaOH 1M tác dụng với 200 ml dung dịch H3PO4 1M. Muối thu được sau phản ứng là
- A NaH2PO4.
- B NaH2PO4 và Na2HPO4.
- C Na2HPO4 và Na3PO4.
- D Na3PO4.
Đáp án: B
Phương pháp giải:
Tính tỉ lệ \((*) = \frac{{{n_{NaOH}}}}{{{n_{{H_3}P{O_4}}}}}\)
Qua sơ đồ ta thấy:
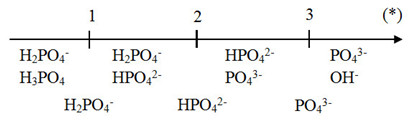
(*) ≤ 1 => tạo muối H2PO4-
1 < (*) < 2 => tạo muối H2PO4- và HPO42-
(*) = 2 => tạo muối HPO42-
2 < (*) < (3) => tạo muối HPO42- và PO43-
(*) ≤ 3 => tạo muối PO43-
Lời giải chi tiết:
Ta có: \(1 < (*) = \frac{{{n_{NaOH}}}}{{{n_{{H_3}P{O_4}}}}} = \frac{{0,3}}{{0,2}} = 1,5 < 2\) => tạo muối NaH2PO4 và Na2HPO4
Đáp án B
Đáp án - Lời giảiCâu hỏi 36 :
Cho dung dịch chứa 0,3 mol KOH vào dung dịch chứa 0,2 mol H3PO4 thu được dung dịch X. Các chất hòa tan có trong dung dịch X là:
- A K3PO4 và KOH
- B KH2PO4 và K2HPO4
- C K2HPO4 và K3PO4
- D KH2PO4 và K3PO4
Đáp án: B
Phương pháp giải:
Xét tỉ lệ nKOH : nH3PO4 = a
KOH + H3PO4 → KH2PO4 + H2O
2KOH + H3PO4 → K2HPO4 + 2H2O
3KOH + H3PO4 → K3PO4 + 3H2O
Nếu a ≤ 1 thì phản ứng chỉ tạo ra KH2PO4
Nếu 1 < a < 2 thì phản ứng tạo 2 muối KH2PO4 và K2HPO4
Nếu a = 2 thì phản ứng chỉ tạo K2HPO4
Nếu 2 < a < 3 thỉ phản ứng tạo 2 muối K2HPO4 và K3PO4
Nếu a ≥ 3 nên phản ứng tạo muối K3PO4
Lời giải chi tiết:
Vì nKOH : nH3PO4 = 0,3 : 0,2 = 1,5 nên phản ứng tạo 2 muối KH2PO4 và K2HPO4
KOH + H3PO4 → KH2PO4 + H2O
2KOH + H3PO4 → K2HPO4 + 2H2O
Đáp án B
Đáp án - Lời giảiCâu hỏi 37 :
Trộn 100 ml dung dịch H3PO4 1M với 100 ml dung dịch NaOH 1M thu được dung dịch X. Thành phần của dung dịch X là
- A Na2HPO4 và Na3PO4.
- B NaH2PO4 và H3PO4 dư.
- C Na3PO4 và NaOH dư.
- D NaH2PO4.
Đáp án: D
Phương pháp giải:
Dạng bài H3PO4 + OH-:
H3PO4 + OH- → H2PO4- + H2O
H3PO4 + 2OH- → HPO42- + 2H2O
H3PO4 + 3OH- → PO43- + 3H2O
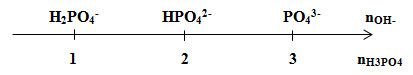
Giải thích trục số:
Đặt \(\frac{{{n_{O{H^ - }}}}}{{{n_{{H_3}P{O_4}}}}} = (*)\)
+ Nếu (*) < 1 => H3PO4 dư và H2PO4-
+ Nếu (*) = 1 => H2PO4-
+ Nếu 1 < (*) < 2 => H2PO4- và HPO42-
+ Nếu (*) = 2 => HPO42-
+ Nếu 2 < (*) < 3 => HPO42- và PO43-
+ Nếu (*) = 3 => PO43-
+ Nếu (*) > 3 => PO43- và OH‑ dư
Lời giải chi tiết:
\({n_{{H_3}P{O_4}}} = 0,1\,(mol);\,\,\,{n_{NaOH}} = 0,1(mol)\)
Ta thấy: \(\frac{{{n_{NaOH}}}}{{{n_{{H_3}P{O_4}}}}} = \frac{{0,1}}{{0,1}} = 1\) → Phản ứng chỉ tạo muối NaH2PO4.
Đáp án D
Đáp án - Lời giảiCâu hỏi 38 :
Trộn 200 gam dung dịch NaOH 3% với m gam dung dịch H3PO4 10% thu được 26,2 gam muối. Giá trị của m là:
- A 22,9.
- B 229.
- C 190,8.
- D 202.
Đáp án: B
Phương pháp giải:
Các phản ứng xảy ra:
H3PO4 + OH- → H2PO4- + H2O
H3PO4 + 2OH- → HPO42- + 2H2O
H3PO4 + 3OH- → PO43- + 3H2O
Xét các trường hợp sau:
*Trường hợp 1: Sản phẩm thu được gồm NaH2PO4 và H3PO4 dư
*Trường hợp 2 : Sản phẩm thu được gồm Na3PO4 và NaOH dư
*Trường hợp 3: NaOH và H3PO4 đều phản ứng hết
+ Ta luôn có nNaOH = nH2O
+ Áp dụng bảo toàn khối lượng ta tính được khối lượng H3PO4.
Lời giải chi tiết:
Ta có: nNaOH = 0,15 mol
Các phản ứng xảy ra:
H3PO4 + OH- → H2PO4- + H2O
H3PO4 + 2OH- → HPO42- + 2H2O
H3PO4 + 3OH- → PO43- + 3H2O
*Trường hợp 1: Sản phẩm thu được gồm NaH2PO4 và H3PO4 dư
Bảo toàn Na → nNaH2PO4 = nNaOH = 0,15 mol → m muối = 0,15.120 = 18 gam (loại)
*Trường hợp 2 : Sản phẩm thu được gồm Na3PO4 và NaOH dư
→ mNa3PO4 = m muối = 26,2 gam
→ nNa3PO4 = 16,2/164 = 0,16 mol
Nhận thấy rằng trong trường hợp này nNaOH ≥ 3nH3PO4 nên loại.
*Trường hợp 3: NaOH và H3PO4 đều phản ứng hết
+ Ta luôn có: nNaOH = nH2O = 0,15 mol
+ Bảo toàn khối lượng ta có: mNaOH + mH3PO4 = m muối + mH2O
→ 0,15 . 40 + mH3PO4 = 26,2 + 0,15 . 18
→ mH3PO4 = 22,9 gam
→ mdd = 22,9.(100/10) = 229 gam
Đáp án B
Đáp án - Lời giảiCâu hỏi 39 :
Cho 44 gam dung dịch NaOH 10% tác dụng với 10 gam dung dịch axit photphoric 39,2%. Muối nào sau đây thu được sau phản ứng?
- A Na2HPO4
- B NaH2PO4
- C Na2HPO4 và NaH2PO4
- D Na3PO4 và Na2HPO4
Đáp án: D
Phương pháp giải:
Khi cho H3PO4 tác dụng với OH- xảy ra các PTHH sau:
H3PO4 + OH- → H2PO4- + H2O
H3PO4 + 2OH- → HPO42- + 2H2O
H3PO4 + 3OH- → PO43- + 3H2O
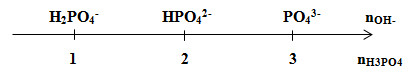
Giải thích trục số:
Đặt \((*) = \frac{{{n_{O{H^ - }}}}}{{{n_{{H_3}P{O_4}}}}}\)
+ Nếu (*) < 1 → H3PO4 dư và H2PO4-
+ Nếu (*) = 1 → H2PO4-
+ Nếu 1 < (*) < 2 → H2PO4- và HPO42-
+ Nếu (*) = 2 → HPO42-
+ Nếu 2 < (*) < 3 → HPO42- và PO43-
+ Nếu (*) = 3 → PO43-
+ Nếu (*) > 3 → PO43- và OH‑ dư
Lời giải chi tiết:
Ta có: nNaOH = 0,11 mol và nH3PO4 = 0,04 mol
Xét tỉ lệ: (*) = nNaOH : nH3PO4 = 0,11 : 0,04 = 2,75
Ta thấy 2 < (*) < (3) → Muối tạo thành là PO43- và HPO42-
Đáp án D
Đáp án - Lời giảiCâu hỏi 40 :
Cho 50 gam dung dịch KOH 33,6%. Tính khối lượng dung dịch H3PO4 50% cần cho vào dung dịch KOH để thu được hai muối kali đihiđrophotphat và kali hiđrophotphat với tỉ lệ số mol là 2 :1.
- A 29,4 gam
- B 58,5 gam
- C 44,1 gam
- D 49,0 gam
Đáp án: C
Phương pháp giải:
Đặt số mol muối KH2PO4 và K2HPO4 lần lượt là 2x mol và x mol
Bảo toàn nguyên tố K và nguyên tố P để tìm số mol H3PO4. Từ đó tìm được khối lượng dung dịch H3PO4 50%.
Lời giải chi tiết:
Ta có: mKOH = 50 . 33,6/100 = 16,8 (gam) → nKOH = 0,3 mol
Đặt số mol muối KH2PO4 và K2HPO4 lần lượt là 2x mol và x mol
Bảo toàn nguyên tố K ta có: nKOH = nKH2PO4 + 2.nK2HPO4 = 2x + 2x = 4x = 0,3 mol → x = 0,075 mol
Bảo toàn nguyên tố P ta có: nH3PO4 = nKH2PO4 + nK2HPO4 = 2x + x = 3x = 0,225 mol
→ mH3PO4 = 0,225 . 98 = 22,05 (g)
Vậy khối lượng dung dịch H3PO4 50% là mdd H3PO4 = 22,05 . 100/50 = 44,1 (g)
Đáp án C
Đáp án - Lời giảiXem thêm
20 bài tập về P2O5 tác dụng với dung dịch kiềm có lời giải20 bài tập về P2O5 tác dụng với dung dịch kiềm hay nhất có đáp án và lời giải chi tiết
Xem chi tiết 30 câu hỏi lý thuyết về axit photphoric - Muối photphat có lời giải30 câu hỏi lý thuyết về axit photphoric - Muối photphat hay nhất có đáp án và lời giải chi tiết
Xem chi tiết 20 bài tập vận dụng cao về axit photpphoric và muối photphat có lời giải20 bài tập vận dụng cao về axit photpphoric và muối photphat hay nhất có đáp án và lời giải chi tiết
Xem chi tiết>> 2K9 Học trực tuyến - Định hướng luyện thi TN THPT, ĐGNL, ĐGTD ngay từ lớp 11 (Xem ngay) cùng thầy cô giáo giỏi trên Tuyensinh247.com. Bứt phá điểm 9,10 chỉ sau 3 tháng, tiếp cận sớm các kì thi.
 |  |  |  |
 |  |  |  |
Các bài khác cùng chuyên mục
- 30 bài tập vận dụng về cracking ankan có lời giải
- 30 câu hỏi lý thuyết về mở đầu hợp chất hữu cơ có lời giải
- 20 câu hỏi lý thuyết về mở đầu hợp chất hữu cơ có lời giải (phần 2)
- 15 câu hỏi lý thuyết về phản ứng hữu cơ có lời giải
- 30 câu hỏi ôn tập về công thức phân tử hợp chất hữu cơ có lời giải (phần 2)
- 30 bài tập vận dụng về cracking ankan có lời giải
- 15 câu hỏi lý thuyết về phản ứng hữu cơ có lời giải
- 30 câu hỏi ôn tập về công thức phân tử hợp chất hữu cơ có lời giải (phần 2)
- 30 câu hỏi ôn tập về công thức phân tử hợp chất hữu cơ có lời giải (phần 1)
- 10 bài tập vận dụng cao về công thức phân tử hợp chất hữu cơ có lời giải
Báo lỗi góp ý
Vấn đề em gặp phải là gì ?Sai chính tả
Giải khó hiểu
Giải sai
Lỗi khác
Hãy viết chi tiết giúp Loigiaihay.com
Gửi góp ý Hủy bỏ Liên hệ Chính sáchCopyright © 2021 loigiaihay.com






Từ khóa » Bài Toán Oh Và H3po4
-
Cách Giải Bài Tập Về Axit Photphoric (H3PO4) Hay, Chi Tiết | Hóa Học ...
-
PHƯƠNG PHÁP GIẢI BÀI TẬP DUNG DỊCH BAZƠ TÁC DỤNG VỚI ...
-
Bài Tập H3PO4 Tác Dụng Với Dd Kiềm
-
Bài Tập H3po4 Tác Dụng Với Dung Dịch Kiềm - Hóa 11 - 123doc
-
Phương Pháp Giải P2O5 Và H3PO4 Tác Dụng Với Dung Dịch Kiềm
-
BÀI TẬP H 3 PO 4 TÁC DỤNG VỚI DD KIỀM
-
Chủ Đề 23 Bài Toán Về Axit H3PO4. | PDF - Scribd
-
SKKN Tư Duy Giải Nhanh Bài Toán H3PO4, P2O5 Tác Dụng Với Kiềm ...
-
[PDF] Điền Số Cho Bài Toán H3PO4 Tác Dụng Với OH - MSkill
-
Phương Pháp Giải Bài Tập H3PO4 - Tài Liệu, Giáo án điện Tử
-
PHƯƠNG PHÁP XÁC ĐỊNH NHANH SẢN PHẨM TRONG CÁC ...
-
Dạng Toán H3PO4 + OH