Bài 2 Phân Loại Các Chất điện Li - HOCMAI Forum


- Diễn đàn Bài viết mới Tìm kiếm trên diễn đàn
- Đăng bài nhanh
- Có gì mới? Bài viết mới New media New media comments Status mới Hoạt động mới
- Thư viện ảnh New media New comments Search media
- Story
- Thành viên Đang truy cập Đăng trạng thái mới Tìm kiếm status cá nhân
Tìm kiếm
Everywhere Đề tài thảo luận This forum This thread Chỉ tìm trong tiêu đề Search Tìm nâng cao… Everywhere Đề tài thảo luận This forum This thread Chỉ tìm trong tiêu đề By: Search Advanced…- Bài viết mới
- Tìm kiếm trên diễn đàn
- Thread starter riven
- Ngày gửi 3 Tháng sáu 2009
- Replies 1
- Views 3,925
- Bạn có 1 Tin nhắn và 1 Thông báo mới. [Xem hướng dẫn] để sử dụng diễn đàn tốt hơn trên điện thoại
- Diễn đàn
- HÓA HỌC
- TRUNG HỌC PHỔ THÔNG
- Hóa học lớp 11
- Sự điện li
riven
 [TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn
[TẶNG BẠN] TRỌN BỘ Bí kíp học tốt 08 môn  Chắc suất Đại học top - Giữ chỗ ngay!! ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn. 1, Tính nồng độ mol của CH3COOH, CH3COO- và H+ trong dung dịch CH3COOH 0,043M biết rằng độ điện li
Chắc suất Đại học top - Giữ chỗ ngay!! ĐĂNG BÀI NGAY để cùng trao đổi với các thành viên siêu nhiệt tình & dễ thương trên diễn đàn. 1, Tính nồng độ mol của CH3COOH, CH3COO- và H+ trong dung dịch CH3COOH 0,043M biết rằng độ điện li 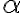 của CH3COOH bằng 20%. Nồng độ của các phân tử và ion trên lần lượt là
của CH3COOH bằng 20%. Nồng độ của các phân tử và ion trên lần lượt là - 0,043; 0,068 và 0,068
- 0,0344; 0,0086 và 0,0086
- 0,0344; 0,0344 và 0,0086 x
- 0,0344; 0,0344 và 0,0344
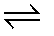 CH3COO- + H+Độ điện li
CH3COO- + H+Độ điện li 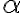 của CH3COOH sẽ giảm khi
của CH3COOH sẽ giảm khi - pha loãng dung dịch.
- nhỏ vào vài giọt dung dịch NaOH.
- nhỏ vào vài giọt NaCl.
- nhỏ vào vài giọt HCl.x
- không đổi
- giảm
- tăng . x
- cả 3 phương án đều sai x
keobong401
1, Tính nồng độ mol của CH3COOH, CH3COO- và H+ trong dung dịch CH3COOH 0,043M biết rằng độ điện li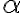 của CH3COOH bằng 20%. Nồng độ của các phân tử và ion trên lần lượt là
của CH3COOH bằng 20%. Nồng độ của các phân tử và ion trên lần lượt là - 0,043; 0,068 và 0,068
- 0,0344; 0,0086 và 0,0086
- 0,0344; 0,0344 và 0,0086 x
- 0,0344; 0,0344 và 0,0344
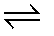 CH3COO- + H+Độ điện li
CH3COO- + H+Độ điện li 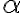 của CH3COOH sẽ giảm khi
của CH3COOH sẽ giảm khi - pha loãng dung dịch.
- nhỏ vào vài giọt dung dịch NaOH.
- nhỏ vào vài giọt NaCl.
- nhỏ vào vài giọt HCl.x
- không đổi
- giảm
- tăng . x
- cả 3 phương án đều sai x
- Diễn đàn
- HÓA HỌC
- TRUNG HỌC PHỔ THÔNG
- Hóa học lớp 11
- Sự điện li
- Vui lòng cài đặt tỷ lệ % hiển thị từ 85-90% ở trình duyệt trên máy tính để sử dụng diễn đàn được tốt hơn.
Từ khóa » Ka Ch3cooh/ch3coo-
-
Ka(CH3COOH) = 1,75.10-5
-
VD: CH3COOH CH3COO- + H+ Ka= = 1,8.10-5 - 123doc
-
5. Tính PH Của Dung Dịch Chứa CH3COOH 0,05M Và HCl 0,15M ...
-
Tính Nồng độ Mol Của CH3COOH, CH3COO− Và H+ Trong Dung ...
-
H{+} .Kc. Biết [CH3COOH] + 0,5M Và ở Trạng Thái Cân Bằng [H{+}] = 2 ...
-
Sự Phân Li Của Axit Axetic : CH3COOH CH3COO– + H+ Tại 25oC ...
-
Tính Nồng độ Mol Của Các Ion CH3COOH, CH3COO-, H+ Tại Cân ...
-
Phương Trình điện Li CH3COOH
-
CH3COOH Là Gì? Tính Chất đặc Trưng Và ứng Dụng Quan Trọng Của ...
-
Một Bài Toán Về Dung Dịch ? - Hóa Học | Narkive
-
Hóa Học - Kỹ Thuật Giải Bài Tập PH – Ka – Kb - Thư Viện Đề Thi
-
Hóa - Tính PH | Cộng đồng Học Sinh Việt Nam - HOCMAI Forum
-
Chuẩn độ Một Dung Dịch CH3COOH 0,1M Bằng Dung Dịch NaOH 0,1M