Bài 37. Etilen - Củng Cố Kiến Thức
Có thể bạn quan tâm
Công thức phân tử: $C_{2}H_{4}$
Phân tử khối: $28$
I. TÍNH CHẤT VẬT LÍ
- Etilen là chất khí, không màu, không mùi, ít tan trong nước và nhẹ hơn không khí $(d = \frac {28}{29}).$
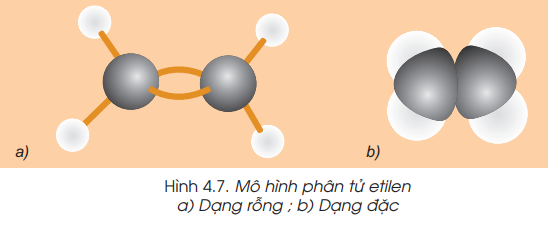
II. CẤU TẠO PHÂN TỬ
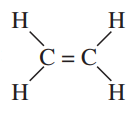
- Etilen có công thức cấu tạo:
$\Longrightarrow $ Viết gọn là: $CH_{2}=CH_{2}$
- Trong phân tử etilen $C_{2}H_{4},$ có một liên kết đôi giữa hai nguyên tử cacbon.
$\Longrightarrow $ Chú ý: Trong liên kết đôi có một liên kết kém bền. Liên kết này dễ đứt ra trong các phản ứng hóa học.
III. TÍNH CHẤT HÓA HỌC
1. Etilen có cháy không?
- Khi đốt etilen trong oxi, etilen cháy tạo thành khí $CO_{2}$ và $H_{2}O,$ phản ứng tỏa nhiều nhiệt.
$C_{2}H_{4}\,\,{}_{(k)}\,\, + \,\,3\,O_{2}\,\,{}_{(k)}\,\, {\overset{t^o}{\longrightarrow}} \,\,2\,CO_{2}\,\,{}_{(k)}\,\, + \,\,2\,H_{2}O\,\,{}_{(h)}$
$\Longrightarrow $ Nhận xét: Khi đốt cháy khí etilen thu được số mol $CO_{2}$ bằng số mol $H_{2}O.$
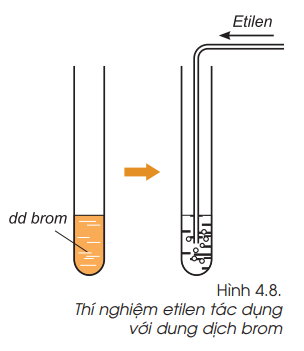
2. Etilen có làm mất màu dung dịch brom không?
- Etilen phản ứng với brom trong dung dịch $\longrightarrow $ Dung dịch brom bị mất màu.
$\underbrace {\mathop {CH_{2}=CH_{2}}\limits_{}^{}\,\,{}_{(k)}}_{\mathop {(Etilen)}\limits_{}^{}}\,\, + \,\,\underbrace {\mathop {Br_{2}}\limits_{}^{}\,\,{}_{(dd)}}_{\mathop {(Brom)}\limits_{}^{}}\,\, \longrightarrow \,\,\underbrace {\mathop {Br-CH_{2}-CH_{2}-Br}\limits_{}^{}\,\,{}_{(l)}}_{\mathop {(Đibrometan)}\limits_{}^{}}$
- Liên kết kém bền trong liên kết đôi bị đứt ra và mỗi phân tử etilen đã kết hợp thêm một phân tử brom.
- Phản ứng trên gọi là phản ứng cộng. Ngoài brom, trong những điều kiện thích hợp, etilen có thể tham gia phản ứng cộng với $Cl_{2},$ $H_{2},$ $HBr…$
$\Longrightarrow$ Các chất có liên kết đôi như etilen dễ tham gia phản ứng cộng.
3. Các phân tử etilen có kết hợp được với nhau không?
- Ở điều kiện thích hợp (nhiệt độ, áp suất, xúc tác), các phân tử etilen kết hợp với nhau tạo thành phân tử có kích thước và khối lượng rất lớn, gọi là polietilen (viết tắt là PE).
$...\,+ \,\,CH_{2}=CH_{2}\,\, + \,\,CH_{2}=CH_{2}\,\, + \,\,CH_{2}=CH_{2}\,\,+\,...\,\,\, \underset{Áp\,\,suất,\,\,t^{o}}{\overset{Xúc\,\,tác}{\longrightarrow}} \,\,\,...-CH_{2}-CH_{2}-CH_{2}-CH_{2}-CH_{2}-CH_{2}-...$
- Phản ứng trên gọi là phản ứng trùng hợp.
- Polietilen là chất rắn, không tan trong nước, không độc. Nó là nguyên liệu quan trọng trong công nghiệp chất dẻo.
IV. ỨNG DỤNG
- Etilen dùng để điều chế axit axetic, rượu etylic, polietilen (PE), poli (vinyl clorua) (PVC),...
- Etilen dùng kích thích quả mau chín.
Từ khóa » Etilen Có Liên Kết 3 Không
-
Etilen Là Gì? Tính Chất Hóa Học Và ứng Dụng Etilen Như Thế Nào?
-
Etilen: Định Nghĩa, Cấu Tạo, Tính Chất, điều Chế Và ứng Dụng - Monkey
-
Lý Thuyết Etilen | SGK Hóa Lớp 9
-
Công Thức Cấu Tạo Của Etilen C2H4. Tính Chất Hoá ... - Soạn Bài Tập
-
Tính Chất Hóa Học Của Etilen C2H4 | Tính Chất Vật Lí, Nhận Biết, điều ...
-
Etilen Là Gì? Công Thức, Tính Chất Hóa Học Của Etilen C2H4 - VietChem
-
[CHUẨN NHẤT] Tính Chất Hóa Học Của Etilen - TopLoigiai
-
Etilen C2H4 Cấu Tạo Phân Tử Tính Chất Hoá Học Của Etilen Và Bài Tập
-
Etilen C2H4 Cấu Tạo Phân Tử Tính Chất Hoá Học Của Etilen Và Bài Tập
-
Cấu Tạo Phân Tử, Tính Chất Vật Lý Và Hóa Học Của Etilen (C2H4)
-
Etilen C2H4 Cấu Tạo Phân Tử Tính Chất Hoá Học Của Etilen Và Bài Tập
-
Bài 37. Etilen - Hoc24
-
Etilen Không Phản ứng Với Chất Nào Trong Dãy Sau
-
Hóa 9 Bài 37: Etilen - VOH