Bài 9 (SGK Trang 90)Cân Bằng Các Phương Trình Phản ứng Oxi Hoá
Có thể bạn quan tâm
HOC24
Lớp học Học bài Hỏi bài Giải bài tập Đề thi ĐGNL Tin tức Cuộc thi vui Khen thưởng- Tìm kiếm câu trả lời Tìm kiếm câu trả lời cho câu hỏi của bạn
Lớp học
- Lớp 12
- Lớp 11
- Lớp 10
- Lớp 9
- Lớp 8
- Lớp 7
- Lớp 6
- Lớp 5
- Lớp 4
- Lớp 3
- Lớp 2
- Lớp 1
Môn học
- Toán
- Vật lý
- Hóa học
- Sinh học
- Ngữ văn
- Tiếng anh
- Lịch sử
- Địa lý
- Tin học
- Công nghệ
- Giáo dục công dân
- Tiếng anh thí điểm
- Đạo đức
- Tự nhiên và xã hội
- Khoa học
- Lịch sử và Địa lý
- Tiếng việt
- Khoa học tự nhiên
- Hoạt động trải nghiệm
- Hoạt động trải nghiệm, hướng nghiệp
- Giáo dục kinh tế và pháp luật
Chủ đề / Chương
Bài học
HOC24
 Khách vãng lai Đăng nhập Đăng ký Khám phá Hỏi đáp Đề thi Tin tức Cuộc thi vui Khen thưởng
Khách vãng lai Đăng nhập Đăng ký Khám phá Hỏi đáp Đề thi Tin tức Cuộc thi vui Khen thưởng - Tất cả
- Toán
- Vật lý
- Hóa học
- Sinh học
- Ngữ văn
- Tiếng anh
- Lịch sử
- Địa lý
- Tin học
- Công nghệ
- Giáo dục công dân
- Tiếng anh thí điểm
- Hoạt động trải nghiệm, hướng nghiệp
- Giáo dục kinh tế và pháp luật
Câu hỏi
Hủy Xác nhận phù hợp Chọn lớp Tất cả Lớp 12 Lớp 11 Lớp 10 Lớp 9 Lớp 8 Lớp 7 Lớp 6 Lớp 5 Lớp 4 Lớp 3 Lớp 2 Lớp 1 Môn học Toán Vật lý Hóa học Sinh học Ngữ văn Tiếng anh Lịch sử Địa lý Tin học Công nghệ Giáo dục công dân Tiếng anh thí điểm Đạo đức Tự nhiên và xã hội Khoa học Lịch sử và Địa lý Tiếng việt Khoa học tự nhiên Hoạt động trải nghiệm Hoạt động trải nghiệm, hướng nghiệp Giáo dục kinh tế và pháp luật Mới nhất Mới nhất Chưa trả lời Câu hỏi hay
- Nguyễn Hoàng Nam
Cân bằng các phương trình phản ứng oxi hóa – khử sau đây bằng phương pháp thăng bằng electron và cho biết chất khử, chất oxi hóa ở mỗi phản ứng:
a) Al + Fe3O4 → Al2O3 + Fe
b) FeSO4 + KMnO4 + H2SO4 → Fe2(SO4)3 + MnSO4 + K2SO4 + H2O
c) FeS2 + O2 → Fe2O3 + SO3
d) KClO3 → KCl + O2
e) Cl2 +KOH → KCl + KClO3 + H2O
Xem chi tiết Lớp 10 Hóa học 2 0 Gửi Hủy
Gửi Hủy 
- Ngô Quang Sinh
-
Cân bằng các phương trình phản ứng oxi hóa – khử:
![]()
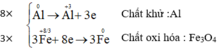
![]()
![]()

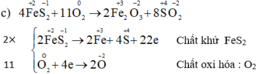


- Fen Fan
U
Đúng 0 Bình luận (0)
- pήươпg 亗ᄂơ ✿пgơ亗×͜× .
Cân bằng các phương trình phản ứng oxi hóa – khử sau đây bằng phương pháp thăng bằng electron và cho biết chất khử, chất oxi hóa ở mỗi phản ứng:
b) FeSO4 + KMnO4 + H2SO4 → Fe2(SO4)3 + MnSO4 + K2SO4 + H2O
e) Cl2 +KOH → KCl + KClO3 + H2O
Xem chi tiết Lớp 10 Hóa học 3 0
 Gửi Hủy
Gửi Hủy 
- pήươпg 亗ᄂơ ✿пgơ亗×͜× .
20p nữa ra đáp án
Đúng 0 Bình luận (0)
- chuche
-
Tham khảo:


- ︵✰Ah
-
b) 2FeSO4 + 2KMnO4 + 3H2SO4 → Fe2(SO4)3 + 2MnSO4 + K2SO4 + 3H2O
e) Cl2 +2KOH → KCl + KClO3 + H2O
Đúng 1 Bình luận (0)

- Cao Tùng Lâm
-
Cân bằng các phương trình phản ứng oxi hóa – khử sau đây bằng phương pháp thăng bằng electron và cho biết chất khử, chất oxi hóa ở mỗi phản ứng:
b) FeSO4 + KMnO4 + H2SO4 → Fe2(SO4)3 + MnSO4 + K2SO4 + H2O
e) CI2 +KOH → KCl + KClO3 + H2O
Giúp anh mik
Xem chi tiết Lớp 10 Hóa học 1 0 Gửi Hủy
Gửi Hủy 
- ILoveMath
-
b,10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4+ 8H2O
e,3CI2 +6KOH → 5KCl + KClO3 + 3H2O
Đúng 0 Bình luận (2)
- Tử Ái
Cân bằng phương trình hoá học các phương oxi hóa khử sau bằng phương pháp thăng bằng electron và cho biết chất khử, chất oxi hóa trong mỗi phản ứng đó:
a) NH3 + O2 --> NO + H2O
b) H2S + O2 --> S + H2O
c) Al + Fe2O3 --> Al2O3 + Fe
d) CO + Fe2O3 --> Fe + CO2
e) CuO + CO --> Cu + CO2
Xem chi tiết Lớp 10 Hóa học Bài 17: Phản ứng oxi hóa khử 1 1 Gửi Hủy
Gửi Hủy 
- ๖ۣۜDũ๖ۣۜN๖ۣۜG
-
a) 4NH3 + 5O2 -to-> 4NO + 6H2O
Chất khử: NH3, chất oxh: O2
| \(N^{-3}-5e->N^{+2}\) | x4 |
| \(O_2^0+4e->2O^{-2}\) | x5 |
b) 2H2S + O2 -to-> 2S + 2H2O
Chất khử: H2S, chất oxh: O2
| \(S^{-2}-2e->S^0\) | x2 |
| \(O^0_2+4e->2O^{-2}\) | x1 |
c) 2Al + Fe2O3 -to-> Al2O3 + 2Fe
Chất khử: Al, chất oxh: Fe2O3
| Al0-3e--> Al+3 | x2 |
| Fe2+3 +6e--> 2Fe0 | x1 |
d) Fe2O3 + 3CO -to-> 2Fe + 3CO2
Chất oxh: Fe2O3, chất khử: CO
| Fe2+3 +6e-->2Fe0 | x1 |
| C+2 - 2e --> C+4 | x3 |
e) CuO + CO -to-> Cu + CO2
Chất oxh: CuO, chất khử: CO
| Cu+2 +2e-->Cu0 | x1 |
| C+2 -2e --> C+4 | x1 |
Đúng 2 Bình luận (0)

- nguyễn tuấn kiệt A
DỀ 16
Câu 1: Cân bằng các phương trình phản ứng oxi hóa – khử bằng phương pháp thăng bằng electron. Cho biết chất oxi hóa và chất khử của mỗi phản ứng.
1. Cu + HNO3 -> Cu(NO3)2 + NO + H2O
2. Fe + H2SO4 -> Fe2(SO4)3 + SO2 + H2O
Câu 2: Cho 6,72 lít khí clo phản ứng vừa đủ với m gam sắt, thu được muối clorua. Tính m.
Câu 3: Hòa tan hoàn toàn 10,16g hỗn hợp (Fe và Mg) trong 500ml dung dịch HCl vừa đủ thì thu được 5,6 lít khí(đktc). a. Tính khối lượng mỗi kim loại trong hỗn hợp b. Tính nồng độ mol dung dịch HCl dã dùng
Xem chi tiết Lớp 10 Hóa học 1 1 Gửi Hủy
Gửi Hủy 
- Nguyễn Hoàng Minh
-
Câu 2:
\(n_{Cl_2}=\dfrac{6,72}{22,4}=0,3(mol)\\ PTHH:2Fe+3Cl_2\xrightarrow{t^o} 2FeCl_3\\ \Rightarrow n_{Fe}=0,2(mol)\\ \Rightarrow m=m_{Fe}=0,2.56=11,2(g)\)
Câu 3:
Đặt \(\begin{cases} n_{Fe}=x(mol)\\ n_{Mg}=y(mol) \end{cases} \)
\(a,n_{H_2}=\dfrac{5,6}{22,4}=0,25(mol) PTHH:Fe+2HCl\to FeCl_2+H_2\\ Mg+2HCl\to MgCl_2+H_2\\ \Rightarrow \begin{cases} 56x+24y=10,16\\ x+y=0,25 \end{cases} \Rightarrow\begin{cases} x=0,13(mol)\\ y=0,12(mol) \end{cases}\\ \Rightarrow \begin{cases} \%_{Fe}=\dfrac{0,13.56}{10,16}.100\%=71,65\%\\ \%_{Mg}=100\%-71,65\%=28,35\% \end{cases}\\ b,\Sigma n_{HCl}=2n_{Fe}+2n_{Mg}=0,5(mol)\\ \Rightarrow C_{M_{HCl}}=\dfrac{0,5}{0,5}=1M\)
Đúng 1 Bình luận (0)
- Ngô Đăng Khôi
1. Cân bằng phương trình hóa học của các phản ứng sau bằng phương pháp thăng bằng electron. Cho biết chất oxi hóa và chất khử của mỗi phản ứng :
Fe + H2SO4 đặc,nóng → Fe2 (SO4)3 + SO2+ H2O
KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O
2. Tính khối lượng CaF2 cần dùng để điều chế 2,5 kg dung dịch axit Flohidric nồng độ 40%.
3. Hòa tan 11 gam hỗn hợp bột sắt và nhôm trong dung dịch HCl thu được 8,96 lit khí (điều kiện tiêu chuẩn).
a. Xác định thành phần phần trăm về khối lượng của mỗi kim loại trong hỗn hợp. b. Tính thể tích dung dịch HCl 2M đã dùng.
(Cho Ca = 40; F = 19; H =1; Fe = 56; Al = 27)
Xem chi tiết Lớp 11 Hóa học 1 0
 Gửi Hủy
Gửi Hủy 
- Nguyễn Hoàng Minh
-
Bài 2:
\(m_{HF}=\dfrac{2,5.40\%}{100\%}=1(kg)\\ \Rightarrow n_{HF}=\dfrac{1}{20}=0,05(kmol)\\ PTHH:CaF+H_2SO_4\to CaSO_4+2HF\\ \Rightarrow n_{CaF}=0,025(kmol)\\ \Rightarrow m_{CaF}=0,025.78=1,95(kg)\)
Bài 3:
\(a,\) Đặt \(\begin{cases} n_{Fe}=x(mol)\\ n_{Al}=y(mol) \end{cases} \)
\(n_{H_2}=\dfrac{8,96}{22,4}=0,4(mol)\\ PTHH:2Al+6HCl\to 2AlCl_3+3H_2\\ Fe+2HCl\to FeCl_2+H_2\\ \Rightarrow \begin{cases} 56x+27y=11\\ x+1,5y=0,4 \end{cases} \Rightarrow \begin{cases} x=0,1(mol)\\ y=0,2(mol) \end{cases}\\ \Rightarrow \begin{cases} \%_{Fe}=\dfrac{0,1.56}{11}.100\%=50,91\%\\ \%_{Al}=100\%-50,91\%=49,09\% \end{cases} \)
\(b,\Sigma n_{HCl}=3n_{Al}+2n_{Fe}=0,2+0,6=0,7(mol)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{0,7}{2}=0,35(l)\)
Đúng 1 Bình luận (0)
- Nguyễn Hoàng Nam
Cân bằng PTHH của các phản ứng oxi hoá- khử sau bằng phương pháp thăng bằng electron (xác định chất khử, chất oxi hoá, quá trình khử, quá trình oxi hóa).
A l + H N O 3 → A l N O 3 3 + N O + N H 4 N O 3 + H 2 O
Xem chi tiết Lớp 10 Hóa học 1 0 Gửi Hủy
Gửi Hủy 
- Ngô Quang Sinh
-


- ĐN*Kid .Kill*
4. Cân bằng phương trình hóa học của các phản ứng sau bằng phương pháp thăng bằng electron. Cho biết chất oxi hóa và chất khử của mỗi phản ứng :
Al + H2SO4 đặc,nóng Al2 (SO4)3 + SO2 + H2O
MnO2 + HCl MnCl2 + Cl2 + H2O
Xem chi tiết Lớp 11 Hóa học 0 0 Gửi Hủy
Gửi Hủy 
- Quyên Giang
Cân bằng các phản ứng oxi hóa - khử sau. Xác định chất bị oxi hóa, chất bị khử, chất môi trường:
a. Zn + H2SO4 " ZnSO4 + SO2 + H2O
b. FeSO4 + H2SO4 + KMnO4 " Fe2(SO4)3 + K2SO4 + MnSO4 + H2O
c. Al + HNO3 " Al(NO3)3 + N2O + H2O
d. Cu + HNO3 " Cu(NO3)2 + NO + H2O
Xem chi tiết Lớp 10 Hóa học 0 0 Gửi Hủy
Gửi Hủy 
- Nguyễn Hoàng Nam
Cân bằng PTHH của các phản ứng oxi hoá- khử sau bằng phương pháp thăng bằng electron (xác định chất khử, chất oxi hoá, quá trình khử, quá trình oxi hóa).
C u + H 2 S O 4 đ , n → C u S O 4 + S O 2 + H 2 O
Xem chi tiết Lớp 10 Hóa học 1 0 Gửi Hủy
Gửi Hủy 
- Ngô Quang Sinh
-

Từ khóa » Cân Bằng Phương Trình Al + Fe3o4
-
Al + Fe3O4 → Al2O3 + Fe
-
Al Fe3O4 = Al2O3 Fe | Cân Bằng Phương Trình Hóa Học
-
Al + Fe3O4 | Al2O3 + Fe | Cân Bằng Phương Trình Hóa Học
-
Al + Fe3O4 = Al2O3 + Fe - Trình Cân Bằng Phản ứng Hoá Học
-
Fe3O4 + Al = Fe + Al2O3 - Trình Cân Bằng Phản ứng Hoá Học
-
Cân Bằng Nhanh Phản ứng Oxi Hóa - Khử : Al + Fe3O4 —› Al2O3 + Fe
-
Cân Bằng Các Phương Trình Phản ứng Oxi Hoá - Khử Sau ... - Selfomy
-
Cân Bằng Oxi Hóa- Khử A) Fe3O4+Al-> Al2O3+Fe B)FeSO4 + KMnO4 ...
-
Al + Fe3O4 ---> Al2O3 + Fe - Hóa Học Lớp 10 - Lazi
-
Tính Số Oxi Hóa Như Thế Nào? VD Bằng Cách Cân Bằng Phương ...
-
Cho Phương Trình Hóa Học Sau: Al + Fe3O4 \(\xrightarrow{{{t^0 ...
-
Al + Fe3O4 | Al2O3 + Fe | Phương Trình Hóa Học | Cân Bằng Phương ...
-
3Fe + 2O2 → Fe3O4 - Cân Bằng Phương Trình Hóa Học
-
Cách Cân Bằng Phương Trình Bằng Số Oxi Hóa Khử Hay, Chi Tiết





