Bảng Tính Tan Của Muối, Muối Nào Tan Trong Nước Và Không Tan
Có thể bạn quan tâm
Một số chất hóa học tan trong nước, có chất không tan hoặc có chất tan ít và tan nhiều. Chúng ta học từ lớp 9 đến lớp 11. Hôm nay ở bài viết này THPT Chuyên Lam Sơn xin gửi đến các bạn bảng tính tan của muối axit và bazơ.
=> Xem thêm các công thức hóa học để giải bài tập hóa
Nội Dung
- Bảng tính tan là gì ?
- Bảng tính tan của các chất hóa học
- 1. Tính tan của axit
- 2. Tính tan của bazơ
- 3. Muối nào tan trong nước và muối nào không tan ?
- 4. Cách học bảng tính tan dễ nhớ qua bài thơ
Bảng tính tan là gì ?
Bảng tính tan là bảng tổng hợp tính tan hay không tan của các chất trong nước, tuy nhiên, tính tan của Axit – Bazơ và Muối rất đa dạng và phụ thuộc nhiều yếu tố có chất có thể tan hoàn toàn trong nước, chất khác ít tan hoặc thậm chí là không tan trong nước.
Bảng tính tan của các chất hóa học
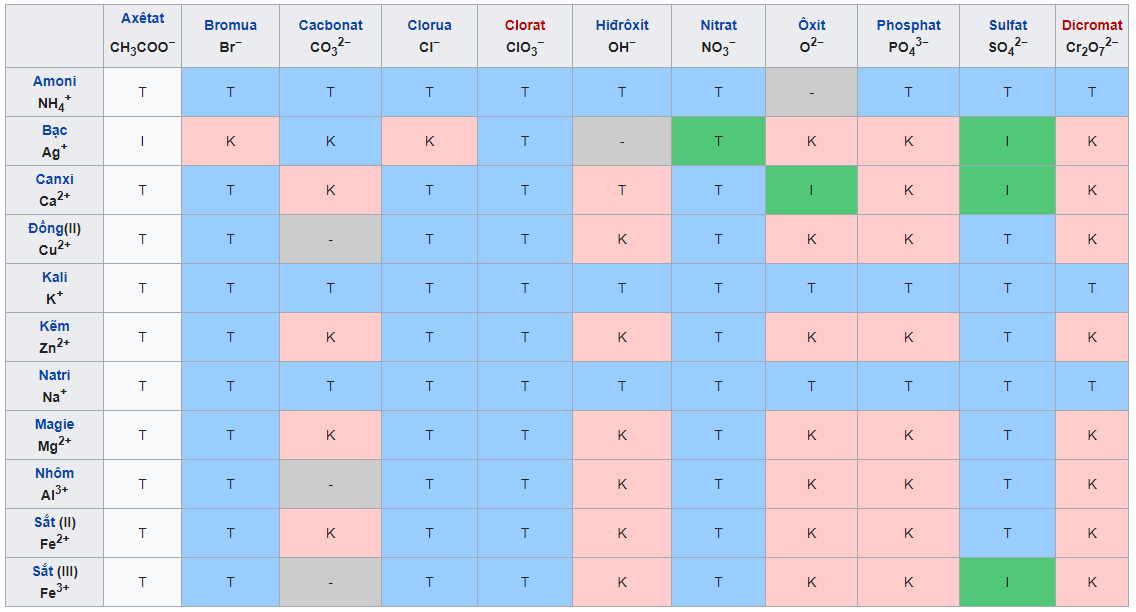
Chú thích:
T : chất dễ tan
I : chất ít tan
K : chất không tan (ô màu xanh)
B : chất bay hơi
– : chất không tồn tại hoặc bị nước phân huỷ
Cách đọc bảng tính tan:
Bảng tính tan gồm các hàng và các cột. Cột là các cation kim loại, còn hàng là các anion gốc axit (hay OH-). Với một chất cụ thể, ta sẽ xác định ion dương và ion âm, gióng theo hàng và cột tương ứng ta sẽ biết được trạng thái của chất đó tại một ô.
1. Tính tan của axit
- Tính chất hóa học chung của các axit là hòa tan tốt trong nước. Cho nên, đa số các axit tan tốt trong nước. Tuy nhiên, axit không tan đó là: H2SiO3, dễ bay hơi đó là HCl, HNO3
- Lưu ý axit yếu như H2CO3 , H2SO3 , là axit yếu (là axit có liên kết không bền) nên dễ dàng bị phân hủy trong nước, giải phóng khí CO2 , SO2 và nước.
2. Tính tan của bazơ
- Kim loại tan trong nước thì oxit và hidroxit tương ứng sẽ tan trong nước.
- Hầu hết các kim loại tạo bazo tương ứng, nhưng AgOH và Hg(OH)2 không tồn tại.
3. Muối nào tan trong nước và muối nào không tan ?
- Muối có gốc axit vẫn còn nguyên tử Hidro là muối axit. Các muối này hầu như tan tốt trong nước điển hình như (-HCO3, – HSO3, – HS).
- Muối của nhóm nitrat, muối Axetat tan tốt trong nước
- Muối Photphat (-PO4)3- của các kim loại kiềm thì tan, còn lại thì không tan.
- Muối gốc Cacbonat (- CO32-) hầu như không tan, ngoại trừ muối của các kim loại kiềm. Các kim loại Hg, Al, Cu, Fe
4. Cách học bảng tính tan dễ nhớ qua bài thơ
Bazơ, những chú không tan: Đồng, nhôm, crôm, kẽm, mangan, sắt, chì Ít tan là của canxi Magie cũng chẳng điện li dễ dàng.
Muối kim loại kiềm đều tan Cũng như nitrat và “nàng” hữu cơ Muốn nhớ thì phải làm thơ! Ta làm thí nghiệm bây giờ thử coi,
Kim koại I (IA), ta biết rồi, Những kim loại khác ta “moi” ra tìm Photphat vào nước đứng im (trừ kim loại IA) Sunfat một số “im lìm trơ trơ”: Bari, chì với S-r Ít tan gồm bạc, “chàng khờ” canxi,
Còn muối clorua thì Bạc đành kết tủa, anh chì cố tan (giống Br- và I-)
Muối khác thì nhớ dễ dàng: Gốc SO3 chẳng tan chút nào! (trừ kim loại IA) Thế gốc S thì sao? (giống muối CO32-) Nhôm không tồn tại, chú nào cũng tan Trừ đồng, thiếc, bạc, mangan, thuỷ ngân, kẽm, sắt không tan cùng chì
Đến đây thì đã đủ thi, Thôi thì chúc bạn trường gì cũng vô!
Thông qua bài viết mà chúng tôi rất mong sẽ giúp được các bạn hiểu hơn về bảng tính tan của các chất hóa học nhất là muối, axit và bazơ bạn cần nhớ các muối tan nhiều trong nước và các muối tan ít trong nước để có thể giải bài tập chính xác nhất.
Tweet Pin ItTừ khóa » Tính Tan Của Bazo Và Muối
-
2. Cách Ghi Nhớ Bảng Tính Tan
-
Bảng Tính Tan Hóa Học đầy đủ Nhất
-
[CHUẨN NHẤT] Bảng Tính Tan Của Các Muối - TopLoigiai
-
Bảng Tính Tan Hóa Học Đầy Đủ Của Axit, Bazơ Và Muối
-
Bảng Tính Tan Hóa Học
-
[ Bảng Tính Tan Của Muối, AXIT, BAZO ] Đầy Đủ Nhất
-
Bảng Tính Tan Hóa Học Lớp 11, Lớp 8 đầy đủ Nhất Từ A - Z
-
Bảng Tính Tan Hoá Học Đầy Đủ Của Muối, Axit Và Bazo Dễ Nhớ
-
Bảng Tính Tan Hóa Học Của Axit, Bazơ Và Muối đầy đủ Nhất
-
Bảng Tính Tan Hóa Học đầy đủ Của Muối Và Màu Kết Tủa
-
Bài Tập Tính Tan Của Axit, Bazo, Muối Cực Hay, Chi Tiết | Hóa Học Lớp 8
-
Bảng Tính Tan Của Các Chất Hóa Học, Muối, Axit, Bazơ - Thủ Thuật
-
Cách đọc Bảng Tính Tan Trong Nước Của Các Axit - Bazơ - Muối Lớp 8