Cân Bằng Phương Trình Hóa Học Của Các Phản ứng ôxi Hóa Khử Sau ...
Có thể bạn quan tâm
- Học bài
- Hỏi bài
- Kiểm tra
- ĐGNL
- Thi đấu
- Thư viện số
- Bài viết Cuộc thi Tin tức Blog học tập
- Trợ giúp
- Về OLM
OLM App phiên bản mới, cập nhật trải nghiệm ngay!
🔥ĐẤU TRƯỜNG TRỞ LẠI, THỬ THÁCH TĂNG CẤP!!! THAM GIA NGAY
Chính thức mở đề thi thử tốt nghiệp THPT trên máy tính từ 27/12/2025, xem ngay.
OLM Class tuyển sinh lớp bứt phá học kỳ II! Đăng ký ngay
- Mẫu giáo
- Lớp 1
- Lớp 2
- Lớp 3
- Lớp 4
- Lớp 5
- Lớp 6
- Lớp 7
- Lớp 8
- Lớp 9
- Lớp 10
- Lớp 11
- Lớp 12
- ĐH - CĐ
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
Xác nhận câu hỏi phù hợpChọn môn học Tất cả Toán Vật lý Hóa học Sinh học Ngữ văn Tiếng anh Lịch sử Địa lý Tin học Công nghệ Giáo dục công dân Âm nhạc Mỹ thuật Tiếng anh thí điểm Lịch sử và Địa lý Thể dục Khoa học Tự nhiên và xã hội Đạo đức Thủ công Quốc phòng an ninh Tiếng việt Khoa học tự nhiên Mua vip
- Tất cả
- Mới nhất
- Câu hỏi hay
- Chưa trả lời
- Câu hỏi vip
cân bằng phương trình hóa học của các phản ứng ôxi hóa khử sau bằng phương pháp thăng bằng electron : a) KMnO4 + HCl tạo thành KCl + MnCl2 + Cl2 + H2O ; b) HNO3 + HCl tạo thành NO + Cl2 + H2O ; c) HClO3 + HCl tạo thành Cl2 + H2O ; d) PbO2 + HCl tạo thành PbCl2 + Cl2 + H2O
#Hỏi cộng đồng OLM #Hóa học lớp 10 2 1 1080 7 tháng 1 2016
1 1080 7 tháng 1 2016 2KMnO4 + 16HCl ---> 2KCl + 2MnCl2 + 5Cl2 + 8H2O
2HNO3 + 6HCl ---> 2NO + 3Cl2 + 4H2O
HClO3 + 5HCl ---> 3Cl2 + 3H2O
PbO2 + 4HCl ---> PbCl2 + Cl2 + 2H2O
Đúng(0) LH Lê Hải Ly 23 tháng 4 2017C
Đúng(0) Xem thêm câu trả lời Những câu hỏi liên quan NH Nguyễn Hoàng Nam 3 tháng 9 2019 Cân bằng các phương trình phản ứng oxi hóa – khử sau bằng phương pháp thăng bằng electron: a) KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O. b) HNO3 + HCl → NO + Cl2 + H2O. c) HClO3 + HCl → Cl2 + H2O. d) PbO2 + HCl → PbCl2 + Cl2 +...Đọc tiếpCân bằng các phương trình phản ứng oxi hóa – khử sau bằng phương pháp thăng bằng electron:
a) KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O.
b) HNO3 + HCl → NO + Cl2 + H2O.
c) HClO3 + HCl → Cl2 + H2O.
d) PbO2 + HCl → PbCl2 + Cl2 + H2O
#Hỏi cộng đồng OLM #Hóa học lớp 10 1 NQ Ngô Quang Sinh 3 tháng 9 2019
NQ Ngô Quang Sinh 3 tháng 9 2019 Cân bằng các phản ứng oxi hóa – khử sau bằng phương pháp thăng bằng electron:
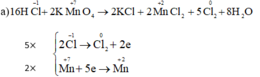
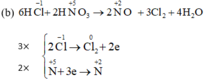
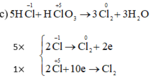
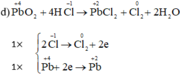
Tại sao chỉ tính oxi hóa của Cl2 mà ko tính oxi hóa của KCl vậy ạ?
Đúng(0) MN Minh Nguyễn 8 tháng 3 2023 Câu 1: Cân bằng phản ứng oxi hóa khử sau theo phương pháp thăng bằng electron, chỉ rõ chất khử, chất oxi hóa, sự oxi hóa, sự khử: (1) KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O (2) HNO3 + Cu→ Cu(NO3)2 + NO2 + H2O 80 (3) NH3 + O2 NO +...Đọc tiếpCâu 1: Cân bằng phản ứng oxi hóa khử sau theo phương pháp thăng bằng electron, chỉ rõ chất khử, chất oxi hóa, sự oxi hóa, sự khử:
(1) KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O
(2) HNO3 + Cu→ Cu(NO3)2 + NO2 + H2O 80
(3) NH3 + O2 NO + H2O
#Hỏi cộng đồng OLM #Hóa học lớp 10 1 LN Lê Ng Hải Anh 8 tháng 3 2023
LN Lê Ng Hải Anh 8 tháng 3 2023 (1) \(K\overset{+7}{Mn}O_4+H\overset{-1}{Cl}\rightarrow KCl+\overset{+2}{Mn}Cl_2+\overset{0}{Cl_2}+H_2O\)
- Chất khử: HCl
Chất oxh: KMnO4
- Sự oxh: \(2Cl^{-1}\rightarrow Cl_2^0+2e|\times5\)
Sự khử: \(Mn^{+7}+5e\rightarrow Mn^{+2}|\times2\)
\(\rightarrow2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
(2) \(H\overset{+5}{N}O_3+\overset{0}{Cu}\rightarrow\overset{+2}{Cu}\left(NO_3\right)_2+\overset{+4}{N}O_2+H_2O\)
- Chất khử: Cu
Chất oxh: HNO3
- Sự khử: \(N^{+5}+1e\rightarrow N^{+4}|\times2\)
Sự oxh: \(Cu^0\rightarrow Cu^{+2}+2e|\times1\)
\(\rightarrow4HNO_3+Cu\rightarrow Cu\left(NO_3\right)_2+2NO_2+2H_2O\)
(3) \(\overset{-3}{N}H_3+\overset{0}{O_2}\rightarrow\overset{+2}{N}\overset{-2}{O}+H_2O\)
- Chất khử: NH3
Chất oxh: O2
- Sự khử: \(O_2^0+4e\rightarrow2O^{-2}|\times5\)
Sự oxh: \(N^{-3}\rightarrow N^{+2}+5e|\times4\)
\(\rightarrow4NH_3+5O_2\rightarrow4NO+6H_2O\)
Đúng(1) ND Ngô Đăng Khôi 3 tháng 12 2021 1. Cân bằng phương trình hóa học của các phản ứng sau bằng phương pháp thăng bằng electron. Cho biết chất oxi hóa và chất khử của mỗi phản ứng : Fe + H2SO4 đặc,nóng → Fe2 (SO4)3 + SO2 + H2O KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O 2. Tính khối lượng CaF2 cần dùng để điều chế 2,5 kg dung dịch axit Flohidric nồng độ 40%. 3. Hòa tan 11 gam hỗn hợp bột sắt và nhôm trong dung dịch HCl thu được 8,96...Đọc tiếp1. Cân bằng phương trình hóa học của các phản ứng sau bằng phương pháp thăng bằng electron. Cho biết chất oxi hóa và chất khử của mỗi phản ứng :
Fe + H2SO4 đặc,nóng → Fe2 (SO4)3 + SO2+ H2O
KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O
2. Tính khối lượng CaF2 cần dùng để điều chế 2,5 kg dung dịch axit Flohidric nồng độ 40%.
3. Hòa tan 11 gam hỗn hợp bột sắt và nhôm trong dung dịch HCl thu được 8,96 lit khí (điều kiện tiêu chuẩn).
a. Xác định thành phần phần trăm về khối lượng của mỗi kim loại trong hỗn hợp. b. Tính thể tích dung dịch HCl 2M đã dùng.
(Cho Ca = 40; F = 19; H =1; Fe = 56; Al = 27)
#Hỏi cộng đồng OLM #Hóa học lớp 11 1
 NH Nguyễn Hoàng Minh 3 tháng 12 2021
NH Nguyễn Hoàng Minh 3 tháng 12 2021 Bài 2:
\(m_{HF}=\dfrac{2,5.40\%}{100\%}=1(kg)\\ \Rightarrow n_{HF}=\dfrac{1}{20}=0,05(kmol)\\ PTHH:CaF+H_2SO_4\to CaSO_4+2HF\\ \Rightarrow n_{CaF}=0,025(kmol)\\ \Rightarrow m_{CaF}=0,025.78=1,95(kg)\)
Bài 3:
\(a,\) Đặt \(\begin{cases} n_{Fe}=x(mol)\\ n_{Al}=y(mol) \end{cases} \)
\(n_{H_2}=\dfrac{8,96}{22,4}=0,4(mol)\\ PTHH:2Al+6HCl\to 2AlCl_3+3H_2\\ Fe+2HCl\to FeCl_2+H_2\\ \Rightarrow \begin{cases} 56x+27y=11\\ x+1,5y=0,4 \end{cases} \Rightarrow \begin{cases} x=0,1(mol)\\ y=0,2(mol) \end{cases}\\ \Rightarrow \begin{cases} \%_{Fe}=\dfrac{0,1.56}{11}.100\%=50,91\%\\ \%_{Al}=100\%-50,91\%=49,09\% \end{cases} \)
\(b,\Sigma n_{HCl}=3n_{Al}+2n_{Fe}=0,2+0,6=0,7(mol)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{0,7}{2}=0,35(l)\)
Đúng(1) CT Chi Trần 27 tháng 11 2021Cân bằng PTHH của các phản ứng oxi hoá- khử sau bằng phương pháp thăng bằng electron (xác định chất khử, chất oxi hoá, quá trình khử, quá trình oxi hóa).
1) KClO3+HCl --> KCl +Cl2+H2O2)K2Cr2O7 +HCl -->KCl+CrCl3 +Cl2+H2O3) KMnO4 +HCl --> KCl+MnCl2+Cl2+H2O4)Al+HNO3 --> Al(NO3)3+N2O+H2O5)Fe3O4 +HNO3 -->Fe(NO3)3 +NO+H2O6) FeS +O2 --> Fe2O3 +SO2
giúp mình với
#Hỏi cộng đồng OLM #Hóa học lớp 10 0 DK ĐN*Kid .Kill* 8 tháng 12 2021
DK ĐN*Kid .Kill* 8 tháng 12 2021 4. Cân bằng phương trình hóa học của các phản ứng sau bằng phương pháp thăng bằng electron. Cho biết chất oxi hóa và chất khử của mỗi phản ứng :
Al + H2SO4 đặc,nóng Al2 (SO4)3 + SO2 + H2O
MnO2 + HCl MnCl2 + Cl2 + H2O
#Hỏi cộng đồng OLM #Hóa học lớp 11 0 DA Danh Ẩn 5 tháng 12 2021
DA Danh Ẩn 5 tháng 12 2021 Cân bằng các phương trình sau theo phương pháp thăng bằng electron. Cho biết chất khử, chất oxi hóa. a. SO2 + Cl2 + H2O → HCl + H2SO4 b. Ag + HNO3 → AgNO3 + NO + H2O
#Hỏi cộng đồng OLM #Hóa học lớp 10 1
 NP Nguyễn Phúc 8 tháng 12 2021 Đúng(0) D Duy25 5 tháng 12 2021
NP Nguyễn Phúc 8 tháng 12 2021 Đúng(0) D Duy25 5 tháng 12 2021 Câu 1. Cân bằng các phương trình sau theo phương pháp thăng bằng electron. Cho biết chất khử, chất oxi hóa. a. SO2 + Cl2 + H2O → HCl + H2SO4 b. Ag + HNO3 → AgNO3 + NO + H2O
#Hỏi cộng đồng OLM #Hóa học lớp 10 0
 PO pήươпg 亗ᄂơ ✿пgơ亗×͜× . 12 tháng 1 2022
PO pήươпg 亗ᄂơ ✿пgơ亗×͜× . 12 tháng 1 2022 Cân bằng các phương trình phản ứng oxi hóa – khử sau đây bằng phương pháp thăng bằng electron và cho biết chất khử, chất oxi hóa ở mỗi phản ứng:
b) FeSO4 + KMnO4 + H2SO4 → Fe2(SO4)3 + MnSO4 + K2SO4 + H2O
e) Cl2 +KOH → KCl + KClO3 + H2O
#Hỏi cộng đồng OLM #Hóa học lớp 10 3
 PO pήươпg 亗ᄂơ ✿пgơ亗×͜× . 12 tháng 1 2022
PO pήươпg 亗ᄂơ ✿пgơ亗×͜× . 12 tháng 1 2022 20p nữa ra đáp án
Đúng(0) C chuche 12 tháng 1 2022Tham khảo:

4. Cân bằng phương trình hóa học của các phản ứng sau bằng phương pháp thăng bằng electron. Cho biết chất oxi hóa và chất khử của mỗi phản ứng :
Al + H2SO4 đặc,nóng Al2 (SO4)3 + SO2 + H2O
MnO2 + HCl MnCl2 + Cl2 + H2O
5. Tính khối lượng KMnO4 cần dùng để điều chế 1120 lít khí Clo (điều kiện tiêu chuẩn).
6. Hòa tan 10,2 gam hỗn hợp bột magie và nhôm trong dung dịch HCl thu được 11,2 lit khí (điều kiện tiêu chuẩn).
c. Xác định thành phần phần trăm về khối lượng của mỗi kim loại trong hỗn hợp.
d. Tính thể tích dung dịch HCl 2M đã dùng.
(Cho K = 39; Mn = 55; O =16; Mg = 24; Al = 27)
#Hỏi cộng đồng OLM #Hóa học lớp 11 1 MD Monkey D. Luffy 8 tháng 12 2021
MD Monkey D. Luffy 8 tháng 12 2021 Câu 5:
\(n_{Cl_2}=\dfrac{1120}{22,4}=50(mol)\\ PTHH:2KMnO_4+16HCl\to 2KCl+2MnCl_2+5Cl_2\uparrow+8H_2O\\ \Rightarrow n_{KMnO_4}=\dfrac{2}{5}n_{Cl_2}=20(mol)\\ \Rightarrow m_{KMnO_4}=20.158=3160(g)\)
Câu 6:
Đặt \(n_{Mg}=x(mol);n_{Al}=y(mol)\Rightarrow 24x+27y=10,2(1)\)
\(n_{H_2}=\dfrac{11,2}{22,4}=0,5(mol)\\ PTHH:2Al+6HCl\to 2AlCl_3+3H_2\\ Mg+2HCl\to MgCl_2+H_2\\ \Rightarrow x+1,5y=0,5(2)\\ (1)(2)\Rightarrow x=y=0,2(mol)\\ \Rightarrow \%_{Al}=\dfrac{0,2.27}{10,2}.100\%=52,94\%\\ \Rightarrow \%_{Mg}=100\%-52,94\%=47,06\%\\ b,\Sigma n_{HCl}=3y+2x=1(mol)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{1}{2}=0,5(l)\)
Đúng(1) NH Nguyễn Hoàng Nam 21 tháng 11 2017 Cân bằng các phương trình phản ứng oxi hóa – khử sau đây bằng phương pháp thăng bằng electron và cho biết chất khử, chất oxi hóa ở mỗi phản ứng: a) Al + Fe3O4 → Al2O3 + Fe b) FeSO4 + KMnO4 + H2SO4 → Fe2(SO4)3 + MnSO4 + K2SO4 + H2O c) FeS2 + O2 → Fe2O3 + SO3 d) KClO3 → KCl + O2 e) Cl2 +KOH → KCl + KClO3 +...Đọc tiếpCân bằng các phương trình phản ứng oxi hóa – khử sau đây bằng phương pháp thăng bằng electron và cho biết chất khử, chất oxi hóa ở mỗi phản ứng:
a) Al + Fe3O4 → Al2O3 + Fe
b) FeSO4 + KMnO4 + H2SO4 → Fe2(SO4)3 + MnSO4 + K2SO4 + H2O
c) FeS2 + O2 → Fe2O3 + SO3
d) KClO3 → KCl + O2
e) Cl2 +KOH → KCl + KClO3 + H2O
#Hỏi cộng đồng OLM #Hóa học lớp 10 2 NQ Ngô Quang Sinh 21 tháng 11 2017
NQ Ngô Quang Sinh 21 tháng 11 2017 Cân bằng các phương trình phản ứng oxi hóa – khử:
![]()
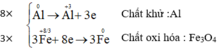
![]()
![]()

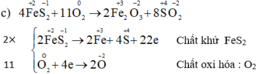

U
Đúng(0) Xem thêm câu trả lời Xếp hạng Tất cả Toán Vật lý Hóa học Sinh học Ngữ văn Tiếng anh Lịch sử Địa lý Tin học Công nghệ Giáo dục công dân Âm nhạc Mỹ thuật Tiếng anh thí điểm Lịch sử và Địa lý Thể dục Khoa học Tự nhiên và xã hội Đạo đức Thủ công Quốc phòng an ninh Tiếng việt Khoa học tự nhiên- Tuần
- Tháng
- Năm
- B 🐊Bombardiro💣Crocodilo✈️ 7 GP
- E ✦ ꧁𝓑é✿𝓬𝓱í𝓹꧂ ✦ 6 GP
- DM ༒☬Đăng Minh☬༒ (Meokonhonguongthuoc) 6 GP
- HG Happy great day GD ! 6 GP
- PN professor's name ThAnH 4 GP
- O ꧁༺©ⓤ✞ঔৣ㊎ɦƯղɕლɑꜱζℰℜɦỒղղɦ¡Êղ2ƙ13✿❤☯... VIP 4 GP
- NT Nguyễn Thị Bảo Linh 4 GP
- NT Nguyễn Thanh Trúc 4 GP
- NB Nguyễn Bá Tĩnh 4 GP
- NT Nguyễn Trường An 4 GP
Các khóa học có thể bạn quan tâm
Mua khóa học Tổng thanh toán: 0đ (Tiết kiệm: 0đ) Tới giỏ hàng ĐóngYêu cầu VIP
Học liệu này đang bị hạn chế, chỉ dành cho tài khoản VIP cá nhân, vui lòng nhấn vào đây để nâng cấp tài khoản.
Từ khóa » Cân Bằng Hno3+hcl
-
HNO3 + HCl = NO + Cl2 + H2O - Trình Cân Bằng Phản ứng Hoá Học
-
HCl HNO3 = Cl2 H2O NO | Cân Bằng Phương Trình Hóa Học
-
Cân Bằng Phương Trình Hóa Học HNO3 + HCl Tạo Thành NO + Cl2 + ...
-
HCl + HNO3 | Cl2 + H2O + NO | Cân Bằng Phương Trình Hóa Học
-
Cân Bằng Phản ứng HNO3 + HCl = Cl2 + H2O + NO (và Phương ...
-
HCl + HNO3 | Cl2 + H2O + NOCl | Cân Bằng Phương Trình Hóa Học
-
Cho Phương Trình Phản ứng: HNO3 + HCl → NO2 + Cl2 + H2OCác
-
HNO3 + HCl → NO2 + Cl2 + H2O Các Hệ Số Cân Bằng Trong Phương ...
-
Khử Sau Bằng Các Phương Pháp Thăng Bằng Electron : A ... - Hoc24
-
Cân Bằng Phương Trình Hóa Học Của Các Phản ứng Oxi Hóa - Selfomy
-
Cân Bằng Phản ứng HCl + HNO3 | Cl2 + H2O + NO (và ... - BYTUONG
-
FeS2 + 5 HNO3 + 3 HCl → FeCl3 + 5 NO + 2 H2SO4 + 2 H2O
-
Interaction In The Ternary Complexes Of HNO3···HCl···H2O - PubMed
-
Au + HNO 3 + 4HCl → H[AuCl 4 ] + NO + 2H 2 O - Haylamdo