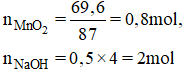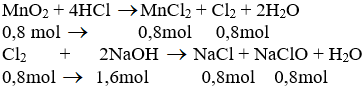Cho 26 1g Mno2 Vào Dung Dịch Hcl Dư Thu được Khí(x),cho ... - Hoc24
Có thể bạn quan tâm
HOC24
Lớp học Học bài Hỏi bài Giải bài tập Đề thi ĐGNL Tin tức Cuộc thi vui Khen thưởng- Tìm kiếm câu trả lời Tìm kiếm câu trả lời cho câu hỏi của bạn
Lớp học
- Lớp 12
- Lớp 11
- Lớp 10
- Lớp 9
- Lớp 8
- Lớp 7
- Lớp 6
- Lớp 5
- Lớp 4
- Lớp 3
- Lớp 2
- Lớp 1
Môn học
- Toán
- Vật lý
- Hóa học
- Sinh học
- Ngữ văn
- Tiếng anh
- Lịch sử
- Địa lý
- Tin học
- Công nghệ
- Giáo dục công dân
- Tiếng anh thí điểm
- Đạo đức
- Tự nhiên và xã hội
- Khoa học
- Lịch sử và Địa lý
- Tiếng việt
- Khoa học tự nhiên
- Hoạt động trải nghiệm
- Hoạt động trải nghiệm, hướng nghiệp
- Giáo dục kinh tế và pháp luật
Chủ đề / Chương
Bài học
HOC24
 Khách vãng lai Đăng nhập Đăng ký Khám phá Hỏi đáp Đề thi Tin tức Cuộc thi vui Khen thưởng
Khách vãng lai Đăng nhập Đăng ký Khám phá Hỏi đáp Đề thi Tin tức Cuộc thi vui Khen thưởng - Tất cả
- Toán
- Vật lý
- Hóa học
- Sinh học
- Ngữ văn
- Tiếng anh
- Lịch sử
- Địa lý
- Tin học
- Công nghệ
- Giáo dục công dân
- Tiếng anh thí điểm
- Hoạt động trải nghiệm, hướng nghiệp
- Giáo dục kinh tế và pháp luật
Câu hỏi
Hủy Xác nhận phù hợp Chọn lớp Tất cả Lớp 12 Lớp 11 Lớp 10 Lớp 9 Lớp 8 Lớp 7 Lớp 6 Lớp 5 Lớp 4 Lớp 3 Lớp 2 Lớp 1 Môn học Toán Vật lý Hóa học Sinh học Ngữ văn Tiếng anh Lịch sử Địa lý Tin học Công nghệ Giáo dục công dân Tiếng anh thí điểm Đạo đức Tự nhiên và xã hội Khoa học Lịch sử và Địa lý Tiếng việt Khoa học tự nhiên Hoạt động trải nghiệm Hoạt động trải nghiệm, hướng nghiệp Giáo dục kinh tế và pháp luật Mới nhất Mới nhất Chưa trả lời Câu hỏi hay
- Nguyễn Toàn
cho 26 1g mno2 vào dung dịch hcl dư thu được khí(x),cho khí (x) vào 250 ml dung dịch koh 3m người ta thu được dung dịch (a),
a)viết phương trình hóa học sảy ra
b) tính nồng độ mol của dung Dịch A.
(cho Mn=55,0=16,h=1, cl=35,5,k=39)
các bạn giúp mình với nha
Xem chi tiết Lớp 9 Hóa học Chương III. Sơ lược về bảng tuần hoàn các nguyên t... 2 0 Gửi Hủy
Gửi Hủy  Phạm Triệu YH 13 tháng 3 2017 lúc 20:50
Phạm Triệu YH 13 tháng 3 2017 lúc 20:50 nMnO2=261/87=3 mol
nKOH=(250/1000)*3=0.75 mol
a, PTHH
MnO2 + 4HCl = MnCl2 + Cl2 + 2H2O (1)
Cl2 + 2KOH = KCl + KClO + H2O (2)
Cl2 + H2O = HCl + HClO (3)
b, Theo pt (1),(2) ta có:
nMnO2 = nCl2 = 3 mol
==> nCl2 pứ ở pt 2 = 0.5*nKOH = 0.5* 0.75 = 0.375 mol
==>nKCl = n KClO = 0.5*nKOH = 0.375 mol
nCl2 pứ ở pt 3 = nCl2 ban đầu - nCL2 pứ ở pt 2 = 3 - 0.375 = 2.625 mol
nHCl = nHClO = nCl2 = 2.675 mol
ta có thể tích dung dịch ko thay đổi sau pứ (giả sử)
CM KCl = 0.375/0.25= 1.5 M
CM KClO = 0.375/0.25= 1.5 M
CM HCl = 2.675/0.25 = 10.7 M
CM HClO = 2.675/0.25 = 10.7 M
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy  Nguyễn Toàn 7 tháng 3 2017 lúc 16:19
Nguyễn Toàn 7 tháng 3 2017 lúc 16:19 26,1 g nha các bạn
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Nguyễn Văn A
Cho 1 ít viên kẽm(zinc) dư vào 100ml dung dịch acid HCl. Phản ứng xong thu được 2,479 lít khí (đkc)
a/ viết phương trình hóa học xảy ra
b/ tính khối lượng kẽm tham gia phản ứng?
c/ tính nồng độ mol của dung dịch HCl đã dùng?
Cho Zn=65, Cl=35,5, O=16, H=1
Xem chi tiết Lớp 9 Hóa học 1 0 Gửi Hủy
Gửi Hủy  nguyễn thị hương giang
nguyễn thị hương giang  8 tháng 10 2021 lúc 11:13
8 tháng 10 2021 lúc 11:13 \(n_{H_2}=\dfrac{2,479}{22,4}=\dfrac{2479}{22400}mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Theo pt ta có: \(n_{Zn}=n_{H_2}=\dfrac{2479}{22400}mol\)\(\approx0,11mol\)
\(\Rightarrow m_{Zn}\approx7,2g\)
\(n_{HCl}=2n_{H_2}=0,22mol\) \(\Rightarrow C_{M_{HCl}}=\dfrac{0,22}{0,1}=2,2M\)
Đúng 0 Bình luận (0)
 Gửi Hủy
Gửi Hủy 
- Nhật Linh
Cho 69,6g MnO2 tác dụng với dung dịch HCl đặc dư thu được một lượng khí X. Dẫn khí X vào 500ml dung dịch NaOH 4M thu được dung dịch A. Tính nồng độ mol của các chất trong dung dịch A. Giả thiết rằng thể tích dung dịch sau phản ứng thay đổi không đáng kể.
Xem chi tiết Lớp 9 Hóa học Bài 32. Luyện tập chương III : Phi kim - Sơ lược v... 1 0 Gửi Hủy
Gửi Hủy  ....
....  13 tháng 10 2021 lúc 9:23
13 tháng 10 2021 lúc 9:23
a) Phương trình hóa học của phản ứng:
b) Theo pt (1): nCl2 = nMnCl2 = nMnO2 = 0,8 mol
Theo pt (2): nNaCl = nNaClO = nCl2 = 0,8 mol
nNaOH pư = 2. nCl2 = 2. 0,8 = 1,6 mol
⇒ nNaOH dư = 2 - 1,6 = 0,4 mol
Nồng độ mol/l của các chất trong dung dịch sau phản ứng:
CM (NaCl) = CM (NaClO) = CM(MnCl2) = 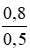
CM (NaOH)dư = 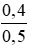
tích cho mình nha![]()
 Gửi Hủy
Gửi Hủy 
- Nguyễn Hoàng Nam
Cho 2,34 gam Mg vào 250 ml dung dịch X chứa hỗn hợp Fe(NO3)3 0,12M và Cu(NO3)2, sau một thời gian thu được 3,78 gam kết tủa và dung dịch Y chứa 3 muối. Lọc bỏ kết tủa, cho dung dịch NaOH đến dư vào dung dịch Y (trong điều kiện không có không khí) thì lượng kết tủa lớn nhất thu được là 8,63 gam. Viết các phương trình hóa học xảy ra và tính nồng độ mol của Cu(NO3)2 trong dung dịch X.
Xem chi tiết Lớp 9 Hóa học 1 0 Gửi Hủy
Gửi Hủy  Ngô Quang Sinh
Ngô Quang Sinh  16 tháng 1 2017 lúc 9:56
16 tháng 1 2017 lúc 9:56 nMg = 0,0975
nFe(NO3)3 = 0,03
Dung dịch Y gồm Mg(NO3)2, Fe(NO3)2, Cu(NO3)2
Mg + 2Fe3+ Mg2+ + 2Fe2+
0,015 0,03 0,015
Mg + Cu2+ Mg2+ + Cu
x x x →x
m chất rắn tăng = -24 . 0,015 + (64-24).x = 3,78 - 2,34
=> x = 0,045
Dung dịch Y gồm Mg(NO3)2: 0,015 + x = 0,06; Fe(NO3)2: 0,03; Cu(NO3)2: y
Kết tủa Mg(OH)2: 0,06; Fe(OH)2:0,03; Cu(OH)2:y
mkết tủa = 0,06 . 58 + 0,03 . 90 + 98 . y = 8,63
=> y = 0,025
=> nCu(NO3)2 = 0,045 + 0,025 = 0,07
=> CM = 0,28
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Hacker
hoà tan a gam hỗn hợp Na2CO3 và KHCO3 vào H2O để được 400 ml dung dịch A.cho từ từ 100 ml dung dịch HCl 1.5 M vào dung dịch A, thu được dung dịch B và 1.008 l khí ( ở đktc) . cho B tác dụng với dung dịch Ba(OH)2 dư thu được 29.55 gam kết tủa.1/ tính a2/ tính nồng độ mol của các ion trong dung dịch A ( bỏ qua sự cho nhận của proton của các ion HCO3- , CO3 (2-)3/ người ta lại cho từ từ dung dịch A vào bình đựng 100 ml dung dịch HCl 1.5 M. tính thể tích khí CO2 tạo ra ở đktc?
Xem chi tiết Lớp 10 Hóa học Bài 24: Sơ lược về hợp chất có oxi của Clo 1 0 Gửi Hủy
Gửi Hủy  Võ Đông Anh Tuấn 14 tháng 9 2016 lúc 11:38
Võ Đông Anh Tuấn 14 tháng 9 2016 lúc 11:38 1/ Gọi x, y lần lượt là số mol của Na2CO3 và KHCO3.Khi cho từ từ HCl vào dung dịch A thì các phản ứng xảy ra lần lượt là :CO3^2- + H^+ => HCO3-x ---------> x ----------> x HCO3^- + H+ => H2O + CO2.0,045 <--- 0,045 <-------- 0,045.........HCO3^- + OH- => CO3^2- + H2O.x+y - 0,045 -------------> x+y-0,045.Giải hệ: x+y-0,045 = 29,55/197; n HCl = x+ 0,045 = 0,15.=> x = 0,105 ; y = 0,09.2/ Nồng độ của HCO3- , CO3^2- lần lượt là 0,225 M; 0,2625 M.3/ Cho từ từ dung dịch A vào bình đựng 100 ml dung dịch HCl 1,5 M => Các phản ứng xảy ra đồng thời:CO3^2- + 2 H^+ => H2O + CO2.HCO3- + H+ => H2O + CO2.Do tỉ lệ trong hỗn hợp : n CO3^2-/ n HCO3- = 7/6 => 7x*2+6x = 0,15 => x=0,0075.=> V = 2,184 lít.
Đúng 0 Bình luận (1) Gửi Hủy
Gửi Hủy 
- đoàn thảo
cho 10,44g Mno2 tác dụng với axit HCL đặc thu được dung dịch X và khí Y.
a. tính thể tích khí Y thoát ra
b. khi thoát ra cho tác dụng với 100ml dung dịch NAOH 4 ( M). viết phương trình hoá học và tính nồng độ mol của các chất trong dung dịchthu được sau phản ứng. coi thể tích dung dịch thay đổi không đáng kể
Xem chi tiết Lớp 9 Hóa học 1 0
 Gửi Hủy
Gửi Hủy  ๖ۣۜDũ๖ۣۜN๖ۣۜG
๖ۣۜDũ๖ۣۜN๖ۣۜG  22 tháng 3 2022 lúc 14:08
22 tháng 3 2022 lúc 14:08 a) \(n_{MnO_2}=\dfrac{10,44}{87}=0,12\left(mol\right)\)
PTHH: MnO2 + 4HCl --> MnCl2 + Cl2 + 2H2O
0,12----------------------->0,12
=> VCl2 = 0,12.22,4 = 2,688 (l)
b)
nNaOH = 0,1.4 = 0,4 (mol)
PTHH: 2NaOH + Cl2 --> NaCl + NaClO + H2O
0,24<---0,12--->0,12--->0,12
=> dd sau pư chứa \(\left\{{}\begin{matrix}NaOH_{dư}:0,4-0,24=0,16\left(mol\right)\\NaCl:0,12\left(mol\right)\\NaClO:0,12\left(mol\right)\end{matrix}\right.\)
\(\left\{{}\begin{matrix}C_{M\left(NaOH_{dư}\right)}=\dfrac{0,16}{0,1}=1,6M\\C_{M\left(NaCl\right)}=\dfrac{0,12}{0,1}=1,2M\\C_{M\left(NaClO\right)}=\dfrac{0,12}{0,1}=1,2M\end{matrix}\right.\)
Đúng 3 Bình luận (0) Gửi Hủy
Gửi Hủy 
- hồ bảo thành
Sục Cl2 vào dung dịch KOH loãng thu được dung dịch A, hòa tan I2 vào dung dịch KOH loãng thu được dung dịch B (tiến hành ở nhiệt độ phòng).
1) Viết phương trình hóa học xảy ra.
2) Viết phương trình hóa học xảy ra khi cho lần lượt các dung dịch: hỗn hợp HCl và FeCl2, Br2, H2O2, CO2 vào dung dịch A (không có Cl2 dư, chỉ chứa các muối).
Xem chi tiết Lớp 0 Hóa học 1 0 Gửi Hủy
Gửi Hủy  hóa 13 tháng 3 2016 lúc 11:03
hóa 13 tháng 3 2016 lúc 11:03 a) Ở nhiệt độ thường:
2KOH + Cl2 \(\rightarrow\) KCl + KClO + H2O
6KOH + 3I2 \(\rightarrow\) 5KI + KIO3 + 3H2O
(Trong môi trường kiềm tồn tại cân bằng : \(\text{3XO- ⇌X- + XO}_3^-\)
Ion ClO- phân hủy rất chậm ở nhiệt độ thường và phân hủy nhanh khi đun nóng, ion IO- phân hủy ở tất cả các nhiệt độ).
b) Các phương trình hóa học :
Ion ClO- có tính oxi hóa rất mạnh, thể hiện trong các phương trình hóa học:
- Khi cho dung dịch FeCl2 và HCl vào dung dịch A có khí vàng lục thoát ra và dung dịch từ không màu chuyển sang màu vàng nâu :
2FeCl2 + 2KClO + 4HCl \(\rightarrow\) 2FeCl3 + Cl2 + 2KCl + 2H2O
- Khi cho dung dịch Br2 vào dung dịch A, dung dịch brom mất màu :
Br2 + 5KClO + H2O \(\rightarrow\) 2HBrO3 + 5KCl
- Khi cho H2O2 vào dung dịch A, có khí không màu, không mùi thoát ra:
H2O2 + KClO \(\rightarrow\) H2O + O2 + KCl
- khi cho CO2 vào A
CO2 + KClO + H2O \(\rightarrow\) KHCO3 + HClO
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Nguyễn Hữu Khánh
Sục 3,36 lít khí SO2 (ở đktc) vào 200 ml dung dịch KOH 1 M, sau phản ứng thu được dung dịch X. Cô cạn dung dịch X thu được m gam chất rắn khan. (a) Viết phương trình hóa học xảy ra. (b) Tính m
Xem chi tiết Lớp 9 Hóa học Chương I. Các loại hợp chất vô cơ 1 0 Gửi Hủy
Gửi Hủy  hnamyuh
hnamyuh  20 tháng 8 2021 lúc 21:30
20 tháng 8 2021 lúc 21:30 a)
$2KOH + SO_2 \to K_2SO_3 + H_2O$
$KOH + SO_2 \to KHSO_3$
b)
Gọi $n_{K_2SO_3} = a(mol) ; n_{KHSO_3} = b(mol)$Ta có :
$n_{KOH} = 2a + b = 0,2(mol)$$n_{SO_2} = a + b= 0,15(mol)$
Suy ra a = 0,05 ; b = 0,1
$m = 0,05.158 + 0,1.120 = 19,9(gam)$
Đúng 2 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Nguyễn Đỗ Minh Tâm
Cho 69,6 (g) MnO2 tác dụng với dung dịch HCl đặc (dư) thu được một lượng khí X. Dẫn khí X vào 500 (ml) dung dịch NaOH 4M, biết D=1,25 (g/ml) thu được dung dịch A
a) Tính thể tích khí X (đktc)
b) Tính nồng độ mol các chất có trong dung dịch A
Xem chi tiết Lớp 8 Hóa học Bài 43. Pha chế dung dịch 1 0 Gửi Hủy
Gửi Hủy  Do Minh Tam 14 tháng 6 2016 lúc 14:08
Do Minh Tam 14 tháng 6 2016 lúc 14:08 nMnO2=69,6/87=0,8 molMnO2 +4 HCl =>MnCl2 +Cl2 +2H2O0,8 mol =>0,8 molkhí X là Cl2VCl2=0,8.22,4=17,92 lit
nNaOHbđ=0,5.4=2 molCl2 +2NaOH =>NaCl +NaClO +H2O0,8 mol=>1,6 mol=>0,8 mol=>0,8 moldư 0,4 molCM dd NaOH dư=0,4/0,5=0,8MCM dd NaCl=CM dd NaClO=0,8/0,5=1,6M0,8 mol
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Nguyễn Hoàng Nam
Hấp thụ hết 5,6 lít khí CO2 (đktc) vào dung dịch chứa x mol KOH và y mol K2CO3, thu được 250 ml dung dịch X. Cho từ từ đến hết 125 ml dung dịch X vào 375 ml dung dịch HCl 0,5M, thu được 3,36 lít khí (đktc). Mặt khác, cho 125 ml dung dịch X tác dụng với dung dịch Ba(OH)2 dư, thu được 49,25 gam kết tủa. Giá trị của x là
A. 0,100.
B. 0,125
C. 0,050.
D. 0,300.
Xem chi tiết Lớp 11 Hóa học 1 0 Gửi Hủy
Gửi Hủy  Ngô Quang Sinh
Ngô Quang Sinh  28 tháng 9 2019 lúc 3:59
28 tháng 9 2019 lúc 3:59 Đáp án B
► Xét TN1: đặt nCO32– phản ứng = a; nHCO3– phản ứng = b.
⇒ nCO2 = a + b = 0,15 mol; nHCl phản ứng = 2a + b = 0,1875 mol
||⇒ giải hệ có: a = 0,0375 mol; b = 0,1125 mol ⇒ nCO32–/X : nHCO3–/X = a : b = 1 : 3.
► Xét TN2: ∑nC/X = n↓ = 0,25 mol ⇒ 250 ml X chứa 0,5 mol C.
Bảo toàn nguyên tố Cacbon: y = 0,5 – 0,25 = 0,25 mol.
● Chia 0,5 mol C thành 0,125 mol CO32– và 0,375 mol HCO3–.
Bảo toàn điện tích: nK+ = 0,625 mol. Bảo toàn nguyên tố Kali:
x = 0,625 – 0,25 × 2 = 0,125 mol
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy Từ khóa » Cho 26 1g Mno2 Tác Dụng Với Dung Dịch Hcl
-
Cho 26,1 G MnO2 Tác Dụng Với Dung Dịch HCl Dư ...
-
Cho 26,1g MnO2 Tác Dụng Hết Với Dung Dịch HCl Lấy Dư . Toàn Bộ ...
-
Cho 26,1 Gam MnO2 Tác Dụng Với Dung Dịch HCl Dư Thu được 6,048 ...
-
Câu 6: Cho 26,1 G MnO2 Tác Dụng Với Dung Dịch HCl Dư Thu ...
-
Cho 26,1g MnO2 Tác Dụng Hết Với 400ml Dung Dịch Axit Clohidric ...
-
Cho 26,1g MnO2 Tác Dụng Hết Với Dung Dịch HCl (đặc) Thu được Khí ...
-
Top 15 Cho 26 1g Mno2 Tác Dụng Với Dung Dịch Hcl - MarvelVietnam
-
Cho 26,1 Gam MnO2 Vào Dung Dịch HCl đặc, Nóng, Dư. Khí Cl2 Thoát ...
-
Cho 26 1g MnO2 Tác Dụng Với Dung Dịch HCl Có 20g HCl - Hàng Hiệu
-
Câu 0 Cho 261 G MnO2 Tác Dụng Với D... | Xem Lời Giải Tại QANDA
-
. Cho 26,1g MnO2 Tác Dụng Hết Với 400ml Dung Dịch Axit ... - Hoc24
-
Cho 26,1g MnO2 Tác Dụng Với.... - Selfomy Hỏi Đáp
-
Cho 26,1g MnO2 Tác Dụng Với HCl đặc, Lấy Cl2 Dần Vào Dung Dịch ...
-
Tính Hiệu Suất Phản ứng? - Mỹ Duyên