Cho 29,8 Gam Hh Gồm Zn Và Fe Vào 600ml Dd CuSO4 0,5M . Sau Khi ...
Có thể bạn quan tâm
HOC24
Lớp học Học bài Hỏi bài Giải bài tập Đề thi ĐGNL Tin tức Cuộc thi vui Khen thưởng- Tìm kiếm câu trả lời Tìm kiếm câu trả lời cho câu hỏi của bạn
Lớp học
- Lớp 12
- Lớp 11
- Lớp 10
- Lớp 9
- Lớp 8
- Lớp 7
- Lớp 6
- Lớp 5
- Lớp 4
- Lớp 3
- Lớp 2
- Lớp 1
Môn học
- Toán
- Vật lý
- Hóa học
- Sinh học
- Ngữ văn
- Tiếng anh
- Lịch sử
- Địa lý
- Tin học
- Công nghệ
- Giáo dục công dân
- Tiếng anh thí điểm
- Đạo đức
- Tự nhiên và xã hội
- Khoa học
- Lịch sử và Địa lý
- Tiếng việt
- Khoa học tự nhiên
- Hoạt động trải nghiệm
- Hoạt động trải nghiệm, hướng nghiệp
- Giáo dục kinh tế và pháp luật
Chủ đề / Chương
Bài học
HOC24
 Khách vãng lai Đăng nhập Đăng ký Khám phá Hỏi đáp Đề thi Tin tức Cuộc thi vui Khen thưởng
Khách vãng lai Đăng nhập Đăng ký Khám phá Hỏi đáp Đề thi Tin tức Cuộc thi vui Khen thưởng - Tất cả
- Toán
- Vật lý
- Hóa học
- Sinh học
- Ngữ văn
- Tiếng anh
- Lịch sử
- Địa lý
- Tin học
- Công nghệ
- Giáo dục công dân
- Tiếng anh thí điểm
- Hoạt động trải nghiệm, hướng nghiệp
- Giáo dục kinh tế và pháp luật
Câu hỏi
Hủy Xác nhận phù hợp Chọn lớp Tất cả Lớp 12 Lớp 11 Lớp 10 Lớp 9 Lớp 8 Lớp 7 Lớp 6 Lớp 5 Lớp 4 Lớp 3 Lớp 2 Lớp 1 Môn học Toán Vật lý Hóa học Sinh học Ngữ văn Tiếng anh Lịch sử Địa lý Tin học Công nghệ Giáo dục công dân Tiếng anh thí điểm Đạo đức Tự nhiên và xã hội Khoa học Lịch sử và Địa lý Tiếng việt Khoa học tự nhiên Hoạt động trải nghiệm Hoạt động trải nghiệm, hướng nghiệp Giáo dục kinh tế và pháp luật Mới nhất Mới nhất Chưa trả lời Câu hỏi hay
- Mai Anh
Cho 29,8 gam hh gồm Zn và Fe vào 600ml dd CuSO4 0,5M . Sau khi phản ứng xảy ra hoàn toàn, thu được dd X và 30,4g hh kim loại . Tính % khối lượng Fe có trong hh đầu
Xem chi tiết Lớp 9 Hóa học Chương I. Các loại hợp chất vô cơ 3 0 Gửi Hủy
Gửi Hủy  Phạm Thị Thanh Huyền 11 tháng 11 2018 lúc 19:57 https://i.imgur.com/bVnR9Ye.png Đúng 0 Bình luận (0)
Phạm Thị Thanh Huyền 11 tháng 11 2018 lúc 19:57 https://i.imgur.com/bVnR9Ye.png Đúng 0 Bình luận (0)  Gửi Hủy
Gửi Hủy  Phạm Thị Thanh Huyền 11 tháng 11 2018 lúc 19:58 https://i.imgur.com/Ha1MVcO.png Đúng 0 Bình luận (0)
Phạm Thị Thanh Huyền 11 tháng 11 2018 lúc 19:58 https://i.imgur.com/Ha1MVcO.png Đúng 0 Bình luận (0)  Gửi Hủy
Gửi Hủy  Phạm Thị Thanh Huyền 11 tháng 11 2018 lúc 19:58
Phạm Thị Thanh Huyền 11 tháng 11 2018 lúc 19:58 hơi khó hiểu vì mình làm tắt. bạn cố đọc kĩ sẽ nhanh hiểu thôi
Đúng 0 Bình luận (2) Gửi Hủy
Gửi Hủy 
- Mai Anh
Cho 19,8 gam hh gồm Zn và Fe vào 600ml dd CuSO4 0,5M . Sau khi phản ứng xảy ra hoàn toàn, thu được dd X và 30,4g hh kim loại . Tính % khối lượng Fe có trong hh đầu
Xem chi tiết Lớp 9 Hóa học Chương I. Các loại hợp chất vô cơ 4 0 Gửi Hủy
Gửi Hủy  Phạm Thị Thanh Huyền 14 tháng 11 2018 lúc 20:22 https://i.imgur.com/inRPytN.png Đúng 0 Bình luận (0)
Phạm Thị Thanh Huyền 14 tháng 11 2018 lúc 20:22 https://i.imgur.com/inRPytN.png Đúng 0 Bình luận (0)  Gửi Hủy
Gửi Hủy  Phạm Thị Thanh Huyền 14 tháng 11 2018 lúc 20:23 https://i.imgur.com/f6FQ0wH.png Đúng 0 Bình luận (0)
Phạm Thị Thanh Huyền 14 tháng 11 2018 lúc 20:23 https://i.imgur.com/f6FQ0wH.png Đúng 0 Bình luận (0)  Gửi Hủy
Gửi Hủy  Phạm Thị Thanh Huyền 14 tháng 11 2018 lúc 20:22
Phạm Thị Thanh Huyền 14 tháng 11 2018 lúc 20:22 
 Gửi Hủy Xem thêm câu trả lời
Gửi Hủy Xem thêm câu trả lời 
- Nguyễn Hoàng Nam
Cho 29,8 gam hỗn hợp bột gồm Zn và Fe vào 600 ml dung dịch CuSO4 0,5M. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X và 30,4 gam hỗn hợp kim loại. Phần trăm về khối lượng của Fe trong hỗn hợp ban đầu là
A. 56,37%
B. 64,42%
C. 43,62%
D. 37,58%
Xem chi tiết Lớp 12 Hóa học 1 0 Gửi Hủy
Gửi Hủy  Ngô Quang Sinh
Ngô Quang Sinh  28 tháng 5 2019 lúc 2:40
28 tháng 5 2019 lúc 2:40 Đáp án A
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Nguyễn Hoàng Nam
Cho 21,6 gam hỗn hợp bột gôm Mg và Fe vào 600 ml dd CuSO4 0,5M. Sau khi các phản ứng xảy ra hoàn toàn, thu được dd X và 30,4 gam hỗn hợp kim loại. Phần trăm về khối lượng của Fe trong hỗn hợp ban đầu là
A. 77,78%.
B. 22,22%.
C. 51,85%.
D. 48,15%
Xem chi tiết Lớp 0 Hóa học 1 0 Gửi Hủy
Gửi Hủy  Ngô Quang Sinh
Ngô Quang Sinh  10 tháng 5 2017 lúc 9:31
10 tháng 5 2017 lúc 9:31  Chọn A
Chọn A
 Gửi Hủy
Gửi Hủy 
- Nguyễn Hoàng Nam
Cho hh gồm Fe và Zn vào dd AgNO3 đến khi các pư xảy ra hoàn toàn, thu được dd X gồm hai muối và chất rắn Y gồm hai kim loại. Hai muối trong X là
A. Fe(NO3)3 và Zn(NO3)2.
B. Zn(NO3)2 và Fe(NO3)2.
C. AgNO3 và Zn(NO3)2.
D. Fe(NO3)2 và AgNO3.
Xem chi tiết Lớp 0 Hóa học 1 0 Gửi Hủy
Gửi Hủy  Ngô Quang Sinh
Ngô Quang Sinh  2 tháng 2 2019 lúc 11:47
2 tháng 2 2019 lúc 11:47 Đáp án B
Hai muối tạo ra phải là muối của kim loại mạnh Zn và Fe
Hai kim loại tạo ra phải 1à 2 kim 1oại yếu 1à Ag và Fe => Fe dư => Muối thu được là muối Fe(NO3)2
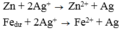
 Gửi Hủy
Gửi Hủy 
- bánh mì que
hoà tan hoàn toàn 16,2 g hh gồm kim loại kiềm M và oxit của nó vào h2o thu được V lít H2 đktc. lấy dd vừa thu được cho vào 50ml dd alcl3 0,5M sau khi phản ứng xảy ra hoàn toàn thu được 15,6 gam tủa
tìm M và V
Xem chi tiết Lớp 11 Hóa học 1 0 Gửi Hủy
Gửi Hủy  nguyệt ánh 7 tháng 11 2023 lúc 16:19
nguyệt ánh 7 tháng 11 2023 lúc 16:19 Câu 3. Hòa tan 16,2 g hh kim loại kiềm và oxit của nó thu được V lít H2 ( đktc) ,lấy dd sau pư cho vào 50 ml dd AlCl3 0,5 M ,sau khi pư xẩy ra hoàn toàn thu được 15,6 gm kết tủa .xác định M
Đúng 0 Bình luận (0)
 Gửi Hủy
Gửi Hủy 
- Lưu Nhân
hòa tan hoàn toàn 13,9g hh gồm al và fe trong đd axit hcl 14,6% vừa đủ sau phản ứng thoát ra 7,84 l khí h2 ở đktc , thu đc dd X a) vieeta pthhb)tính khối lượng mỗi kim loại trong hh ban đầu c) tính nồng độ phần trăm mỗi muối trong dd X
Xem chi tiết Lớp 9 Hóa học Chương II. Kim loại 2 0 Gửi Hủy
Gửi Hủy  Nguyễn Hoàng Minh
Nguyễn Hoàng Minh  9 tháng 12 2021 lúc 21:00
9 tháng 12 2021 lúc 21:00 \(\text{Đặt }n_{Al}=x(mol);n_{Fe}=y(mol)\\ \Rightarrow 27x+56y=13,9(1)\\ n_{H_2}=\dfrac{7,84}{22,4}=0,35(mol)\\ a,PTHH:2Al+6HCl\to 2AlCl_3+3H_2(1)\\ Fe+2HCl\to FeCl_2+H_2(2)\\ b,\text{Từ 2 PT: }1,5x+y=0,35(2)\\ (1)(2)\Rightarrow x=0,1(mol);y=0,2(mol)\\ \Rightarrow m_{Al}=0,1.27=2,7(g)\\ m_{Fe}=0,2.56=11,2(g)\)
\(c,n_{HCl(1)}=3n_{Al}=0,3(mol);n_{AlCl_3}=0,1(mol);n_{H_2(1)}=0,15(mol)\\ \Rightarrow m_{dd_{HCl(1)}}=\dfrac{0,3.36,5}{14,6\%}=75(g)\\ \Rightarrow C\%_{AlCl_3}=\dfrac{0,1.133,5}{2,7+75-0,15.2}.100\%=17,25\%\)
\(n_{HCl(2)}=2n_{Fe}=0,4(mol);n_{FeCl_2}=n_{H_2(2)}=n_{Fe}=0,2(mol)\\ \Rightarrow m{dd_{HCl(2)}}=\dfrac{0,4.36,5}{14,6\%}=100(g)\\ \Rightarrow C\%_{FeCl_2}=\dfrac{0,2.127}{11,2+100-0,2.2}.100\%=22,92\%\)
Đúng 1 Bình luận (0) Gửi Hủy
Gửi Hủy  ๖ۣۜDũ๖ۣۜN๖ۣۜG
๖ۣۜDũ๖ۣۜN๖ۣۜG  9 tháng 12 2021 lúc 21:05
9 tháng 12 2021 lúc 21:05 a) 2Al + 6HCl --> 2AlCl3 + 3H2
Fe + 2HCl --> FeCl2 + H2
b) Gọi số mol Al, Fe lần lượt là a,b
=> 27a + 56b = 13,9
\(n_{H_2}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\)
2Al + 6HCl --> 2AlCl3 + 3H2
a----->3a--------->a------->1,5a______(mol)
Fe + 2HCl --> FeCl2 + H2
b------>2b-------->b----->b__________(mol)
=> 1,5a + b = 0,35
=> \(\left\{{}\begin{matrix}a=0,1=>m_{Al}=0,1.27=2,7\left(g\right)\\b=0,2=>m_{Fe}=0,2.56=11,2\left(g\right)\end{matrix}\right.\)
c) nHCl = 3a + 2b = 0,7 (mol)
=> mHCl = 0,7.36,5 = 25,55(g)
=> \(m_{ddHCl}=\dfrac{25,55.100}{14,6}=175\left(g\right)\)
\(m_{dd\left(saupu\right)}=13,9+175-2.0,35=188,2\left(g\right)\)
\(\left\{{}\begin{matrix}m_{AlCl_3}=0,1.133,5=13,35\left(g\right)\\m_{FeCl_2}=0,2.127=25,4\left(g\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}C\%\left(AlCl_3\right)=\dfrac{13,35}{188,2}.100\%=7,1\%\\C\%\left(FeCl_2\right)=\dfrac{25,4}{188,2}.100\%=13,5\%\end{matrix}\right.\)
Đúng 1 Bình luận (0)
 Gửi Hủy
Gửi Hủy 
- Huỳnh Anh
cho hỗn hợp gồm 1,12g Fe và 1,93g Cu vào 400ml dd chứa hh gồm H2SO4 0,5M và NaNO3 0,2M Sau khi các phản ứng xảy ra hoàn toàn , thu được dd X và khí NO.Cho V ml dd NaOH vào dd X thì lượng kết tủa thu được lớn nhất.Giá trị tối thiểu của V là bao nhiêu?
Xem chi tiết Lớp 12 Hóa học Chủ đề: Polime 2 0 Gửi Hủy
Gửi Hủy  Đặng Thị Cẩm Tú 13 tháng 7 2016 lúc 12:49
Đặng Thị Cẩm Tú 13 tháng 7 2016 lúc 12:49 Số mol Fe và Cu lần lượt là 0,02 và 0,03 mol. 3Cu + 8H+ + 2NO3- ---> 3Cu2+ + 2NO + 4H2O Fe + 4H+ + NO3- ---> Fe3+ + NO + 2H2O Ta tính được số mol H+ dư là 0,24 mol Số mol NO3- dư là 0,04 mol. Vậy trong dung dịch X lúc này có 0,02 mol Fe3+ 0,03 mol Cu2+ 0,24 mol H+ Vậy lượng NaOH cần dùng là 0,02*3 + 0,03*2 + 0,24*1 = 0,36 mol Vì không có nồng độ của dung dịch NaOH nên tiếp theo thì... chịu ^^
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy  Đinh Tuấn Việt 13 tháng 7 2016 lúc 12:51
Đinh Tuấn Việt 13 tháng 7 2016 lúc 12:51 
 Gửi Hủy
Gửi Hủy 
- Υσɾυshἱκα Υυɾἱ
cho 18,6 g hh A gồm Zn và Fe vào dd chứa 0,5a mol HCl. Khi PƯ xảy ra hoàn toàn, cô cạn dd thu được 34,575 g chất rắn. Lập lại thí nghiệm trên với dd chứa a mol HCl rồi cô cạn thì thu được 39,9 g chất rắn. Tính a và khối lượng mỗi kim loại trong 18,6 g hh A
Xem chi tiết Lớp 8 Hóa học Bài 33: Điều chế Hiđro - Phản ứng thế 1 0 Gửi Hủy
Gửi Hủy  ๖ۣۜDũ๖ۣۜN๖ۣۜG
๖ۣۜDũ๖ۣۜN๖ۣۜG  5 tháng 2 2022 lúc 21:40
5 tháng 2 2022 lúc 21:40 Do ở TN2, khi tăng lượng HCl, khối lượng rắn tăng thêm
=> Trong TN1, HCl hết, kim loại dư
- Xét TN1
Theo ĐLBTKL: mA + mHCl = mrắn sau pư + mH2
=> 18,6 + 36,5.0,5a = 34,575 + 2.0,25a
=> a = 0,9
- Xét TN2:
Giả sử HCl hết
Theo ĐLBTKL: 18,6 + 0,9.36,5 = 39,9 + 0,45.2
=> 51,45 = 40,8 (vô lí)
=> HCl dư, kim loại hết
Gọi số mol Zn, Fe là a, b
=> 65a + 56b = 18,6
PTHH: Zn + 2HCl --> ZnCl2 + H2
a--------------->a
Fe + 2HCl --> FeCl2 + H2
b---------------->b
=> 136a + 127b = 39,9
=> a = 0,2 ; b = 0,1
=> \(\left\{{}\begin{matrix}m_{Zn}=0,2.65=13\left(g\right)\\m_{Fe}=0,1.56=5,6\left(g\right)\end{matrix}\right.\)
Đúng 3 Bình luận (0)
 Gửi Hủy
Gửi Hủy 
- Nguyễn Hưng Danh
 Gửi Hủy
Gửi Hủy  Nguyễn Trần Thành Đạt
Nguyễn Trần Thành Đạt  13 tháng 1 2021 lúc 18:11
13 tháng 1 2021 lúc 18:11 nH2= 0,35(mol)
a) PTHH: Mg + 2 HCl -> MgCl2 + H2
x_________2x_______x______x(mol)
PTHH: Fe + 2 HCl -> FeCl2 + H2
y________2y________y_____y(mol)
Ta có hpt: \(\left\{{}\begin{matrix}24x+56y=13,2\\x+y=0,35\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,15\end{matrix}\right.\)
b) m=m(muối khan)= mMgCl2 + mFeCl2= 95.x+127y=95.0,2+127.0,15= 38,05(g)
Đúng 1 Bình luận (0) Gửi Hủy
Gửi Hủy  hnamyuh
hnamyuh  13 tháng 1 2021 lúc 18:16
13 tháng 1 2021 lúc 18:16 a)
Gọi
\(n_{Fe} = a(mol) ; n_{Mg} = b(mol)\\ \Rightarrow 56a + 24b = 13,2(1)\)
\(Mg + 2HCl \to MgCl_2 + H_2\\ Fe + 2HCl \to FeCl_2 + H_2\)
Theo PTHH : \(n_{H_2} = a + b = 0,35(mol)\)(2)
Từ (1)(2) suy ra a = 0,15 ;b = 0,2
Vậy :
\(\%m_{Fe} = \dfrac{0,15.56}{13,2}.100\% = 63,64\%\\ \Rightarrow m_{Mg} = 100\% - 63,64\% = 36,36\%\)
b)
Ta có :\(n_{HCl} = 2n_{H_2} = 0,7(mol)\)
Bảo toàn khối lượng :
\(m_{muối} = m_{kim\ loại} + m_{HCl} - m_{H_2} = 13,2 + 0,7.36,5 - 0,35.2=38,05(gam)\)
Đúng 1 Bình luận (0) Gửi Hủy
Gửi Hủy Từ khóa » Cho 29.8 Gam Hỗn Hợp Gồm Zn Và Fe
-
Cho 29,8 Gam Hỗn Hợp Bột Gồm Zn Và Fe Vào 600 Ml Dung Dịch ...
-
Cho 29,8 Gam Hỗn Hợp Bột Gồm Zn Và Fe Vào 600 Ml ...
-
Cho 298 Gam Hỗn Hợp Gồm Zn Và Fe Vào 600ml Dung Dịch CuSO4 ...
-
Cho 29,8 Gam Hỗn Hợp Bột Gồm Zn Và Fe Vào 600 Ml D...
-
Cho 29,8 Gam Hỗn Hợp Bột Gồm Zn Và Fe Vào ...
-
Cho 29,8 Gam Hỗn Hợp Bột Gồm Zn Và Fe Vào 600ml Dung Dịch 0,5M ...
-
Cho 29,8g Hỗn Hợp Bột Gồm Zn Và Fe Vào 600ml Dung Dịch CuSO40 ...
-
2. Cho 29,8 G Hỗn Hợp Gồm Fe Zn Tác Dụng Hết Với 600 Ml Dung Dịch ...
-
Cho 29,8 Gam Hỗn Hợp Gồm Zn Và Fe Tác Dụng Hết Với 600ml Dung ...
-
Cho 29,8 Hỗn Hợp Gồm Fe, Zn Tác Dụng Hết Với 600ml Dung Dịch HCl ...
-
Cho 29,8 Gam Hỗn Hợp Bột Gồm Zn Và Fe Vào 600 Ml Dung ...
-
Cho 29,8 G Hỗn Hợp Bột Gồm Zn Và Fe Vào 600 Ml Dung Dịch Cuso4 0 ...
-
Cho 29,8 Gam Hỗn Hợp Bột Gồm Zn Và Fe Vào 600 ...
-
Cho 29,8 Gam Hỗn Hợp Gồm Fe, Zn Tác Dụng Hết Với 600 Ml Dung ...