Chọn Phát Biểu đúng Trong Các Phát Biểu Dưới ... - Trắc Nghiệm Online
Có thể bạn quan tâm
- TIỂU HỌC
- THCS
- THPT
- ĐẠI HỌC
- HƯỚNG NGHIỆP
- FLASHCARD
- TÀI LIỆU THAM KHẢO
- Trang chủ
- Đại học
- 800+ câu trắc nghiệm môn Hóa học đại cương có lời giải cụ thể
Chọn phát biểu đúng trong các phát biểu dưới đây:
A.Hợp chất có chứa F, O, N thì luôn luôn cho liên kết hydro
B.Hợp chất tạo được liên kết hydro với nước thì luôn luôn hòa tan trong nước theo bất kỳ tỉ lệ nào
C.Liên kết hydro liên phân tử làm tăng nhiệt độ sôi của hợp chất
D.Liên kết hydro chỉ có khi hợp chất ở thể rắn
Trả lời:Đáp án đúng: C
Phát biểu đúng là: "Liên kết hydro liên phân tử làm tăng nhiệt độ sôi của hợp chất".
- Giải thích:
- Liên kết hydro là một loại tương tác lưỡng cực-lưỡng cực đặc biệt mạnh xảy ra giữa một nguyên tử hydro liên kết với một nguyên tử có độ âm điện cao (như F, O, N) và một cặp electron đơn độc trên một nguyên tử có độ âm điện cao khác.
- Liên kết hydro liên phân tử (giữa các phân tử) làm tăng lực hút giữa các phân tử, do đó cần nhiều năng lượng hơn (nhiệt độ cao hơn) để phá vỡ các liên kết này và chuyển chất lỏng thành khí.
- Các phát biểu khác không đúng vì:
- Không phải hợp chất nào chứa F, O, N cũng tạo liên kết hydro. Hydro phải liên kết trực tiếp với F, O, hoặc N.
- Hợp chất tạo liên kết hydro với nước có thể tan trong nước, nhưng độ tan còn phụ thuộc vào nhiều yếu tố khác như kích thước phân tử, các nhóm chức khác, v.v. Không phải lúc nào cũng tan vô hạn.
- Liên kết hydro có thể tồn tại ở cả ba trạng thái: rắn, lỏng và khí.
800+ câu trắc nghiệm môn Hóa học đại cương có lời giải cụ thể - Phần 5
Sưu tầm và chia sẻ hơn 850 câu trắc nghiệm môn Hóa học đại cương (kèm đáp án) dành cho các bạn sinh viên, sẽ giúp bạn hệ thống kiến thức chuẩn bị cho kì thi sắp diễn ra. Mời các bạn tham khảo!
50 câu hỏi 60 phút Bắt đầu thiCâu hỏi liên quan
Câu 14:Ở trạng thái tinh thể, hợp chất Na2SO4 có những loại liên kết nào:
A.Liên kết ion và liên kết cộng hóa trị
B.Liên kết cộng hóa trị, liên kết ion và liên kết hydro
C.Liên kết cộng hóa trị, liên kết ion và liên kết Van Der Waals
D.Liên kết ion
Lời giải:Đáp án đúng: ANa2SO4 là một hợp chất ion được tạo thành từ cation Na+ và anion SO42-. Liên kết giữa Na+ và SO42- là liên kết ion. Trong ion SO42-, các nguyên tử S và O liên kết với nhau bằng liên kết cộng hóa trị.
Câu 15:Chọn phát biếu đúng: Các muối vô cơ ở trạng thái rắn có các đặc điểm: 1) Đều dễ tan trong các dung môi phân cực. 2) Không có khả năng thăng hoa. 3) Dễ dàng điện ly trong nước.
A.1, 2 đúng
B.2, 3 đúng
C.1, 2, 3 đúng
D.Tất cả đều chưa chính xác
Lời giải:Đáp án đúng: DPhát biểu 1 sai, vì không phải muối vô cơ nào ở trạng thái rắn cũng dễ tan trong dung môi phân cực, ví dụ như BaSO4 rất ít tan. Phát biểu 2 đúng, muối vô cơ ở trạng thái rắn không có khả năng thăng hoa. Phát biểu 3 đúng, muối vô cơ dễ dàng điện ly trong nước. Vậy chỉ có 2 và 3 đúng.Câu 16:Chọn phương án đúng: Xét hệ phản ứng NO(k) + 1/2O2(k) ® NO2(k) \(\Delta H_{298}^0\) = -7,4 kcal. Phản ứng được thực hiện trong bình kín có thể tích không đổi, sau phản ứng được đưa về nhiệt độ ban đầu. Hệ như thế là:
A.Hệ cô lập
B.Hệ kín và đồng thể
C.Hệ kín và dị thể
D.Hệ cô lập và đồng thể
Lời giải:Đáp án đúng: BPhản ứng được thực hiện trong bình kín (không trao đổi chất với môi trường) và sau phản ứng được đưa về nhiệt độ ban đầu (không trao đổi nhiệt với môi trường). Do đó, hệ là hệ cô lập. Vì các chất phản ứng và sản phẩm đều ở trạng thái khí, hệ là hệ đồng thể.
Câu 17:Chọn phương án đúng: Tính hiệu ứng nhiệt DH0 của phản ứng: B ® A, biết hiệu ứng nhiệt của các phản ứng sau: C ® A: DH1 ; D ® C: DH2 ; D ® B DH3.
A.DH0 = DH3 + DH2 - DH1
B.DH0 = DH1 + DH2 + DH3
C.DH0 = DH1 + DH2 - DH3
D.DH0 = DH1 - DH2 - DH3
Lời giải:Đáp án đúng: CĐể tính hiệu ứng nhiệt của phản ứng B → A, ta cần sử dụng định luật Hess. Định luật Hess nói rằng hiệu ứng nhiệt của một phản ứng chỉ phụ thuộc vào trạng thái đầu và trạng thái cuối, không phụ thuộc vào con đường phản ứng. Ta có các phản ứng sau:1. C → A: ΔH₁2. D → C: ΔH₂3. D → B: ΔH₃Chúng ta muốn tìm ΔH₀ cho phản ứng B → A.Ta có thể biểu diễn phản ứng B → A như sau:D → B (ΔH₃)D → C (ΔH₂)C → A (ΔH₁)Để có được phản ứng B → A, ta cần đảo ngược phản ứng D → B thành B → D với hiệu ứng nhiệt là -ΔH₃. Sau đó, ta có thể viết:B → D: -ΔH₃D → C: ΔH₂C → A: ΔH₁Cộng các phản ứng này lại, ta được:B → D + D → C + C → A = B → AVậy, ΔH₀ = -ΔH₃ + ΔH₂ + ΔH₁ = ΔH₁ + ΔH₂ - ΔH₃.Câu 18:Cho phản ứng: 2SO2(k) + O2(k) ⇌ 2SO3(k) ; DH < 0. Để được nhiều SO3 hơn, ta nên chọn biện pháp nào trong 3 biện pháp sau: (1) Giảm nhiệt độ. (2) Tăng áp suất. (3) Thêm O2.
A.Chỉ có biện pháp 1
B.Chỉ có 2
C.Chỉ có 2 và 3
D.Cả 3 biện pháp
Lời giải:Đáp án đúng: DPhản ứng 2SO2(k) + O2(k) ⇌ 2SO3(k) ; DH < 0 là phản ứng tỏa nhiệt và có số mol khí giảm khi phản ứng xảy ra theo chiều thuận. (1) Giảm nhiệt độ: Vì phản ứng tỏa nhiệt (ΔH < 0), giảm nhiệt độ sẽ làm cân bằng chuyển dịch theo chiều thuận, tức là chiều tạo ra SO3, làm tăng lượng SO3.(2) Tăng áp suất: Phản ứng có số mol khí giảm từ 3 xuống 2 khi đi từ trái sang phải. Do đó, tăng áp suất sẽ làm cân bằng chuyển dịch theo chiều làm giảm số mol khí, tức là chiều thuận, làm tăng lượng SO3.(3) Thêm O2: Thêm O2 là tăng nồng độ của O2, làm cân bằng chuyển dịch theo chiều làm giảm nồng độ O2, tức là chiều thuận, làm tăng lượng SO3.Vậy cả 3 biện pháp đều làm tăng lượng SO3.Câu 19:Khi hòa tan trong hexan, acid stearic xảy ra phản ứng chuyển hóa như sau: 2C17H35COOH (dd) ⇌ (C17H35COOH)2 (dd). Tại 28oC phản ứng có Kc = 2900 và tại 48oC có Kc = 40. Tính ∆Ho và ∆So của phản ứng.
A.∆Ho = -2,39 kJ và ∆So = -537,32 J
B.∆Ho = -172,05 kJ và ∆So = -505,32 J
C.∆Ho = -86,32 kJ và ∆So = -249,14 J
D.∆Ho = -55,07 kJ và ∆So = -80,31 J
Lời giải: Bạn cần đăng ký gói VIP để làm bài, xem đáp án và lời giải chi tiết không giới hạn. Nâng cấp VIP Câu 20:Dung dịch của NaCl trong nước nằm cân bằng với NaCl rắn ở áp suất không đổi (P = const). Số cấu tử và bậc tự do của hệ lần lượt là:
A.2 và 1
B.2 và 0
C.3 và 2
D.2 và 2
Lời giải: Bạn cần đăng ký gói VIP để làm bài, xem đáp án và lời giải chi tiết không giới hạn. Nâng cấp VIP Câu 21:Số cấu tử của hệ phản ứng: BaSO4(r) = BaO(r) + SO2(k) + O2(k) là:
A.1
B.2
C.3
D.4
Lời giải: Bạn cần đăng ký gói VIP để làm bài, xem đáp án và lời giải chi tiết không giới hạn. Nâng cấp VIP Câu 22:Chọn phát biểu đúng về tính chất của điểm ơtecti (điểm E) trong giản đồ nóng chảy hệ hai kim loại A – B.
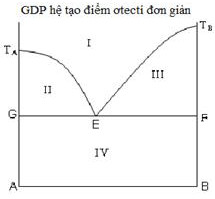
1) Hệ tại E, tùy theo cách điều chỉnh nhiệt độ ta có thể thu được A tinh khiết hoặc B tinh khiết.
2) Hệ tại E có bậc tự do bằng 0 (hệ vô biến).
3) Quá trình tại E xảy ra ở nhiệt độ không đổi vì lượng nhiệt phát ra khi kết tinh đã bù trừ cho lượng nhiệt của hệ mất đi khi làm lạnh.
4) Nhiệt độ tại E có giá trị cao nhất trong các nhiệt độ bắt đầu kết tinh của các hỗn hợp A – B khác nhau.
A.1, 2
B.2, 3
C.3, 4
D.1, 4
Lời giải: Bạn cần đăng ký gói VIP để làm bài, xem đáp án và lời giải chi tiết không giới hạn. Nâng cấp VIP Câu 23:Chọn phát biểu đúng: Chất xúc tác có ảnh hưởng như thế nào đến trạng thái cân bằng của phản ứng tỏa nhiệt?
A.Làm tăng năng lượng của các tiểu phân
B.Làm cho phản ứng nhanh đạt tới cân bằng
C.Làm cho phản ứng xảy ra hoàn toàn
D.Làm tăng hiệu suất của phản ứng theo chiều thuận
Lời giải: Bạn cần đăng ký gói VIP để làm bài, xem đáp án và lời giải chi tiết không giới hạn. Nâng cấp VIP
Bộ Đồ Án Tốt Nghiệp Ngành Trí Tuệ Nhân Tạo Và Học Máy
89 tài liệu310 lượt tải
Bộ 120+ Đồ Án Tốt Nghiệp Ngành Hệ Thống Thông Tin
125 tài liệu441 lượt tải
Bộ Đồ Án Tốt Nghiệp Ngành Mạng Máy Tính Và Truyền Thông
104 tài liệu687 lượt tải
Bộ Luận Văn Tốt Nghiệp Ngành Kiểm Toán
103 tài liệu589 lượt tải
Bộ 370+ Luận Văn Tốt Nghiệp Ngành Kế Toán Doanh Nghiệp
377 tài liệu1030 lượt tải
Bộ Luận Văn Tốt Nghiệp Ngành Quản Trị Thương Hiệu
99 tài liệu1062 lượt tảiĐĂNG KÝ GÓI THI VIP
- Truy cập hơn 100K đề thi thử và chính thức các năm
- 2M câu hỏi theo các mức độ: Nhận biết – Thông hiểu – Vận dụng
- Học nhanh với 10K Flashcard Tiếng Anh theo bộ sách và chủ đề
- Đầy đủ: Mầm non – Phổ thông (K12) – Đại học – Người đi làm
- Tải toàn bộ tài liệu trên TaiLieu.VN
- Loại bỏ quảng cáo để tăng khả năng tập trung ôn luyện
- Tặng 15 ngày khi đăng ký gói 3 tháng, 30 ngày với gói 6 tháng và 60 ngày với gói 12 tháng.
Từ khóa » Chọn Phát Biểu đúng Trong Các Phát Biểu Dưới đây
-
Chọn Phát Biểu đúng Trong Các Phát Biểu Dưới đây:
-
Chọn Phát Biểu đúng Trong Các Phát Biểu Dưới đây:
-
Chọn Phát Biểu đúng Trong Các Phát Biểu Dưới đây:A. Ngoài B
-
Chọn Phát Biểu đúng Trong Các Phát Biểu Dưới đây
-
Chọn Phát Biểu đúng Trong Các Phát Biểu Dưới đây:
-
Chọn Phát Biểu đúng Trong Các Phát Biểu Dưới đây?
-
Chọn Phát Biểu đúng Trong Các Phát Biểu Dưới đây? - Vietjack.online
-
Chọn Phát Biểu đúng Trong Các Phát Biểu Sau:...
-
Chọn Phát Biểu đúng Trong Các Phát Biểu Dưới đây?
-
Chọn Phát Biểu đúng Trong Các Phát Biểu Dưới đây? - Tự Học 365
-
Hãy Chọn Phát Biểu đúng Trong Các Phát Biểu Dưới đây - Haylamdo
-
Chọn Phát Biểu đúng Trong Các Phát Biểu Dưới đây? - Luyện Tập 247
-
Chọn Phát Biểu đúng Về Sóng Cơ Trong Các Phát Biểu Dưới đây
-
Chọn Phát Biểu đúng Trong Các Phát Biểu Dưới đây