Công Thức Tính Nồng độ Mol Và Nồng độ Phần Trăm
Có thể bạn quan tâm
Đây là tài liệu Cao cấp - Chỉ dành cho Thành viên VnDoc ProPlus.
- Tải tất cả tài liệu lớp 8 (Trừ Giáo án, bài giảng)
- Trắc nghiệm không giới hạn
Bài tập tính nồng độ mol và nồng độ phần trăm
- I. Nồng độ phần trăm (C%)
- II. Nồng độ mol (CM )
- Thực hành tính Nồng độ Mol
Công thức tính nồng độ mol và nồng độ phần trăm là kiến thức cơ bản và quan trọng trong môn Hóa học, giúp xác định lượng chất tan trong dung dịch. Nắm vững các công thức này sẽ hỗ trợ học sinh giải nhanh các bài tập liên quan đến dung dịch một cách chính xác và hiệu quả.
- Tổng hợp công thức Hóa học 8 cần nhớ
- Các bài tập về lượng chất dư Hóa học 8
- Bài tập ôn hè môn Hóa học lớp 8 lên lớp 9
Thực hành tính Nồng độ Mol
Cách thực hiện:
- Chọn Lượng chất tan
- Chọn Thể tích dung dịch
Lưu ý: Bạn có thể chọn Chất tan ở ô Drink mix
I. Nồng độ phần trăm (C%)
Nồng độ phần trăm của dung dịch là số gam chất tan có trong 100 gam dung dịch
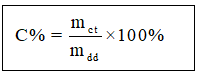
Trong đó:
mct là khối lượng chất tan
mdd là khối lượng dung dịch
mdd = mdm + mct
Ví dụ 1: Hòa tan 15 gam muối vào 50 gam nước. Tính nồng độ phần trăm của dung dịch thu được:
Hướng dẫn giải chi tiết bài tập
Ta có: mdd = mdm + mct = 50 + 15 = 65 gam
Áp dụng công thức:
![]()
![]()
Ví dụ 2: Người ta hòa tan 40 gam muối và nước được dung dịch có nồng độ 20%.
a) Tính khối lượng dung dịch nước muối thu được.
b) Tính khối lượng nước cần dùng cho sự pha chế trên.
Hướng dẫn giải chi tiết bài tập
a) Khối lượng dung dịch nước muối thu được là:
![]()
c) khối lượng nước cần dùng cho sự pha chế trên là:
mdd - mct = 200 - 40 = 160 gam
Ví dụ 3: Trộn 50 gam dung dịch muối ăn có nồng độ 20% với 50 gam dung dịch muối ăn 10%. Tính nồng độ phần trăm của dung dịch thu được?
Hướng dẫn giải chi tiết bài tập
Số gam muối ăn có trong 50 gam dung dịch muối ăn nồng độ 20% là:
![]()
Số gam muối ăn có trong 50 gam dung dịch muối ăn nồng độ 10% là:
![]()
Dung dịch muối ăn thu được sau phản ứng là: mdd1 + mdd2 = 50 + 50 = 100 gam
Nồng độ % dung dịch muối ăn sau khi trộn là:

Ví dụ 4. Hòa tan 25 gam đường vào nước được dung dịch nồng độ 50%
Hãy tính:
a) Khối lượng dung dịch đường pha chế được.
b) Khối lượng nước cần dùng cho sự pha chế.
Hướng dẫn giải chi tiết bài tập
Từ công thức m dd = (mct.100%)/C%
a. Khối lượng dung dịch đường pha chế được
mdd = (25.100)/50 = 50 (gam)
b. Khối lượng nước cần dùng cho sự pha chế:
m dm = mdd - m đường = 50 -25 = 25 (gam)
Ví dụ 5. Hòa tan CaCO3 vào 200 gam dung dịch HCl 7,3% (vừa đủ)
a. Viết phương trình hóa học
b. Tính nồng độ phần trăm của các chất có trong dung dịch sau phản ứng.
Hướng dẫn giải chi tiết bài tập
Khối lượng của HCl có trong 200 gam dung dịch HCl 7,3% là
mHCl = (C%.mdd)/100% = 200.7,3/100 = 14,6 (gam) => nHCl = 0,4 mol
Phương trình: CaCO3 + 2HCl → CaCl2 + H2O + CO2
nCaCO3 = nCaCl2 = nCO2 = 1/2nHCl = 0,2 mol -> mCaCO3 = 20 gam
mCaCl2 = 0,2.111 = 22,2 gam
mCO2= 0,2.44 = 8,8 gam
Khối lượng dung dịch sau phản ứng là:
m dd sau phản ứng = mCaCO3 + mdd HCl - mCO2 = 20 + 200 - 8,8 = 211,2 gam
Nồng độ của CaCl2 là: C% dd CaCl2 = (22,3.100%)/(211.2) = 10,51%
Ví dụ 6. Tiến hành thí nghiệmcho 400 gam dung dịch NaOH 20% tác dụng vừa đủ với 200 gam dung dịch HCl, phản ứng sinh ra NaCl và H2O. Tính nồng độ muối sinh ra sau phản ứng.
Hướng dẫn giải chi tiết bài tập
Khối lượng NaOH là:
mNaOH = mdd.C%/100 = 400.20/100 = 80 gam
=> Số mol NaOH là: nNaOH = 80/40 = 3 mol
Phương trình hóa học phản ứng: NaOH + HCl → NaCl + H2O
Theo phương trình hóa học: 1mol → 1mol → 1mol
Muối thu được sau phản ứng là NaCl
mNaCl = 2.58,5 = 117 gam
Do phản ứng không sinh ra chất khí hay kết tủa nên khối lượng dung dịch sau phản ứng là:
mdd sau pứ = mdd NaOH + mdd HCl = 400 + 200 = 600 (gam)
=> Nồng độ dd NaCl sau phản ứng là: C%ddNaCl = 117/600.100% = 19,5 %
II. Nồng độ mol (CM )
Nồng độ mol của dung dịch cho biết số mol chất tan có trong 1 lít dung dịch
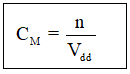
Trong đó: CM là nồng độ mol
n là số mol chất tan
Vdd là thể tích dung dịch (lít)
Ví dụ 1: Tính nồng độ mol của dung dịch khi 0,5 lit dung dịch CuSO4 chứa 100 gam CuSO4
Hướng dẫn giải chi tiết bài tập
Số mol của CuSO4 = 100 : 160 = 0,625 mol
Nồng độ mol của dung dịch CuSO4 = 0,625 : 0,5 = 1,25M
Ví dụ 2: Tính khối lượng H2SO4 có trong 100 ml dung dịch H2SO4 2M
Hướng dẫn giải chi tiết bài tập
Số mol của H2SO4 là = 0,1 x 2 = 0,2 mol
Khối lượng của H2SO4 = 0,2 x 98 = 19,6 gam
Ví dụ 3: Trộn 200 ml dung dịch H2SO4 4M vào 4 lít dung dịch H2SO4 0,25M. Nồng độ mol của dung dịch mới là
Hướng dẫn giải chi tiết bài tập
Số mol H2SO4 2 lít dung dịch H2SO4 4M là
0,2 : 4 = 0,8 mol
Số mol H2SO4 4 lít dung dịch H2SO4 0,25M là
4 : 0,25 = 1 mol
Thể tích sau khi trộn dung dịch là: 4 + 0,2 = 4,2 lít
Nồng độ mol của dung dịch mới là: ( 0,8 + 1) : 4,2 = 0,43M
Ví dụ 4. Cho 6,5 gam kẽm phản ứng vừa đủ với 100 mol dung dịch axit HCl
a. Tính thể tích H2 thu được ở điều kiện tiêu chuẩn
b. Tính nồng độ mol của dung dịch HCl đã dùng.
Hướng dẫn giải chi tiết bài tập
Số mol của Zn là: nZn = 6,5/65 = 0,1 mol
Phương trình hóa học: Zn + 2HCl → ZnCl2 + H2
nZn = nZnCl2 = 0,1 mol, nHCl = 2.nZn = 0,2 mol
a. VH2 = 0,1 . 22,4 = 2,24 (lít)
b. CM (dd HCl) = 0,2/0,1 = 2M
III. Bài tập vận dụng liên quan
Câu 1: Trộn lẫn 100 gam dung dịch H2SO4 10% với 200 gam dung dịch H2SO4 C% thu được dung dịch H2SO4 30%. Tính C%.
Hướng dẫn giải chi tiết bài tập
mddH2SO4.24,5% = 200 .1,12 = 224 (g)
⇒ mH2SO4.24,5% = 224 . 24,5% = 54,88 (g)
mH2SO4.10% = 26×10% = 2,6(g)
Ta có: mddH2SO4mới = 224 + 26 = 250(g)
mH2SO4mới = 54,88 + 2,6 = 57,48(g)
⇒C%H2SO4mới = 57,48/250×100% = 22,992%
Câu 2: Cho D = m/v. Lập công thức thể hiện mối quan hệ giữa C% và CM.
Hướng dẫn giải chi tiết bài tập
Ta có: Lấy V lít hay 1000V ml dung dịch
=> Khối lượng dung dịch là: mdd = 100V. D
Khối lượng chất tan là: ![]()
Số mol của chất tan là: ![]()
Ta có:

Câu 3: Trong Cho m gam NaCl vào nước được 200 gam dung dịch NaCl 15%. Tính nồng độ mol của dung dich NaCl. Biết dung dich NaCl có D= 1,1g/ml.
Hướng dẫn giải chi tiết bài tập
m NaCl = 200. 15/100= 30g
=> n NaCl = 0,5 mol
Vdd NaCl = mdd / D = 200/ 1,1 = 181,8 ml = 0,182 l
=> Nồng độ mol = 0,5/ 0,182 = 2,75 (M)
Câu 4: Trộn 2 lít dung dịch đường 0,5M với 3 lit dung dịch đường 1M. Tính nồng độ mol của dung dịch đường sau khi trộn?
Hướng dẫn giải chi tiết bài tập
Tính số mol đường có trong dung dịch 1:
n1 = CM 1.Vdd 1 = 0,5.2 = 1 mol
Tính số mol đường có trong dung dịch 2:
n2 = CM 2.Vdd 2 = 1.3=3 mol
Tính số mol đường có trong dung dịch 3:
n3 = n1 + n2 = 1+3 = 4 mol
Tính thể tích dung dịch 3
Vdd 3 = Vdd 1 + Vdd 2 = 2 + 3 = 5 lit
Tính nồng độ mol dung dịch 3
CM = n : V = 4: 5 = 0,8 M
Câu 5: Tính nồng độ mol của dung dịch
a. 1 mol KCl trong 750ml dung dịch
b. 0,5 mol MgCl2 trong 1,5 lít dung dịch
c. 0,06 mol trong 1500 ml dung dịch
Hướng dẫn giải chi tiết bài tập
Đổi 750 ml = 0,75 lít
CM = 1/0,75 = 1,33 mol/l
b. CM = 0,5/1,5 = 0,33 mol/l
c. Đổi 1500 ml = 1,5 lít
CM = 0,06/1,5 = 0,04 mol/l
Câu 6: Tính nồng độ phần trăm của các dung dịch sau
a. 20 gam KCl trong 600 gam dung dịch
b. 32 gam KNO3 trong 2 Kg dung dịch
c. 75 g K2CO3 trong 1500 gam dung dịch
Hướng dẫn giải chi tiết bài tập
a) C%KCl = mct/mdd.100 = 20/600.100 = 10/3 ≈ 3,33%
b) Đổi: 2kg = 2000 g
C%NaNO3 = 32/2000.100 = 1,6%
c)C%K2SO4 = 75/1500.100 = 5%
Câu 7: Đun nhẹ 20 gam dung dịch CuSO4 cho đến khi nước bay hơi hết thu được 3,6 gam chất rắn. Xác định nồng độ phần trăm của dung dịch CuSO4.
Hướng dẫn giải chi tiết bài tập
CuSO4 khan là chất tan.
Nồng độ phần trăm của dung dịch CuSO4 là:
C% = 3,6/20.100 = 18%
Vậy: Nồng độ phần trăm của dung dịch CuSO4 trên là 18%
Câu 8: Trung hòa 30ml dung dịch H2SO4 1m cần dung 50 ml dung dịch NaOH:
a) Viết phương trình hóa học
b) Tính nồng độ dung dịch NaOH đã dùng
c) Nếu trung hòa dung dịch H2SO4 ở trên bằng dung dịch KOH 5,6% có khối lượng riêng 1,045g/ml thì cần bao nhiêu ml KOH
Hướng dẫn giải chi tiết bài tập
Phương trình hóa học
a) 2NaOH + H2SO4 → Na2SO4 + 2H2O
b)
nH2SO4 = 0,03.1 = 0,03 (mol)
nNaOH = 2nH2SO4 = 0,06 (mol)
=> CMNaOH = 0,06/0,05 = 1,2M
c) H2SO4 + 2KOH → K2SO4 + 2H2O
nKOH = 2nH2SO4 = 0,06 (mol)
=> mKOH = 0,06.56 = 3,36 gam
=> mddKOH = 3,36/5,6% = 60 (gam)
=> V dung dịch KOH = m/D = 60/1,045 = 57,42 (ml)
Câu 9: Cho bao nhiêu gam NaOH vào bao nhiêu gam nước có trong 200 gam dung dịch NaOH 10%.
Hướng dẫn giải chi tiết bài tập
Khối lượng NaOH là:
mNaOH = 10.200/100 = 20 (g)
Khối lượng nước cần dùng là:
mH2O = mdd − mNaOH = 200 − 20 = 180 (g)
Câu 10: Tính
a. Khối lượng nước có trong 400 gam dung dịch CuSO4 4%
b. Khối lượng NaCl có trong 300ml dung dịch NaCl 3M
Hướng dẫn giải chi tiết bài tập
a) nCuSO4 = 400.4/100 = 16 gam
mH2O = 400 - 16 = 384 g.
b)
Vì đơn vị của nồng độ mol là mol/l nên ta đổi 300 ml thành 0,3 lít
Số mol chất tan trong 0,3 lít dung dịch NaCl 3M là
CM = nV => n = CM.V = 3.0,3 = 0,9mol
Khối lượng NaCl cần lấy là: mNaCl = n.M = 0,9.58,5 = 52,65 gam
Chi tiết bộ câu hỏi nằm trong FILE TẢI VỀ
................................................
Từ khóa » Tính Nồng độ Mol Của Dung Dịch Hcl
-
Công Thức Tính Nồng độ Mol - Luật Hoàng Phi
-
Tính Nồng độ Mol Của Dd HCl đã Dùng - Lê Tấn Vũ
-
Tính Nồng độ Mol/l Của Dd HCl đã Dùng - Mai Rừng - HOC247
-
Tính Nồng độ Mol CM Của Dung Dịch HCl đã Dùng - Hóa Học Lớp 9
-
Công Thức Tính Nồng độ Phần Trăm, Ví Dụ Minh Họa - VietChem
-
Tính Nồng độ Mol Của Dung Dịch HCl, Biết Dung Dịch ...
-
[LỜI GIẢI] Tính Nồng độ Mol Của Dung Dịch HCl đã Dùng? - Tự Học 365
-
Tính Nồng độ Mol Của Dung Dịch HCl, Nếu 30,0 Ml Dung Dịch Này ...
-
D. Tính Nồng độ Mol Của Dung Dịch HCl đã Dùng? Bài 3 (1,0 điểm ...
-
Tính Nồng độ Mol Của Dung Dịch HCl, Nếu 30,0 Ml Dung ... - Haylamdo
-
Bài Tập 1.34 Trang 8 SBT Hóa 11: Tính Nồng độ Mol Của Dung Dịch HCl
-
Tính Nồng độ Mol Của Dung Dịch HCl, Nế... - CungHocVui
-
Để Tính Nồng độ Mol Của Dung Dịch HCl Người Ta Làm Thế Nào