[ Công Thức Tính Số Mol ] Qua Khối Lượng, Qua Thể Tích, Qua ...

Công thức tính số mol là phần kiến thức thường sử dụng trong hầu hết những bài toán tính trong hóa học. Thế nhưng nó có rất nhiều kiểu tính khác nhau
Mỗi bài, mỗi kiểu dữ kiện sẽ là những kiểu tính khác nhau đòi hỏi học sinh cần nắm bắt toàn bộ các công thức đó để vận dụng và làm bài tập hóa của mình.
Đơn giản thôi, hãy theo dõi bài viết dưới đây của chúng tôi, Đồng Hành Cho Cuộc Sống Tốt Đẹp đã tổng hợp lại những câu thức đó rồi đây. Hãy cùng theo dõi nhé !
Tham khảo thêm nội dung bài viết khác:
- Polivinyl Axetat là gì ?
- Polivinyl clorua là gì ?
Cách công thức tính số mol trong Hóa Học lớp 8, lớp 9
Tóm tắt nội dung
- 1 Cách công thức tính số mol trong Hóa Học lớp 8, lớp 9
- 1.1 1. Cách tính số mol theo khối lượng
- 1.2 Cách tính số mol điều kiện tiêu chuẩn (đktc) của chất khí
- 1.3 3. Công thức tính số mol nguyên tử
- 1.4 4. Công thức tính mol ở điều kiện thường
- 1.5 5. Một số công thức tính mol khác
- 1.6
- 2 Một số ví dụ minh họa
1. Cách tính số mol theo khối lượng
n = m/M
– Trong đó:
- n là số mol chất ( mo l)
- M là khối lượng mol (g/mol )
Cách tính số mol điều kiện tiêu chuẩn (đktc) của chất khí
– Thể tích mol của các chất khí ở cùng điều kiện nhiệt độ và áp suất là bằng nhau
– 1mol chất khí có thể tích 22,4 lít ở 0 độ C, 1atm tức là VH2 = VO2 = VSO2 = VN2 = 22,4 lít.
– 1 mol chất khí có thể tích 24 lít ở điều kiện phòng là 20 độ C, 1 atm.
Công thức tính số mol chất khí (đktc)
n = V/22,4
– Trong đó
- n là số mol chất khí (mol).
- V là thể tích chất khí ở điều kiện tiêu chuẩn (lít).
- 22,4 là hằng số trong điều kiện tiêu chuẩn.
Lưu ý: Trong trường hợp điều kiện thường bạn không thể áp dụng kiểu thông thức này mà cần tính toán những phép tính phức tạp hơn
3. Công thức tính số mol nguyên tử
Công thức tính số mol theo hằng số số Avogadro = 6,022.1023 là:
n = A/N
– Trong đó:
- n là số mol chất khí ở điều kiện thường, đơn vị tính là mol
- A là số nguyên tử hoặc phân tử
- N là số Avogadro = 6,022.1023
4. Công thức tính mol ở điều kiện thường
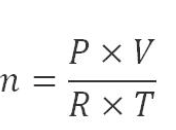
– Trong đó:
- n là số mol chất khí ở điều kiện thường (mol)
- P là áp suất (atm)
- V là thể tích khí (lit)
- R là hằng số = 0.082
- T là nhiệt độ K, với T = 273 + t (K)
– Tuy nhiên, rất hiếm khi đề bài cho dạng tính số mol ở điều kiện bình thường. Nếu gặp dạng bài này thì bạn nên biết được các giá trị là P (áp suất), hằng số R (0.082) và đổi về nhiệt độ K.
5. Một số công thức tính mol khác
Một số ví dụ minh họa
Bài tập minh họa 1: Tính khối lượng của 0.75 mol khí SO2, biết khối lượng mol của SO2 là 64 g/mol.
– Hướng dẫn giải:
Khối lượng của SO2 là: mSO2 = nSO2 x MSO2 = 0.75 x 64 = 48 (g)
Bài tập minh họa 2: Hãy tính nồng độ mol của dung dịch khi tiến hành hòa tan 15,8g KMnO4 trong 7,2 lít nước.
– Hướng dẫn giải:
Số mol của chất nKMnO4 là:
nKMnO4 = 15,8/ 158 = 0,1 ( mol )
➔ CM = 0,1/ 7,2 = 0,0139
Bài tập minh họa 3: Cho 3,9 gam Kali vào dung dịch HCl dư. Tính thể tích khí hidro thu được ở điều kiện chuẩn.
– Hướng dẫn giải:
Phản ứng xảy ra theo 2 phương trình
2K + 2HCl → 2KCl + H2 ↑ (1)
2K + 2H2O → 2KOH + H2 ↑ (2)
Số mol Kali: nK = 3,9/39 = 0,1 mol
Theo phương trình phản ứng (1) và (2), nH2 = nK = 0,1 mol
Vậy thể tích khí hydro thu được ở điều kiện tiêu chuẩn là: VH2 = 0,1 x 22,4 = 2,24 lít.
Hy vọng với những kiến thức này sẽ đem đến cho bạn những thông tin hay và hữu ích nhé. Cám ơn bạn đã theo dõi bài viết của chúng tôi
Người xem: 1.213Từ khóa » Ct Số Mol
-
Công Thức Tính Nồng độ Mol, Số Mol Và C Nồng độ Phần Trăm
-
Công Thức Tính Số Mol
-
Cách Tính Số Mol: Công Thức Tính Và Bài Tập Minh Họa - LabVIETCHEM
-
Công Thức Tính Số Mol, Nồng độ Mol Của Dụng Dịch Chuẩn 100%
-
Công Thức Tính Số Mol. Công Thức Liên Hệ Giữa Nồng độ Mol Và ...
-
Công Thức Tính Số Mol, Nồng độ Mol Của Dung Dịch Chính Xác 100%
-
Công Thức Tính Số Mol, Bài Tập Mol - THPT Sóc Trăng
-
Cách Tính Số Mol, Nồng độ Mol, Nồng độ Phần Trăm
-
Công Thức Tính Số Mol Khí ở điều Kiện Không Chuẩn - CungHocVui
-
Nồng độ Mol Là Gì? Công Thức Tính Số Mol, Nồng độ Mol?
-
Công Thức Tính Nồng độ Mol, Số Mol Của Dung Dịch Chính Xác 100%
-
MOL Và Công Thức Tính Số (n) Mol, Khối Lượng (m) Mol, Thể Tích (V ...