Đại Cương Về UNG THƯ ỐNG HẬU MÔN|| Phần 1
Có thể bạn quan tâm
I – Định nghĩa:
Ung thư ống hậu môn là những khối u có tổn thương nguyên phát nằm trong ống hậu môn. Mặc dù, hiếm gặp và chỉ trên một đoạn ngắn của đường tiêu hóa nhưng ung thư ống hậu môn cũng bao gồm rất nhiều loại khác nhau do đặc điểm giải phẫu và cấu trúc mô học phức tạp của nó. Ung thư biểu mô vảy là loại tổn thương hay gặp nhất nhưng u hạt, u tế bào chuyển tiếp, u hắc tố… cũng có thể gặp đơn độc hoặc phối hợp với nhau [2].
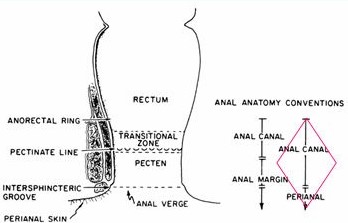
Nhắc lại về giải phẫu: Ống hậu môn là phần cuối cùng của ống tiêu hóa, dài khoảng 2.5 đến 5 cm từ trực tràng ngang mức cơ nâng hậu môn tới da rìa hậu môn. Ống hậu môn được bao bọc quanh bởi các cơ thắt trong và cơ thắt ngoài. Cơ thắt trong là phần kéo dài của bó cơ dọc vòng của trực tràng. Cơ mu trực tràng, có thể sờ thấy được, góp phần cùng phần trên cơ thắt ngoài hậu môn tạo nên vòng hậu môn trực tràng, mốc giải phẫu có giá trị rất quan trọng trong bảo vệ chức năng cơ thắt khi can thiệp phẫu thuật. Cơ thắt trong được bao bọc ở trên bởi cơ nâng hậu môn và ở dưới bởi bó nông của cơ thắt ngoài.
Hình 1: Giải phẫu ống hậu môn [Gordon PH, Nivatvongs S. Principles and practice of surgery for the colon, rectum and anus. 3rd edition. Informa Health-care; 2007]
Dẫn lưu bạch huyết tại vùng này tương đối phức tạp với đoạn cao được dẫn lưu về các hạch cạnh trực tràng dọc theo động mạch mạc treo tràng dưới; còn bạch huyết ở ngay cạnh đường lược được dẫn về hệ thống hạch chậu trong. Ngoài ra, bạch huyết tại đường lược và da rìa hậu môn trở về qua các hạch bẹn, đùi và chậu ngoài.
Mốc giải phẫu quan trọng nhất trong vùng này là đường lược với các hốc hậu môn được tạo thành bời các nếp niêm mạc. Đây là vị trí chuyển tiếp giữa biểu mô trụ đơn ở phía trên (giống như đại trực tràng) và biểu mô vảy ở tầng dưới (giống như da ở rìa hậu môn). Rìa hậu môn được tính từ vị trí xuất hiện da và theo phân loại của Tổ chức y tế thế giới thì u ở rìa hậu môn được phân vào loại u của da.
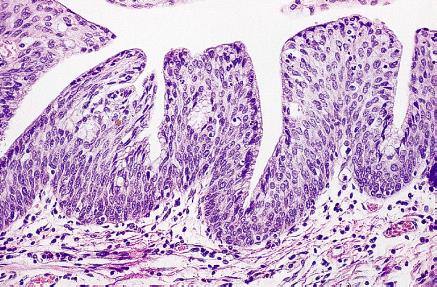
Hình 2: Biểu mô vẩy bình thường của ống hậu môn (không sừng hóa) và vùng chuyển tiếp A: biểu mô, B: mô đệm (mô liên kết )1: lớp tế bào đáy, 2: lớp tế bào vẩy
II – Đặc điểm lâm sàng
Ung thư ống hậu môn chiếm 1.5% ung thư đường tiêu hóa với tỷ lệ mắc tăng dần trong 30 năm nay với khoảng 4000 ca mắc mới và 620 trường hợp tử vong hàng năm tại Hoa Kỳ [16]. Bệnh lý có thể gặp ở cả hai giới nhưng nữ nhiều hơn nam (2 – 4:1) [20]
Các yếu tố nguy cơ thường gặp là virus HPV (Human Papillomavirus), quan hệ tình dục qua đường hậu môn, tiền sử bệnh lý lây nhiễm qua đường sinh dục, hút thuốc lá và suy giảm miễn dịch [17].
Hình thái tổn thương thường dưới dạng thâm nhiễm hoặc loét khu trú ở rìa hậu môn, ống hậu môn hoặc đôi khi ở phần thấp trực tràng.
Triệu chứng lâm sàng thường gặp là xuất huyết tiêu hóa thấp, ngứa hoặc đau vùng tầng sinh môn, tự sờ thấy khối nhưng không đặc hiệu và có tới 25% bệnh nhân được chẩn đoán tình cờ mà không có triệu chứng trực tiếp nào [20]. Phần lớn bệnh nhân được chẩn đoán ở giai đoạn tiến triển do bệnh nhân đến muộn hoặc không được thăm khám hậu môn trực tràng bởi các bác sỹ chuyên khoa được đào tạo căn bản. Trên thực tế, mặc dù chẩn đoán xác định phải dựa vào giải phẫu bệnh nhưng động tác thăm khám hậu môn trực tràng đơn giản hay soi hậu môn – trực tràng ống cứng ngay tại phòng khám có thể mang lại cơ hội chẩn đoán sớm cho bệnh nhân.
Tiến triển của u chủ yếu theo con đường xâm lấn tại chỗ, do vậy, bilan đánh giá chủ yếu dựa vào thăm khám lâm sàng và siêu âm nội soi hậu môn – trực tràng cho phép đánh giá mức độ xâm lấn so với cơ thắt, tổn thương ở các tổ chức lân cận và đánh giá hạch vùng.
Mặc dù di căn xa của ung thư ống hậu môn là khá hiếm gặp nhưng chụp cắt lớp ổ bụng – tiểu khung, chụp X-quang phổi vẫn được coi là cần thiết trong đánh giá giai đoạn bệnh. Trong khi đó, chụp cộng hưởng từ vẫn là lựa chọn đầu tay trong đánh giá xâm lấn vùng của các tổn thương vùng tiểu khung. Chụp PET – CT có giá trị và cần được cân nhắc chỉ định trong đánh giá giai đoạn bệnh nhưng không được khuyến cáo sử dụng thường quy [25].
Bên cạnh đó, các xét nghiệm máu đánh giá chức năng gan, thận, tim mạch cũng cần được tiến hành trước khi thực hiện can thiệp hóa xạ trị hay phẫu thuật.
Kháng nguyên ung thư biểu mô vảy (SCCAg) là một chất chỉ điểm khối u có thể sử dụng trong ung thư biểu mô ống hậu môn, tuy nhiên, giá trị của nó trong chẩn đoán và theo dõi còn chưa rõ ràng. Gần đây, một nghiên cứu hồi cứu tại Vương quốc Anh đưa ra mối liên quan giữa nồng độ SCCAg ban đầu trước khi điều trị với giai đoạn bệnh và tình tràng di căn hạch, do đó, có thể có vai trò trong hỗ trợ điều trị [27].
III – Chẩn đoán xác định :
Cũng giống như tất cả các loại ung thư khác, tiêu chuẩn vàng để chẩn đoán xác định ung thư ống hậu mônlà kết quả xét nghiệm giải phẫu bệnh. Do đó, tất cả các tổn thương nghi ngờ ở vùng hậu môn và các hạch lân cận cần được sinh thiết với mục đích phát hiện và sàng lọc ung thư ống hậu môn ở giai đoạn sớm.
IV – Chẩn đoán giải phẫu bệnh:
Phần lớn các trường hợp ung thư ống hậu môn là ung thư biểu mô vảy (74%), sau đó đến ung thư biểu mô tuyến từ trực tràng thấp (19%), u hắc tố (4%) và các loại u hiếm gặp khác như lymphome, sarcome de Kaposi, sarcome cơ trơn, carcinoide [8]. Các ung thư ở rìa hậu môn có thể xếp vào nhóm ung thư da và điều trị giống như một trường hợp ung thư da.
4.1. Ung thư biểu mô tuyến
- Thường là tổn thương xâm lấn từ trên xuống của ung thư trực tràng hoặc từ lớp biểu mô trụ của vùng chuyển tiếp, rất hiếm khi xuất phát trực tiếp từ các ống tuyến tại hốc hậu môn.
- Thường gặp ở người già hoặc trường hợp dị tật hậu môn trực tràng đôi. Biểu hiện lâm sàng không đặc hiệu với những đợt rò quanh hậu môn, áp-xe tái phát nhiều lần
- Vi thể: biểu mô tiết mucin, thường biệt hóa cao với các tế bào ống tuyến hoặc các nang chứa mucin có các tế bào u tự do trôi nổi, phản ứng viêm hạt với mucin và không thấy niêm mạc trực tràng.
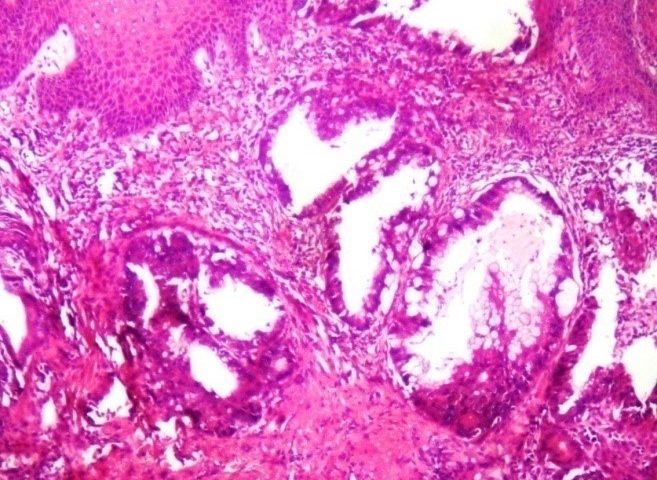
Ung thư biểu mô tuyến nhầy xâm lấn biểu mô vẩy của ống hậu môn 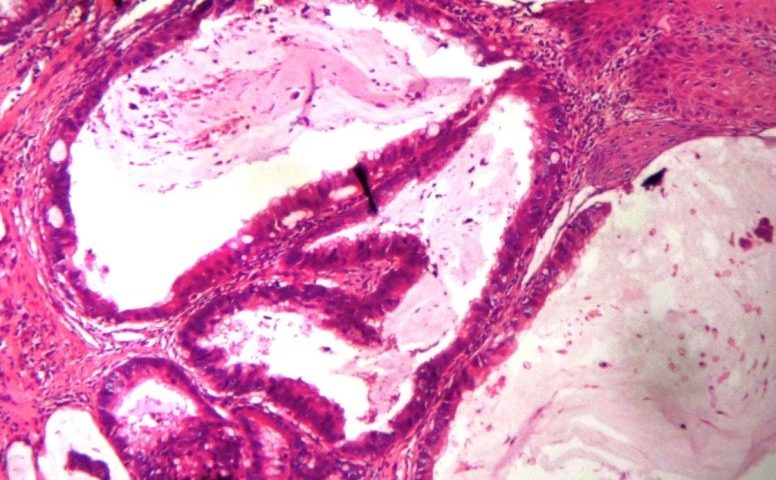
U chế nhầy mạnh trong lòng tuyến và mô đệm
Hình 3: Ung thư biểu mô tuyến của ống hậu môn
4.2. Ung thư biểu mô tế bào đáy
Rất hiếm, được chẩn đoán và điều trị như ung thư tế bào đáy của da. Phương pháp điều trị thường dùng là phẫu thuật cắt bỏ rộng rãi hoặc xạ trị.
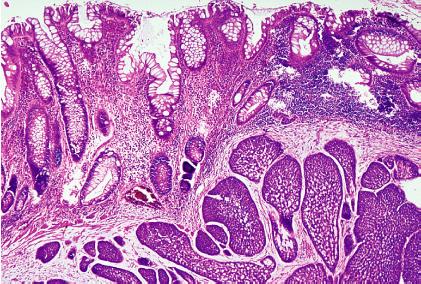
4.3. Ung thư biểu mô tế bào sáng
Rất hiếm gặp với các tế bào ung thư có nguyên sinh chất sáng màu, không bắt thuốc với mucin. [13]
4.4. Bệnh Paget:
Bệnh Paget được James Paget mô tả lần đầu vào năm 1874 với những tổn thương tại vú. Sau đó, tới năm 1889, Radcliffe Crocker báo cáo trường hợp bệnh Paget ngoài vú đầu tiên. [7] Bệnh Paget ở hậu môn thường gắn liền với một tổn thương ác tính tại chỗ.
Các khối u có GCDFP (+) và CK20 (-) thường kèm theo tổn thương ác tính tại da với dấu hiệu biệt hóa tuyến mồ hôi, trong khi các khối u bộc lộ MUC 2 (+), CK20 (+) hoặc GCDFP 15 (-) có thể đi kèm với một ung thư biểu mô đường tiêu hóa tiềm tàng. [9]
Tổn thương đại thể dạng xung huyết, loét hoặc dạng vết chàm. Hình ảnh vi thể: Các tế bào ung thư biểu mô thường đứng đơn độc, đôi khi tạo thành dạng chùm hoặc ống tuyến, bắt màu mucin, bộc lộ CK7, CEA, EMA và có thể cả CK2.

Bệnh Paget , Hình ảnh nhuộm HE 
Bệnh Paget, tế bào u dương tính với dấu ấn CK20 
Bệnh Paget, tế bào u dương tính với dấu ấn miễn dịch EMA
4.5. Ung thư biểu mô dạng sarcome:
Hay còn gọi là ung thư biểu mô tế bào hình thoi
4.6. Ung thư biểu mô tế bào nhỏ (thần kinh nội tiết) [26]
Hiếm gặp nhưng rất ác tính với tỷ lệ sống sau 5 năm chỉ dưới 10% và thường gặp ở các bệnh nhân nhiễm HPV.
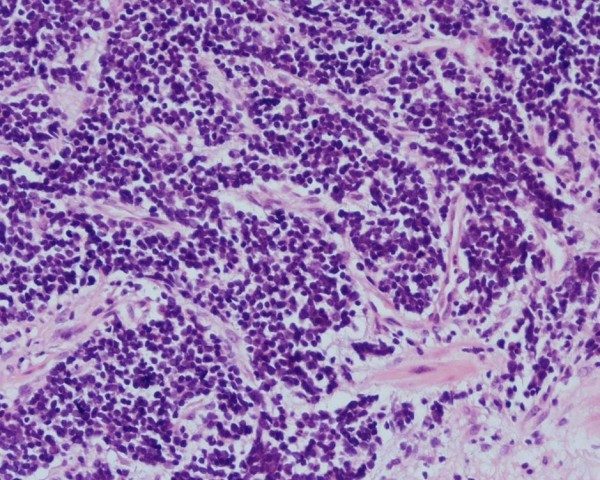
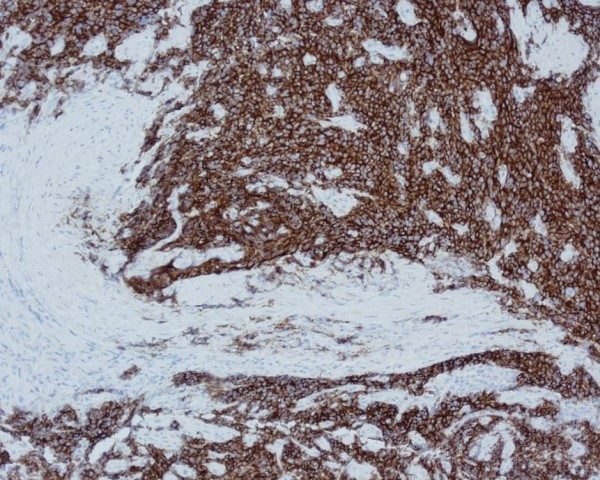
Vi thể: u không biệt hóa với các tế bào có nguyên sinh chất tối thiểu tập trung thành đám có hoại tử trung tâm. Hóa mô miễn dịch: bộc lộ chromogranin (usually), synaptophysin, neuron specific enolase, Leu7/CD57.
Hình 5: Ung thư biểu mô tế bào nhỏ của ống hậu môn
4.7. Ung thư biểu mô vảy [31]:
Thường gặp ở lứa tuổi trung niên, nữ nhiều hơn nam với biểu hiện lâm sàng có xuất huyết tiêu hóa thấp, đau tầng sinh môn hoặc sờ thấy khối tại chỗ.
Đại thể: thường gặp các khối u dạng nốt, loét bề mặt, kích thước từ 3 đến 4 cm hoặc hơn, xâm lấn sâu vào thành ống hậu ông và thâm nhiễm rộng ra xa ở lớp dưới niêm mạc của trực tràng cũng như ra ngoài rìa hậu môn. Vi thể: rất thay đổi nhưng gợi ý phần nào tới cấu trúc da (có keratin, biệt hóa cao) hoặc không (ở vùng chuyển tiếp), có thể dạng biểu mô lát với các thành phần đa dạng và che phủ bởi các tế bào nhỏ không biệt hóa ở xung quanh kèm theo hoại tử trung tâm khối u; có thể có thâm nhiễm mạnh của bạch cầu ưa toan.

Còn tiếp…
TÀI LIỆU THAM KHẢO
1. P. Vuong N. Lemarchand, J. Denis (1996), “Ano-rectal malignant non hodgkinian lymphoma : about 7 cases”, Acta Endoscopia, 26(1): p. 35 – 45.
2. American Joint Committee On Cancer, Anal Canal, in AJCC Cancer Staging Manual. 1997, Lippincott-Raven Publishers: Philadelphia. tr. 91 – 95.
3. Zucali R Doci R, La Monica G, Meroni E, Kenda R, Eboli M Et Al. (1996), “Primary chemoradiation therapy with fluorouracil and cisplatin for cancer of the anus: results in 35 consecutive patients”, J Clin Oncol, 14(12): p. 3121 – 3125.
4. John M Flam M, Pajak Tf, Petrelli N, Myerson R, Doggett S Et Al. (1996), “Role of mitomycin in combination with fluorouracil and radiotherapy, and of salvage chemoradiation in the definitive nonsurgical treatment of epidermoid carcinoma of the anal canal: results of a phase III randomized intergroup study”, J Clin Oncol, 14(9): p. 2527 – 2539.
5. Ayzac L Gerard Jp, Hun D, Romestaing P, Coquard R, Ardiet Jm Et Al. (1998), “Treatment of anal canal carcinoma with high dose radiation therapy and concomitant fluorouracilcisplatinum. Long-term results in 95 patients.”, Radiother Oncol, 46(3): p. 249 – 256.
6. Arie Perry Gustavo Alvarez, Benjamin R Tan and Hanlin L Wang (2006), “Expression of epidermal growth factor receptor in squamous cell carcinomas of the anal canal is independent of gene amplification”, Modern Pathology, 19: p. 942 – 949.
7. Chanda Jj. (1985), “Extramammary Paget’s disease: prognosis and relationship to internal malignancy”, J Am Acad Dermatol, 13(6): p. 1009 – 1014.
8. Rothenberger Da Klas Jv, Wong Wd, Madoff Rd (1999), “Malignant tumors of the anal canal: the spectrum of disease, treatment, and outcomes”, Cancer, 85(8): p. 1686 – 1693.
9. Montag Ag Kuan Sf, Hart J, Krausz T, Recant W (2001), “Differential expression of mucin genes in mammary and extramammary Paget’s disease”, Am J Surg Pathol, 25(12): p. 1469 – 1977.
10. Montbarbon Jf Papillon J (1987), “Epidermoid carcinoma of the anal canal. A series of 276 cases”, Dis Colon Rectum, 30(5): p. 324 – 333.
11. Bey P Peiffert D, Pernot M, Guillemin F, Luporsi E, Hoffstetter S Et Al. (1997), “Conservative treatment by irradiation of epidermoid cancers of the anal canal: prognostic factors of tumoral control and complications”, Int J Radiat Oncol Biol Phys, 37(2): p. 313 – 324.
12. Seitz Jf Peiffert D, Rougier P, Francois E, Cvitkovic F, Mirabel X Et Al. (1997), “Preliminary results of a phase II study of high-dose radiation therapy and neoadjuvant plus concomitant 5-fluorouracil with CDDP chemotherapy for patients with anal canal cancer: a French cooperative study”, Ann Oncol, 8(6): p. 575 – 581.
13. Watson Ph (1990), “Clear-cell carcinoma of the anal canal: a variant of anal transitional zone carcinoma.”, Hum Pathol, 21(3): p. 350 – 352.
14. Tiret E Pocard M, Nugent K, Dehni N, Parc R. (1998), “Results of salvage abdominoperineal resection for anal cancer after radiotherapy”, Dis Colon Rectum, 41(12): p. 1488 – 1493.
15. Ukcccr Anal Cancer Trial Working Party. Uk Co-Ordinating Committee on Cancer Research (1996), “Epidermoid anal cancer: results from the UKCCCR randomised trial of radiotherapy alone versus radiotherapy, 5-fluorouracil, and mitomycin”, Lancet, 348(9034): p. 1049 – 1054.
16. Compton Cc Ryan Dp, Mayer Rj (2000), “Carcinoma of the anal canal”, N Engl J Med 342(11): p. 792 – 800.
17. Vuagnat A Sobhani I, Walker F, Vissuzaine C, Mirin B, Hervatin F (2001), “Prevalence of high-grade dysplasia and cancer in the anal canal in human papillomavirus infected individuals”, Gastroenterology, 120(4): p. 857 – 866.
18. Wittekind C Sobin Lh, Anal Canal, in TNM: Classification of Malignant Tumours. 1997, Wiley-Liss, Inc.: New York. tr. 70 – 73.
19. Schlienger M Touboul E, Buffat L, Lefkopoulos D, Pene F, Parc R Et Al. (1994), “Epidermoid carcinoma of the anal canal. Results of curative-intent radiation therapy in a series of 270 patients”, Cancer, 73(6): p. 1569 – 1579.
20. De La Rochefordière A Vincent-Salomon A, Salmon R, Validire P, Zafrani B, Sastre-Garau X. (1996), “Frequent association of human papillomavirus 16 and 18 DNA with anal squamous cell and basaloid carcinoma”, Mod Pathol, 9(6): p. 614 – 620.
21. Mobiglia A Mistrangelo M, Cassoni P, Castellano I, Maass J, Martina Mc, Bellò M, Mussa A (2005), “Verrucous carcinoma of the anus or Buschke-Lowenstein tumor of the anus: staging and treatment. Report of 3 cases”, Suppl Tumori, 4(3): p. 29 – 30.
22. D.M. Ackermann, H.C. Jr. Polk & G.R. Schrodt (1985), “Desmoplastic melanoma of the anus”, Hum Pathol, 16(12): p. 1277 – 1279.
23. J. A. Ajani, K. A. Winter, L. L. Gunderson, J. Pedersen, và cs (2008), “Fluorouracil, mitomycin, and radiotherapy vs fluorouracil, cisplatin, and radiotherapy for carcinoma of the anal canal: a randomized controlled trial”, JAMA, 299(16): p. 1914-21.
24. H. Bartelink, F. Roelofsen, F. Eschwege, P. Rougier, và cs (1997), “Concomitant radiotherapy and chemotherapy is superior to radiotherapy alone in the treatment of locally advanced anal cancer: results of a phase III randomized trial of the European Organization for Research and Treatment of Cancer Radiotherapy and Gastrointestinal Cooperative Groups”, J Clin Oncol, 15(5): p. 2040 – 2049.
25. N. J. Bhuva, R. Glynne-Jones, L. Sonoda, W. L. Wong, và cs (2012), “To PET or not to PET? That is the question. Staging in anal cancer”, Ann Oncol, 23(8): p. 2078-82.
26. S. Doddi, T. Singhal, C. De Silva, F. Smedley, và cs (2009), “Small cell carcinoma of the anus: a case report”, Cases J, 2: p. 9396.
27. R. Glynne-Jones, J. M. Northover & A. Cervantes (2010), “Anal cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up”, Ann Oncol, 21 Suppl 5: p. v87-92.
28. H. L. Ioachim, C. Antonescu, F. Giancotti, B. Dorsett, và cs (1997), “EBV-associated anorectal lymphomas in patients with acquired immune deficiency syndrome”, Am J Surg Pathol, 21(9): p. 997-1006.
29. M. Miettinen, M. Furlong, M. Sarlomo-Rikala, A. Burke, và cs (2001), “Gastrointestinal stromal tumors, intramural leiomyomas, and leiomyosarcomas in the rectum and anus: a clinicopathologic, immunohistochemical, and molecular genetic study of 144 cases”, Am J Surg Pathol, 25(9): p. 1121-33.
30. G. R. Nigri, M. Dente, S. Valabrega, P. Aurello, và cs (2007), “Gastrointestinal stromal tumor of the anal canal: an unusual presentation”, World J Surg Oncol, 5: p. 20.
31. D. P. Ryan, C. C. Compton & R. J. Mayer (2000), “Carcinoma of the anal canal”, N Engl J Med, 342(11): p. 792-800.
32. L. Thalheimer, B. Richmond & J. Lohan (2008), “Leiomyosarcoma of the anal canal: case report and review of the literature”, Am Surg, 74(1): p. 76-8.
33. C. Faivre, P. Rougier, M. Ducreux, E. Mitry, và cs (1999), “[5-fluorouracile and cisplatinum combination chemotherapy for metastatic squamous-cell anal cancer]”, Bull Cancer, 86(10): p. 861-5.
Từ khóa » Giải Phẫu Bệnh Ung Thư ống Hậu Môn
-
Ung Thư Ống Hậu Môn: Nguyên Nhân, Triệu Chứng Và Cách Điều Trị
-
Ung Thư ống Hậu Môn
-
Ung Thư ống Hậu Môn Là Gì? Nguyên Nhân, Triệu Chứng Và Cách điều Trị
-
[PDF] đánh Giá Kết Quâ điều Trị Triệt Căn Ung Thư Trực Tràng Thấp Bằng Phẫu ...
-
UNG THƯ TRỰC TRÀNG - Slideshare
-
Ung Thư Hậu Môn - Rối Loạn Tiêu Hóa - Phiên Bản Dành Cho Chuyên Gia
-
Ứng Dụng Phẫu Thuật Miệng Nối đại Tràng - ống Hậu Môn Cải Thiện ...
-
Hình ảnh Giải Phẫu ống Hậu Môn Trên Cộng Hưởng Từ
-
Bệnh Học Ngoại Khoa Ung Thư Trực Tràng
-
Ung Thư Trực Tràng - Bệnh Viện Quân Y 103
-
Ung Thư ống Hậu Môn - - Q & A
-
Ung Thư Biểu Mô Tế Bào Vảy Của ống Hậu Môn
-
Giải Pháp Mới điều Trị Hiệu Quả Cho Bệnh Nhân Ung Thư Trực Tràng ...