đun Nóng Hh Fe Và S (không Có Khí Oxi) được Chất Rắn A ... - Hoc24
Có thể bạn quan tâm
HOC24
Lớp học Học bài Hỏi bài Giải bài tập Đề thi ĐGNL Tin tức Cuộc thi vui Khen thưởng- Tìm kiếm câu trả lời Tìm kiếm câu trả lời cho câu hỏi của bạn
Lớp học
- Lớp 12
- Lớp 11
- Lớp 10
- Lớp 9
- Lớp 8
- Lớp 7
- Lớp 6
- Lớp 5
- Lớp 4
- Lớp 3
- Lớp 2
- Lớp 1
Môn học
- Toán
- Vật lý
- Hóa học
- Sinh học
- Ngữ văn
- Tiếng anh
- Lịch sử
- Địa lý
- Tin học
- Công nghệ
- Giáo dục công dân
- Tiếng anh thí điểm
- Đạo đức
- Tự nhiên và xã hội
- Khoa học
- Lịch sử và Địa lý
- Tiếng việt
- Khoa học tự nhiên
- Hoạt động trải nghiệm
- Hoạt động trải nghiệm, hướng nghiệp
- Giáo dục kinh tế và pháp luật
Chủ đề / Chương
Bài học
HOC24
 Khách vãng lai Đăng nhập Đăng ký Khám phá Hỏi đáp Đề thi Tin tức Cuộc thi vui Khen thưởng
Khách vãng lai Đăng nhập Đăng ký Khám phá Hỏi đáp Đề thi Tin tức Cuộc thi vui Khen thưởng - Tất cả
- Toán
- Vật lý
- Hóa học
- Sinh học
- Ngữ văn
- Tiếng anh
- Lịch sử
- Địa lý
- Tin học
- Công nghệ
- Giáo dục công dân
- Tiếng anh thí điểm
- Hoạt động trải nghiệm, hướng nghiệp
- Giáo dục kinh tế và pháp luật
Câu hỏi
Hủy Xác nhận phù hợp Chọn lớp Tất cả Lớp 12 Lớp 11 Lớp 10 Lớp 9 Lớp 8 Lớp 7 Lớp 6 Lớp 5 Lớp 4 Lớp 3 Lớp 2 Lớp 1 Môn học Toán Vật lý Hóa học Sinh học Ngữ văn Tiếng anh Lịch sử Địa lý Tin học Công nghệ Giáo dục công dân Tiếng anh thí điểm Đạo đức Tự nhiên và xã hội Khoa học Lịch sử và Địa lý Tiếng việt Khoa học tự nhiên Hoạt động trải nghiệm Hoạt động trải nghiệm, hướng nghiệp Giáo dục kinh tế và pháp luật Mới nhất Mới nhất Chưa trả lời Câu hỏi hay
- Phương Đỗ
đun nóng hh Fe và S (không có khí oxi) được chất rắn A. Hòa tan A bằng HCL dư thoát ra 6.72 lít khí ở đktc, dd B và chất rắn E nặng 3.2g.cho khí thoát ra ở trên đi qua CuSO4 được 19.2g kết tủa đen.tính kim loại Fe, S ban đầu
Xem chi tiết Lớp 9 Hóa học Chương II. Kim loại 1 1 Gửi Hủy
Gửi Hủy  Hồ Hữu Phước
Hồ Hữu Phước  30 tháng 10 2017 lúc 6:19
30 tháng 10 2017 lúc 6:19 Fe+S\(\overset{t^0}{\rightarrow}FeS\)(1)
-A gồm FeS, Fe dư và S dư
Fe+2HCl\(\rightarrow\)FeCl2+H2(2)
FeS+2HCl\(\rightarrow\)FeCl2+H2S(3)
-E là S dư\(\rightarrow\)mS(dư)=3,2 gam\(\rightarrow\)nS=0,1mol
\(n_{Fe\left(dư\right)}=n_{H_2}=\dfrac{6,72}{22,4}=0,3mol\)
H2S+CuSO4\(\rightarrow\)CuS\(\downarrow\)+H2SO4(4)
\(n_{H_2S}=n_{CuS}=\dfrac{19,2}{96}=0,2mol\)
-Theo PTHH(1,3):
\(n_{Fe\left(pu\right)}=n_{S\left(pu\right)}=n_{FeS}=n_{H_2S}=0,2mol\)
\(\rightarrow\)Ban đầu có:
nFe=0,2+0,3=0,5mol\(\rightarrow\)mFe=0,5.56=28gam
nS=0,2+0,1=0,3 mol\(\rightarrow\)mS=0,3.32=9,6 gam
Đúng 1 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Nghị Hồng Vân Anh
Đun nóng hỗn hợp sắt và lưu huỳnh ko có ko khí thu được chất rắn A. Hòa tan A bằng HCl thoát ra 6,72 l khí D ở đktc và nhận được dung dịch B cùng chất rắn E. Cho khí D đi qua dung dịch CuSO4 tách ra 19,2 g kết tủa đen.
a) Viết phương trình.
b) Tính khối lượng sắt và lưu huỳnh ban đầu biết lượng E bằng 3,2 g.
Xem chi tiết Lớp 8 Toán Câu hỏi của OLM 0 0 Gửi Hủy
Gửi Hủy 
- T_T_N_Y_2005
Đun nóng hỗn hợp Fe và S có khối lượng m (g) sau khi phản ứng kết thúc thu được chất rắn, hòa tan chất rắn trong HCl (dư) thu được 4,47l khí. Dẫn toàn bộ chất khí này vào dd Chì(ll)nitrat thu được 23,9g và thoát ra 1 chất khí. Xác định m
Xem chi tiết Lớp 10 Hóa học 1 0 Gửi Hủy
Gửi Hủy  hnamyuh
hnamyuh  15 tháng 4 2021 lúc 21:14
15 tháng 4 2021 lúc 21:14 \(H_2S + Pb(NO_3)_2 \to PbS + 2HNO_3\\ n_{H_2S} = n_{PbS} = \dfrac{23,9}{239} = 0,1(mol)\\ \Rightarrow n_{H_2} = \dfrac{4,48}{22,4} - 0,1 = 0,1(mol)\\ Fe + 2HCl \to FeCl_2 + H_2\\ FeS + 2HCl \to FeCl_2 + H_2S\\ Fe + S \xrightarrow{t^o} FeS\\ n_{Fe} = n_{Fe} + n_{FeS} = n_{H_2} + n_{H_2S} = 0,2(mol)\\ n_S = n_{FeS} = n_{H_2S} = 0,1(mol)\\ \Rightarrow m = 0,2.56 + 0,1.32 = 14,4(gam) \)
Đúng 1 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Nguyễn Hoàng Nam
Nung nóng 3,72g hỗn hợp bột các kim loại Zn và Fe trong bột S dư. Chất rắn thu được sau phản ứng được hòa tan hoàn toàn bằng dung dịch H2SO4 loãng, nhận thấy có 1,344 lít khí (đktc) thoát ra. Xác định khối lượng mỗi kim loại trong hỗn hợp ban đầu.
Xem chi tiết Lớp 10 Hóa học 1 0 Gửi Hủy
Gửi Hủy  Ngô Quang Sinh
Ngô Quang Sinh  23 tháng 12 2019 lúc 6:36
23 tháng 12 2019 lúc 6:36 Đặt nZn = x mol; nFe = y mol.
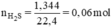
Ta có hệ phương trình: 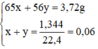
Giải hệ phương trình trên ta được:
x = 0,04 mol, y = 0,02 mol.
mZn = 65 × 0,04 = 2,6g
mFe = 56 × 0,02 = 1,12g
Đúng 1 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Nguyễn thị ngọc hoan
-
Đun nóng hh gồm 16,8g Fe và 3,2g S trong bình kín không có không khí thu được chất rắn A. Hòa tan A trong 0,5 lít dd HCl nồng độ x (mol/lít) dư thu được hh khí B và dd C
a) Tính % thể tích các khí trong B
b) Trung hòa HCl dư cần 100ml NaOH 2M. Tính CM của HCl đã dùng
(mk lm vt lại đầu bài😊😊)
Xem chi tiết Lớp 10 Hóa học Chương 6. Oxi - Lưu huỳnh 1 0 Gửi Hủy
Gửi Hủy  Lê Ng Hải Anh
Lê Ng Hải Anh  29 tháng 1 2021 lúc 20:44
29 tháng 1 2021 lúc 20:44 a, PT: \(Fe+S\underrightarrow{t^o}FeS\)
Ta có: \(n_{Fe}=\dfrac{16,8}{56}=0,3\left(mol\right)\)
\(n_S=\dfrac{3,2}{32}=0,1\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,3}{1}>\dfrac{0,1}{1}\), ta được Fe dư.
Chất rắn A gồm Fe dư và FeS.
Theo PT: \(n_{Fe\left(pư\right)}=n_{FeS}=n_S=0,1\left(mol\right)\)
\(\Rightarrow n_{Fe\left(dư\right)}=0,2\left(mol\right)\)
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(FeS+2HCl\rightarrow FeCl_2+H_2S\)
Theo PT: \(\left\{{}\begin{matrix}n_{H_2}=n_{Fe\left(dư\right)}=0,2\left(mol\right)\\n_{H_2S}=n_{FeS}=0,1\left(mol\right)\end{matrix}\right.\)
Ở cùng điều kiện nhiệt độ và áp suất, %V cũng là % số mol.
\(\Rightarrow\left\{{}\begin{matrix}\%V_{H_2}=\dfrac{0,2}{0,2+0,1}.100\%\approx66,67\%\\\%V_{H_2S}\approx33,33\%\end{matrix}\right.\)
b, Ta có: \(\Sigma n_{HCl\left(dadung\right)}=2n_{Fe}+2n_{FeS}=0,6\left(mol\right)\) (1)
PT: \(NaOH+HCl\rightarrow NaCl+H_2O\)
Ta có: \(n_{NaOH}=0,1.2=0,2\left(mol\right)\)
\(\Rightarrow n_{HCl\left(dư\right)}=n_{NaOH}=0,2\left(mol\right)\) (2)
Từ (1) và (2) \(\Rightarrow\Sigma n_{HCl}=0,8\left(mol\right)\)
\(\Rightarrow C_{M_{ddHCl}}=\dfrac{0,8}{0,5}=1,6\left(M\right)\)
Bạn tham khảo nhé!
Đúng 2 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Dt Dương
dẫn khí H2 dư đi qua 40 gam hỗn hợp A gồn Fe2O3 và CuO nung nóng đến phản ứng hoàn toàn thu được chất rắn B . Hòa tan B vào dung dịch HCL dư thu được dung dịch D , thoát ra V lít khí H2 (ở đktc) và còn lại chất rắn E . Nung E trong không khí đến khối lược không đổi thấy khối lượng chất rắn tăng 1,6 gam .viết phương trình phản ứng xảy ra . tính phần trăm khối lược các chất trong A và tính V
Xem chi tiết Lớp 8 Hóa học 1 0 Gửi Hủy
Gửi Hủy  𝓓𝓾𝔂 𝓐𝓷𝓱
𝓓𝓾𝔂 𝓐𝓷𝓱  12 tháng 3 2021 lúc 21:51
12 tháng 3 2021 lúc 21:51 PTHH: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
\(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
\(2Cu+O_2\underrightarrow{t^o}2CuO\)
Ta có: \(n_{O_2}=\dfrac{1,6}{32}=0,05\left(mol\right)\)\(\Rightarrow n_{Cu}=n_{CuO}=0,1\left(mol\right)\)
\(\Rightarrow\%m_{CuO}=\dfrac{0,1\cdot80}{40}\cdot100\%=20\%\)
\(\Rightarrow\%m_{Fe_2O_3}=80\%\)
Đúng 2 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Anh Đỗ Đức
bài 1:Cho 11,2 gam Fe và 4,8 gam S vào bình kín, nung nóng hỗn hợp thu được chấ rắn X
a. Cho biết thành phần chất X? Tính khối lượng các chất trong X?
b. Cho toàn bộ X qua dd HCl dư. Tính thể tích khí thoát ra ở đktc?
bài 2: hòa tan 7,68g kim loại M trong dd H2SO4 đặc, nóng dư thu được dung dịch X và 2,688 lít khí SO2 ( sản phẩm khử duy nhất đktc). Xác định tên kim loại M. Lượng khí SO2 thu được tác dụng với 500 ml dd NaOH 2M. Tính nồng độ mol các chất trong dd thu được sau phản ứng.
Xem chi tiết Lớp 10 Hóa học 1 0
 Gửi Hủy
Gửi Hủy  Nguyễn Ngọc Huy Toàn
Nguyễn Ngọc Huy Toàn  6 tháng 5 2022 lúc 21:31
6 tháng 5 2022 lúc 21:31 Bài 1.
\(n_{Fe}=\dfrac{11,2}{56}=0,2mol\)
\(n_S=\dfrac{4,8}{32}=0,15mol\)
\(Fe+S\rightarrow\left(t^o\right)FeS\)
0,2 < 0,15 ( mol )
0,15 0,15 0,15 ( mol )
X gồm FeS và Fe(dư)
\(\left\{{}\begin{matrix}m_{FeS}=0,15.88=13,2g\\m_{Fe\left(dư\right)}=\left(0,2-0,15\right).56=2,8g\end{matrix}\right.\)
\(Fe+HCl\rightarrow FeCl_2+H_2\)
0,05 0,05 ( mol )
\(FeS+2HCl\rightarrow FeCl_2+H_2S\)
0,15 0,15 ( mol )
\(V_{hh}=V_{H_2}+V_{H_2S}=\left(0,05+0,15\right).22,4=4,48l\)
Bài 2.
\(n_{SO_2}=\dfrac{2,688}{22,4}=0,12mol\)
\(M+nH_2SO_4\left(đ\right)\rightarrow\left(t^o\right)\dfrac{1}{2}M_2\left(SO_4\right)_n+\dfrac{n}{2}SO_2+nH_2O\)
\(\dfrac{0,24}{n}\) \(0,12\) ( mol )
\(\rightarrow\dfrac{0,24M_M}{n}=7,68\)
\(\Leftrightarrow M_M=32n\)
Xét:
n=1 --> Lưu huỳnh ( loại )
n=2 --> Cu ( nhận )
n=3 --> Loại
Vậy kim loại đó là Cu
\(n_{NaOH}=2.0,5=1mol\)
\(T=\dfrac{n_{NaOH}}{n_{SO_2}}=\dfrac{1}{0,12}=8,3\) --> Tạo ra muối Na2SO3
\(2NaOH+SO_2\rightarrow Na_2SO_3+H_2O\)
0,12 0,12 ( mol )
\(C_{M_{Na_2SO_3}}=\dfrac{0,12}{0,5}=0,24M\)
Đúng 4 Bình luận (4) Gửi Hủy
Gửi Hủy 
- Cát Phượng
Hòa tan 13,2g hh bột Fe,FeO,và Fe2O3 vào dd HCl.sau phản ứng thu được chất răn A là kim loại ; 0,56l khí B và một dd C.Cho dd C tác dụng hết với dd NaOH dư thu được kết tủa D.Nung kết tủa D trong không khí đến khối lượng không đổi thu được 12g chất rắn.Mặt khác,nếu lấy khối lượng chất rắn A đúng bằng khối lượng của nó đem hòa tan hoàn trong H2SO4 đặc,nóng dư thu được 3,36l khí mùi xốc(đktc).tính %FeO trong hh.
Xem chi tiết Lớp 10 Hóa học Chương 4. Phản ứng oxy hóa - khử 0 0 Gửi Hủy
Gửi Hủy 
- Nguyễn Hoàng Nam
Nung nóng 3,72g hỗn hợp bột các kim loại Zn và Fe trong bột S dư. Chất rắn thu được sau phản ứng được hòa tan hoàn toàn bằng dung dịch H2SO4 loãng, nhận thấy có 1,344 lít khí (đktc) thoát ra.
Viết các phương trình phản ứng xảy ra.
Xem chi tiết Lớp 10 Hóa học 1 0 Gửi Hủy
Gửi Hủy  Ngô Quang Sinh
Ngô Quang Sinh  31 tháng 12 2019 lúc 16:21
31 tháng 12 2019 lúc 16:21 Theo đề bài cho, bột S dư nên Fe và Zn tác dụng hết với S.
Phương trình hóa học của phản ứng:
Zn + S → ZnS
Fe + S → FeS
ZnS + H2SO4 → ZnSO4 + H2S
FeS + H2SO4 → H2S + FeSO4
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Nguyễn Hoàng Nam
Cho 100 gam hợp kim của Fe, Cr, Al tác dụng với dd NaOH dư thoát ra 5,04 lít khí (đktc) và một phần rắn không tan. Lọc lấy phần không tan đem hoà tan hết bằng dung dịch HCl dư (không có không khí) thoát ra 38,8 lít khí (đktc). Thành phần % khối lượng các chất trong hợp kim là
A. 13,66%Al; 82,29% Fe và 4,05% Cr.
B. 4,05% Al; 83,66%Fe và 12,29% Cr.
C. 4,05% Al; 82,29% Fe và 13,66% Cr.
D. 4,05% Al; 13,66% Fe và 82,29% Cr
Xem chi tiết Lớp 12 Hóa học 1 0 Gửi Hủy
Gửi Hủy  Ngô Quang Sinh
Ngô Quang Sinh  29 tháng 6 2019 lúc 14:28
29 tháng 6 2019 lúc 14:28 Đáp án C
Chỉ có Al tác dụng với NaOH
![]()
![]() =
= ![]()
![]()
![]()
![]()
![]()
 Gửi Hủy
Gửi Hủy Từ khóa » Fe + S Không Có Oxi
-
Đun Nóng Hỗn Hợp Fe, S (không Có Không Khí) Thu được Chất Rắn A ...
-
Viết PTHH Khi đốt Cháy Bột Fe Và S Trong điều Kiện Không ... - HOC247
-
Đun Nóng Hỗn Hợp Fe, S (không Có Không Khí) Thu được ...
-
A. Fe2S3. B. FeS. C. FeS2. D. Fe2(SO4)3.
-
Fe + S → FeS | , Phản ứng Hoá Hợp, Phản ứng Oxi-hoá Khử
-
Fe + S Trong điều Kiện Không Có Không Khí
-
Đun Nóng Hỗn Hợp Fe + S Trong Điều Kiện Không Có Không Khí ?
-
Đun Nóng Hỗn Hợp Gồm Bột Fe Và Bột S Trong điều ...
-
220897 Kim Loại Fe Tác Dụng Với S (không Có Oxi), Sinh Ra Muối Nào ...
-
Fe + S Trong Điều Kiện Không Có Không Khí
-
Nung Nóng 14,4 G Hỗn Hợp X Gồm Fe Và S (trong điều Kiện Không Có ...
-
Đun Nóng Hỗn Hợp Gồm Bột Fe Và Bột S Trong điều Kiện Không Có Oxi
-
Thực Hiện Các Thí Nghiệm Sau:(1). Đốt Dây Sắt Dư Trong Khí Clo.(2 ...
-
Đun Nóng Hỗn Hợp Gồm Bột Fe Và Bột S Trong điều Kiện Không Có Oxi ...