Dung Dịch FeSO4 Và Dung Dịch CuSO4 đều Tác Dụng được Với
Có thể bạn quan tâm
-
-
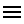
-
Mầm non
-
Lớp 1
-
Lớp 2
-
Lớp 3
-
Lớp 4
-
Lớp 5
-
Lớp 6
-
Lớp 7
-
Lớp 8
-
Lớp 9
-
Lớp 10
-
Lớp 11
-
Lớp 12
-
Thi vào lớp 6
-
Thi vào lớp 10
-
Thi Tốt Nghiệp THPT
-
Đánh Giá Năng Lực
-
Khóa Học Trực Tuyến
-
Hỏi bài
-
Trắc nghiệm Online
-
Tiếng Anh
-
Thư viện Học liệu
-
Bài tập Cuối tuần
-
Bài tập Hàng ngày
-
Thư viện Đề thi
-
Giáo án - Bài giảng
-
Tất cả danh mục
-
- Mầm non
- Lớp 1
- Lớp 2
- Lớp 3
- Lớp 4
- Lớp 5
- Lớp 6
- Lớp 7
- Lớp 8
- Lớp 9
- Lớp 10
- Lớp 11
- Lớp 12
- Thi Chuyển Cấp
-
- Hôm nay +3
- Ngày 2 +3
- Ngày 3 +3
- Ngày 4 +3
- Ngày 5 +3
- Ngày 6 +3
- Ngày 7 +5
Nâng cấp gói Pro để trải nghiệm website VnDoc.com KHÔNG quảng cáo, và tải file cực nhanh không chờ đợi.
Tìm hiểu thêm » Mua ngay Từ 79.000đ Hỗ trợ ZaloDãy điện hóa của kim loại
- Dung dịch FeSO4 và dung dịch CuSO4 đều tác dụng được với
- Ý nghĩa dãy điện hóa của kim loại
- Xác định chiều của phản ứng oxi hóa – khử
- Câu hỏi vận dụng liên quan
Dung dịch FeSO4 và dung dịch CuSO4 đều tác dụng được với được VnDoc biên soạn hướng dẫn bạn đọc dựa vào dãy điện hóa của kim loại để xác định cặp oxi hóa khử của kim loại.
Dung dịch FeSO4 và dung dịch CuSO4 đều tác dụng được với
A. Ag
B. Cu
C. Fe
D. Zn
Đáp án hướng dẫn giải chi tiết
Ta có cặp oxi hóa khử sắp xếp như sau: Zn2+/ Zn; Fe2+/ Fe; Cu2+/ Cu do vậy Fe2+ và Cu2+ có tính oxi hóa mạnh hơn Zn2+ nên có thể oxi hóa Zn thành Zn2+.
Zn + Fe2+ → Fe + Zn2+
Zn + Cu2+ → Cu + Zn2+
Đáp án D
Ý nghĩa dãy điện hóa của kim loại
Dãy điện hóa của kim loại là dãy những cặp oxi hóa khử của kim loại được được sắp xếp theo chiều tăng dần tính oxi hóa của ion kim loại và giảm dần tính khử của kim
Các kim loại đứng phía trước sẽ có tính khử mạnh hơn kim loại đứng sau. Ngược lại, các kim loại đứng sau sẽ có tính oxi hóa mạnh hơn những kim loại đứng trước.
Ví dụ: Ag2++ Cu → Cu2++ Ag (kết tủa)
Quy tắc α cũng có những trường hợp ngoại lệ.
Thí dụ:
Các kim loại kiềm đầu dãy sẽ không khử kim loại. Mà ngược lại, chúng sẽ khử nước.
2K + 2H2O → 2KOH + H2
Các kim loại từ Mg đến trước Hidro, khi tác dụng với dung dịch axit sẽ tạo ra muối và giải phóng khí hidro.
Thí dụ:
Fe + 2HCl → FeCl2 + H2
Al, Fe, Cr sẽ thụ động với HNO3 đặc nguội và H2SO4 đặc nguội.
Các kim loại cuối dãy (Au, Pt,…) ko tác dụng được với axit.
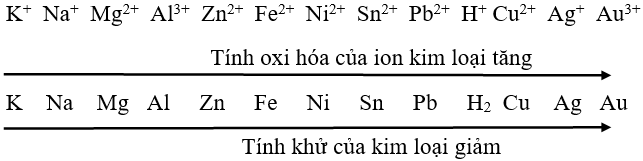
Dãy điện hóa của kim loại đầy đủ cho biết tính oxi hóa và tính khử của các chất
Xác định chiều của phản ứng oxi hóa – khử
Quy tắc α
Để viết đúng chiều của phản ứng oxi hóa – khử, người ta viết cặp oxi hóa – khử có thế điện cực chuẩn nhỏ ở bên trái, cặp oxi hóa – khử có thế điện cực chuẩn lớn hơn ở bên phải rồi viết phương trình theo quy tắc α
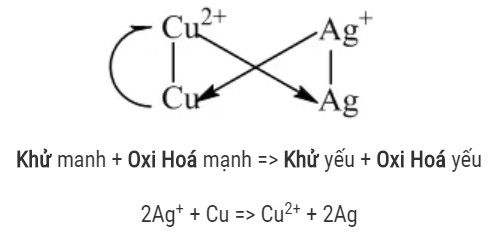
Xác định suất điện động chuẩn của pin điện hóa
Eopin = Eo (+) – Eo (−)
Câu hỏi vận dụng liên quan
Câu 1. Các hỗn hợp chất nào sau đây không cùng tồn tại trong cùng một dung dịch?
A. Ni(NO3)2 và AgNO3
B. Fe(NO3)2 và AgNO3
C. Fe(NO3)2 và Cu(NO3)2
D. Hg(NO3)2 và Cu(NO3)2
Xem đáp án Đáp án BCâu 2. Cho bột Fe vào dung dịch AgNO3 dư, sau khi kết thúc thí nghiệm thu được dung dịch X gồm:
A. Fe(NO3)2, H2O
B. Fe(NO3)2, AgNO3
C. Fe(NO3)3, AgNO3
D. Fe(NO3)2, Fe(NO3)3, AgNO3
Xem đáp án Đáp án CPhương trình phản ứng hóa học
2AgNO3 + Fe → 2Ag + Fe(NO3)2
AgNO3 + Fe(NO3)2 → Ag + Fe(NO3)3
Câu 3. Cho hỗn hợp gồm Fe và Mg vào dung dịch AgNO3, khi các phản ứng xảy ra hoàn toàn thu được dung dịch X (gồm hai muối) và chất rắn Y (gồm hai kim loại). Hai muối trong X là
A. Mg(NO3)2 và Fe(NO3)2.
B. Fe(NO3)3 và Mg(NO3)2.
C. AgNO3 và Mg(NO3)2.
D. Fe(NO3)2 và AgNO3.
Xem đáp án Đáp án AChất rắn Y gồm hai kim loại có tính khử yếu nhất là: Ag, Fe
Dung dịch X gồm hai muối của kim loại có tính khử mạnh nhất, mà Fe dư
→ Hai muối trong X là Mg(NO3)2 và Fe(NO3)2.
Mg + 2Ag+ → Mg2+ + 2Ag↓
Fe + 2Ag+ → Fe2+ + 2Ag ↓
Câu 4. X là kim loại phản ứng được với dung dịch H2SO4 loãng, Y là kim loại tác dụng được với dung dịch Fe(NO3)3. Hai kim loại X, Y lần lượt là (biết thứ tự trong dãy thế điện hoá: Fe3+/Fe2+ đứng trước Ag+/Ag
A. Fe, Cu.
B. Cu, Fe.
C. Ag, Mg.
D. Mg, Ag.
Xem đáp án Đáp án AX phản ứng được với dung dịch H2SO4 → X đứng trước H trong dãy điện hóa → Loại đáp án B vì có Cu, loại C vì có Ag
Y tác dụng được với Fe3+ → Loại đáp án D
Đáp án A: X là Fe, Y là Cu
Fe + H2SO4 loãng → FeSO4 + H2↑
Cu + 2Fe(NO3)3 → 2Fe(NO3)2 + Cu(NO3)2
Câu 5. Cho khí CO (dư) đi vào ống sứ nung nóng đựng hỗn hợp X gồm Al2O3, MgO, Fe3O4, CuO thu được chất rắn Y. Cho Y vào dung dịch NaOH (dư), khuấy kĩ, thấy còn lại phần không tan Z. Giả sử các phản ứng xảy ra hoàn toàn. Phần không tan Z gồm
A. MgO, Fe, Cu.
B. Mg, Fe, Cu.
C. MgO, Fe3O4, Cu.
D. Mg, Al, Fe, Cu.
Xem đáp án Đáp án ACO khử được các oxit của kim loại đứng sau Al trong dãy hoạt động hoá học.
CO + Al2O3 → không phản ứng
CO + MgO → không phản ứng
4CO + Fe3O4 → 3Fe + 4CO2
CO + CuO → Cu + CO2
→ Hỗn hợp Y: Al2O3, MgO, Cu, Fe
Al2O3 + 2NaOH → 2NaAlO2 + H2O
→ Hỗn hợp Z: MgO, Fe, Cu
Câu 6. X là kim loại phản ứng được với dung dịch H2SO4 loãng, Y là kim loại tác dụng được với dung dịch Fe(NO3)3. Hai kim loại X, Y lần lượt là (biết thứ tự trong dãy thế điện hoá: Fe3+/Fe2+ đứng trước Ag+/Ag.
A. Fe, Cu.
B. Cu, Fe.
C. Ag, Mg.
D. Mg, Ag.
Xem đáp án Đáp án AX phản ứng được với dung dịch H2SO4 → X đứng trước H trong dãy điện hóa → Loại đáp án B vì có Cu, loại C vì có Ag
Y tác dụng được với Fe3+ → Loại đáp án D
Đáp án A: X là Fe, Y là Cu
Fe + H2SO4 loãng → FeSO4 + H2↑
Cu + 2Fe(NO3)3 → 2Fe(NO3)2 + Cu(NO3)2
Câu 7. Cho luồng khí H2 dư qua hỗn hợp các oxit CuO, Fe2O3, ZnO, MgO nung nóng ở nhiệt độ cao. Sau phản ứng, hỗn hợp chất rắn còn lại là
A. Cu, Fe, ZnO, MgO.
B. Cu, Fe, Zn, Mg.
C. Cu, Fe, Zn, MgO.
D. Cu, FeO, ZnO, MgO.
Xem đáp án Đáp án CCuO, Fe2O3, ZnO bị bởi khử C, CO, H2 tạo thành Cu, Fe, Zn.
Còn lại MgO.
=> Hỗn hợp chất rắn thu được là Cu, Fe, Zn, MgO.
Câu 8. Cho hỗn hợp kim loại Mg, Zn, Fe vào dung dịch chứa AgNO3 và Cu(NO3)2. Sau khi phản ứng xảy ra hoàn toàn thu được dung dịch X gồm 3 muối và chất rắn Y gồm 3 kim loại. Ba muối trong X là
A. Mg(NO3)2, Fe(NO3)3, AgNO3.
B. Mg(NO3)2, Zn(NO3)2, Cu(NO3)2.
C. Mg(NO3)2, Zn(NO3)2, Fe(NO3)3.
D. Mg(NO3)2, Zn(NO3)2, Fe(NO3)2.
Xem đáp án Đáp án DDãy điện hóa : Mg2+/Mg Zn2+/Zn Fe2+/Fe Cu2+/Cu Ag+/Ag
→ Dung dịch X gồm 3 muối (ion có tính oxi hóa yếu nhất) là Mg(NO3)2, Zn(NO3)2 và Fe(NO3)2
............................................
Để tham khảo chi tiết đầy đủ nội dung dãy điện hóa của kim loại, mời các bạn ấn vào link:
- Dãy điện hóa của kim loại chi tiết đầy đủ
>> Mời các bạn tham khảo thêm một số câu hỏi liên quan:
- Kim loại nào sau đây có tính khử mạnh nhất
- Trong pin điện hóa Zn- Cu quá trình khử trong pin là
- Ion kim loại nào sau đây có tính oxi hóa yếu nhất
- Ion kim loại nào sau đây có tính oxi hóa mạnh nhất
- Sắt tây là sắt được phủ lên bề mặt bởi kim loại nào sau đây
- Chia sẻ bởi:
 Haraku Mio
Haraku Mio

Có thể bạn quan tâm
Xác thực tài khoản!Theo Nghị định 147/2024/ND-CP, bạn cần xác thực tài khoản trước khi sử dụng tính năng này. Chúng tôi sẽ gửi mã xác thực qua SMS hoặc Zalo tới số điện thoại mà bạn nhập dưới đây:
Số điện thoại chưa đúng định dạng! Xác thực ngay Số điện thoại này đã được xác thực! Bạn có thể dùng Sđt này đăng nhập tại đây! Lỗi gửi SMS, liên hệ Admin Sắp xếp theo Mặc định Mới nhất Cũ nhấtTham khảo thêm
-
Tơ capron thuộc loại - Điều chế Tơ capron
-
Polymer nào sau đây được tổng hợp bằng phản ứng trùng ngưng
-
Công thức phân tử của cao su thiên nhiên
-
Bộ 5 đề thi học kì 1 môn Hóa học lớp 12 năm học 2025 - 2026 Có đáp án
-
Cách gọi tên Amine, Amino Acid
-
Công thức cấu tạo của chất béo
-
Phenylammonium chloride (C6H5NH3Cl)
-
Công thức tính nhanh số đồng phân
-
Lý thuyết hóa 12 học kì 1 đầy đủ chi tiết nhất
-
Công thức tổng quát của ester
-
 Lớp 12
Lớp 12 -
 Hóa 12 - Giải Hoá 12
Hóa 12 - Giải Hoá 12

Hóa 12 - Giải Hoá 12
-
Công thức tính nhanh số đồng phân
-
Phenylammonium chloride (C6H5NH3Cl)
-
Công thức tổng quát của ester
-
Tơ capron thuộc loại - Điều chế Tơ capron
-
Công thức cấu tạo của chất béo
-
Lý thuyết hóa 12 học kì 1 đầy đủ chi tiết nhất

Gợi ý cho bạn
-
Bài tập cuối tuần môn Toán lớp 6 Cánh diều - Tuần 1
-
Được 18-20 điểm khối A1 nên đăng ký trường nào?
-
TOP 13 Viết thư cho ông bà để hỏi thăm và kể về tình hình gia đình em lớp 4
-
Bài tập tiếng Anh lớp 10 Unit 1 Family life nâng cao
-
Trong phân tử của cacbohiđrat luôn có
-
Dãy gồm các chất đều làm giấy quỳ tím ẩm chuyển sang màu xanh là
Từ khóa » Feso4 Và Cuso4 đều Tác Dụng được Với
-
Dung Dịch FeSO4 Và Dung Dịch CuSO4 đều Tác Dụng ...
-
Dung Dịch FeSO4 Và Dung Dịch CuSO4 đều Tác Dụng được Với Ag
-
Dung Dịch FeSO4 Và Dung Dịch CuSO4 đều Tác Dụng được Với
-
Dung Dịch FeSO4 Và Dung Dịch CuSO4 đều Tác Dụng được Với A. Ag ...
-
Dung Dịch Feso4 Và Dung Dịch Cuso4 đều Tác Dụng được Với
-
Dung Dịch FeSO4 Và Dung Dịch CuSO4 đều Tác Dụng ...
-
Dung Dịch FeSO4 Và Dung Dịch CuSO4 đều Tác Dụng được
-
Dung Dịch FeSO4 Và Dung Dịch CuSO4 đều Tác Dụng ...
-
Dung Dịch Feso4 Và Dung Dịch Cuso4 đều Tác Dụng được Với
-
Dung Dịch FeSO4 Và Dung Dịch CuSO4 đều Tác ...
-
Dung Dịch FeSO4 Và Dung Dịch CuSO4 đều Tác Dụng ... - Haylamdo
-
Dung Dịch FeSO4 Và Dung Dịch CuSO4 đều Tác Dụng được Với Kim ...
-
Dung Dịch FeSO4 Và Dung Dịch CuSO4 đều Tác Dụng được Với
-
Dung Dịch ZnSO4 Và Dung Dịch CuSO4 đều Tác Dụng được Với



























