Giải SBT Hóa 8 Bài 10: Hóa Trị
Nâng cấp gói Pro để trải nghiệm website VnDoc.com KHÔNG quảng cáo, và tải file cực nhanh không chờ đợi.
Tìm hiểu thêm » Mua ngay Từ 79.000đ Hỗ trợ ZaloGiải SBT Hóa 8 bài 10
- A. Giải sách bài tập Hóa 8 bài 10: Hóa trị
- Bài 10.1 trang 14 SBT Hóa 8
- Bài 10.2 trang 14 SBT Hóa 8
- Bài 10.3 trang 14 SBT Hóa 8
- Bài 10.4 trang 14 SBT Hóa 8
- Bài 10.5 trang 14 SBT Hóa 8
- Bài 10.6 trang 14 SBT Hóa 8
- Bài 10.7 trang 14 SBT Hóa 8
- Bài 10.8 trang 15 SBT Hóa 8
- Bài 10.9* trang 15 SBT Hóa 8
- Bài 10.10* trang 15 SBT Hóa 8
- B. Giải Hóa 8 bài 10 SGK: Hóa trị
- C. Trắc nghiệm hóa 8 bài 10
Giải SBT Hóa 8 bài 10: Hóa trị tổng hợp lời giải chi tiết, rõ ràng các câu hỏi trong vở bài tập Hóa học lớp 8, các bài giải tương ứng với từng bài học trong sách giúp cho các em học sinh ôn tập và củng cố các dạng bài tập, rèn luyện kỹ năng giải môn Hóa lớp 8. Chúc các em học tốt.
- Giải bài tập SBT Hóa học lớp 8 bài 9: Công thức hóa học
- Giải bài tập SBT Hóa học lớp 8 bài 12: Sự biến đổi chất
- Giải bài tập SBT Hóa học lớp 8 bài 13: Phản ứng hóa học
A. Giải sách bài tập Hóa 8 bài 10: Hóa trị
Bài 10.1 trang 14 SBT Hóa 8
Chép vào vở bài tập những câu sau đây với đầy đủ các từ hay cụm từ thích hợp chọn trong khung.
| Hóa trị, nguyên tử, nguyên tố, nhóm nguyên tử, khả năng liên kết, phân tử. | "Hóa trị là con số biểu thị ... của ... nguyên tố này (hay ...) với ... nguyên tố khác. Hóa trị của một ... (hay ...) được xác định theo ... của H chọn là đơn vị và ... của O là hai đơn vị". |
Đáp án hướng dẫn giải chi tiết
Khả năng liên kết; nguyên tử (hay nhóm nguyên tử); nguyên tử; nguyên tố(hay nhóm nguyên tố); hóa trị; hóa trị.
Bài 10.2 trang 14 SBT Hóa 8
Người ta quy ước mỗi vạch ngang giữa kí hiệu biểu thị một hóa trị của mỗi bên nguyên tử. Cho biết sơ đồ công thức của hợp chất giữa nguyên tố X, Y với H và O như sau:
a) Tính hóa trị của X và Y.
b) Viết sơ đồ công thức hợp chất giữa nguyên tố Y và O, giữa nguyên tố X và Y.
Đáp án hướng dẫn giải chi tiết
a) Vì và X = O → X có hóa trị II.
Vì → Y có hóa trị I.
b) Y-O-Y; Y-X-Y.
Bài 10.3 trang 14 SBT Hóa 8
Viết sơ đồ công thức của các hợp chất sau: HCl; H2O; NH3; CH4.
Đáp án hướng dẫn giải chi tiết
a) HCl: H-Cl
b) H2O: H-O-H
c) NH3:
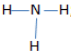
d) CH4:
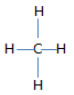
Bài 10.4 trang 14 SBT Hóa 8
Tính hóa trị của mỗi nguyên tố trong công thức phân tử các hợp chất sau. Cho biết S hóa trị II:
K2S; MgS; Cr2S3; CS2
Đáp án hướng dẫn giải chi tiết
a) K2S: Ta có Ka2SII
Theo quy tắc hóa trị: a.2 = II.1 → a = (II.1)/2= I
Vậy K có hóa trị I.
b) MgS: Ta có MgbSII
Theo quy tắc hóa trị: b.1 = II.1 → b = (II.1)/I = II
Vậy Mg có hóa trị II.
c, Cr2S3: Ta có Crb2S3II
Theo quy tắc hóa trị: c.2 = II.3 → c = (II.3)/2 = III
Vậy Cr có hóa trị III.
d, CS2: Ta có CdSII2 ![]()
Theo quy tắc hóa trị: d.1 = II.2 → d = (II.2)/1 = IV
Vậy C có hóa trị IV.
Bài 10.5 trang 14 SBT Hóa 8
Tính hóa trị của mỗi nguyên tố trong công thức phân tử các hợp chất sau, biết nhóm (NO3) hóa trị O và nhóm (CO3) hóa trị II:
Ba(NO3)2; Fe(NO3)3; CuCO3; Li2CO3.
Đáp án hướng dẫn giải bài tập
a) Ba(NO3)2: Ta có Baa(NO3)I3
Theo quy tắc hóa trị: a.1 = II.2 → a = (I.2)/1 = II
Vậy Ba có hóa trị II.
b) Fe(NO3)3: Ta có Feb(NO3)I3
Theo quy tắc hóa trị: b.1 = I.3 → b = (I.3)/1 = III
Vậy Fe có hóa trị III.
c) CuCO3: Ta có Cuc(CO3)II
Theo quy tắc hóa trị: c.1 = II.1 → c = (II.1)/1 = II
Vậy Cu có hóa trị II.
d) Li2CO3: Ta có Lid(CO3)II
Theo quy tắc hóa trị: d.2 = II.1 → d = (II.1)/2 = I
Vậy Li có hóa trị I.
Bài 10.6 trang 14 SBT Hóa 8
Lập công thức hóa học của những chất hai nguyên tố như sau:
Si(IV) và H; P(V) và O;
Fe(III) và Br(I); Ca và N(III).
Đáp án hướng dẫn giải bài tập
a) Si(IV) và H: Ta có: SiIVxHIy
Theo quy tắc hóa trị: IV.x = y.I
Tỉ lệ:
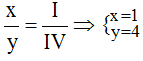 .
.
Vậy công thức hóa học của SixHy là SiH4.
b) P(V) và O: Ta có: ![]()
Theo quy tắc hóa trị: V.x = II.y
Tỉ lệ:
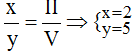 .
.
Vậy công thức hóa học của PxOy là P2O5.
c) Fe(III) và Br(I): Ta có: ![]()
Theo quy tắc hóa trị: III.x = I.y
Tỉ lệ:
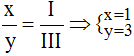 .
.
Vậy công thức hóa học của FexBry là FeBr3.
d) Ca và N(III): Ta có: 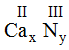
Theo quy tắc hóa trị: II.x = III.y
Tỉ lệ:
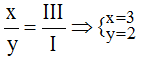 .
.
Vậy công thức hóa học của CaxNy là Ca3N2.
Bài 10.7 trang 14 SBT Hóa 8
Lập công thức hóa học của những chất hợp chất tạo bởi một nguyên tố và nhóm nguyên tử như sau:
Ba và nhóm (OH); Al và nhóm (NO3);
Cu(II) và nhóm (CO3) Na và nhóm (PO4)(III).
Đáp án hướng dẫn giải bài tập
a) Ba và nhóm (OH): Ta có: ![]()
Theo quy tắc hóa trị: II.x = I.y
Tỉ lệ:
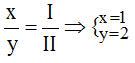
Vậy công thức hóa học của Bax(OH)y là Ba(OH)2.
b) Al và nhóm (NO3): Ta có: ![]()
Theo quy tắc hóa trị: III.x = I.y
Tỉ lệ:
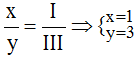
Vậy công thức hóa học của Alx(NO3)y là Al(NO3)3.
c) Cu(II) và nhóm (CO3): Ta có: ![]()
Theo quy tắc hóa trị: II.x = II.y
Tỉ lệ: 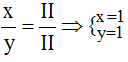
Vậy công thức hóa học của Cux(CO3)y là CuCO3.
d) Na và nhóm (PO4)(III): Ta có: ![]()
Theo quy tắc hóa trị: I.x = III.y
Tỉ lệ: 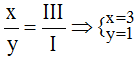
Vậy công thức hóa học của Nax(PO4)y là Na3PO4.
Bài 10.8 trang 15 SBT Hóa 8
Biết Cr (crom) hóa trị III, hãy chọn công chức hóa học đúng trong số các công thức cho sau đây:
(1) CrSO4; (2) Cr2S04; (3) CrO; (4) CrO2
(5) Cr(SO4)2; (6) Cr2(SO4)3. (7) Cr2O; (8) Cr2O3
b) Tính phân tử khối của những chất biểu diễn bởi công thức hoá học đúng.
Đáp án hướng dẫn giải bài tập
a) Những công thức hoá học đúng:
Cr hoá trị II: CrSO4, CrO.
Cr hoá trị III: Cr2(SO4)3, Cr2O3.
b) Phân tử khối của những chất biểu diễn bởi các công thức hoá học này :
CrSO4 = 52 + 32 + 4 . 16 = 148 (đvC),
CrO = 52 + 16 = 68 (đvC).
Cr2(SO4)3 = 2 . 52 + 3 . (32 + 4 . 16) = 392 (đvC),
Cr2O3 = 2 . 52 + 3 .16 = 152 (đvC).
Bài 10.9* trang 15 SBT Hóa 8
Người ta xác định được rằng nguyên tố silic(Si) chiếm 87,5% về khối lượng trong hợp chất với nguyên tố hidro.
a) Viết công thức hóa học và tính phân tử khối của hợp chất.
b) Xác định hóa trị của Silic trong hợp chất.
Đáp án hướng dẫn giải bài tập
a) Gọi công thức của hợp chất là SixHy.
Theo đề bài ta có:
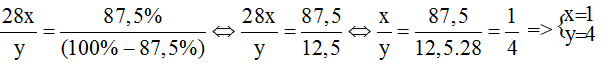
CTHH của hợp chất là SiH4.
Phân tử khối là: 28 + 4.1 = 32 (đvC)
b) Hóa trị của Si trong hợp chất SiH4 là IV.
Bài 10.10* trang 15 SBT Hóa 8
Phân tích một mẫu hợp chất tạo bởi hai nguyên tố là sắt và oxi. Kết quả cho thấy cứ 7 phần khối lượng sắt có tương ứng với 3 phần khối lượng oxi.
a) Viết công thức hóa học và tính phân tử khối của hợp chất.
b) Xác định hóa trị của sắt trong hợp chất.
Đáp án hướng dẫn giải bài tập
a) Công thức chung của hợp chất FexOy.
Theo đề bài ta có:
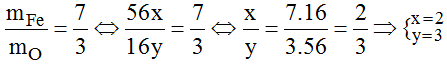
Vậy CTHH của hợp chất là Fe2O3.
Phân tử khối là: 56.2 + 16.3 = 160 (đvC)
b) Hóa trị của Fe trong hợp chất là III.
>> Mời các bạn tham khảo nội dung giải bài tậpsách bài tập hóa 8 bài tiếp theo tại: Giải SBT Hóa 8 bài 11: Luyện tập chương 1
B. Giải Hóa 8 bài 10 SGK: Hóa trị
Để giúp các em học sinh học tốt môn Hóa học 8 hơn cũng như biết cách giải các dạng bài tập hóa 8. VnDoc đã biên soạn hướng dẫn giải chi tiết các bài tập trong sách giáo khoa tại: Giải Hóa 8 Bài 10 Hóa trị
C. Trắc nghiệm hóa 8 bài 10
Ngoài các dạng câu hỏi bài tập sách giáo khoa cũng như sách bài tập, các bạn học sinh làm thêm các dạng câu hỏi bài tập dưới hình thức trắc nghiệm, giúp rèn luyện kĩ năng thao tác làm bài tập trắc nghiệm, từ đó ghi nhớ nội dung kiến thức bài học nhanh hơn. Mời các bạn tham khảo chi tiết bộ câu hỏi trắc nghiệm hóa 8 bài 10 tại: Trắc nghiệm Hóa học 8 bài 10
.................................................
Mời các bạn tham khảo thêm một số tài liệu liên quan:
- Hóa học 8 Bài 11: Bài luyện tập 2
- Giải bài tập trang 41 SGK Hóa học lớp 8: Bài luyện tập 2
- Hóa học 8 Bài 12: Sự biến đổi chất
Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Chuyên đề Toán 8, Chuyên đề Vật Lý 8, Chuyên đề Hóa 8, Tài liệu học tập lớp 8 mà VnDoc tổng hợp và đăng tải.
Ngoài ra, VnDoc.com đã thành lập group chia sẻ tài liệu học tập THCS miễn phí trên Facebook: Tài liệu học tập lớp 8. Mời các bạn học sinh tham gia nhóm, để có thể nhận được những tài liệu mới nhất.
Từ khóa » Hóa Sbt 8 Bài 10
-
Giải SBT Hóa 8 Bài 10: HÓA TRỊ
-
Giải SBT Hóa Học 8 - Bài 10: Hóa Trị
-
Giải SBT Hóa 8 Bài 10. Hóa Trị | Giải Sách Bài Tập Hóa 8 - TopLoigiai
-
SBT Hóa 8 Bài 10: Hóa Trị - Haylamdo
-
Giải SBT Hóa 8 Bài 10: Hóa Trị
-
Hoá Học 8 - Sách Bài Tập - Bài 10 - Hóa Trị - Cô Nguyễn Thị Thu (DỄ ...
-
Giải SBT Hóa Học 8 Bài 10: Hóa Trị
-
Giải SBT Hóa 8 Bài 10 - TopList #Tag
-
Giải SBT Hóa Học 8 - Bài 10: Hóa Trị
-
Giải Hóa 8 Bài 10: Hóa Trị | Hay Nhất Giải Bài Tập Hóa Học 8.
-
Giải SBT Hóa 8 Bài 10: HÓA TRỊ - Zaidap
-
Giải Bài 10.1, 10.2, 10.3, 10.4 Trang 14 Sách Bài Tập Hóa Học 8
-
Bài 10: Hóa Trị
-
[SBT Scan] Bài 10: Hóa Trị - Sách Bài Tập