Hoá Học 10 Bài 9: Sự Biến đổi Tuần Hoàn Tính Chất Của Các Nguyên ...
Có thể bạn quan tâm
Nội dung bài học Sự biến đổi tuần hoàn tính chất của các nguyên tố hóa học và Định luật tuần hoàn tìm hiểu Thế nào là tính kim loại, tính phi kim của các nguyên tố hóa học? Sự biến đổi tuần hoàn tính kim loại, tính phi kim? Khái niệm độ âm điện và sự biến đổi tuần hoàn độ âm điện. Sự biến đổi tuần hoàn hóa trị cao nhất đối với oxi của nguyên tố trong oxit và hóa trị cao nhất trong hợp chất khí đối với hiđro. Sự biến đổi tính chất oxit và hiđroxit của các nguyên tố nhóm A. Hiểu được định luật tuần hoàn.
ATNETWORK YOMEDIA1. Tóm tắt lý thuyết
1.1. Tính kim loại, tính phi kim
1.2. Hóa trị của các nguyên tố
1.3. Oxit và hiđroxit của các nguyên tố nhóm A
1.4. Định luật tuần hoàn
2. Bài tập minh hoạ
3. Luyện tập Bài 9 Hóa học 10
3.1. Trắc nghiệm
3.2. Bài tập SGK và Nâng cao
4. Hỏi đáp về Bài 9 Chương 2 Hóa học 10

Tóm tắt lý thuyết
1.1. Tính kim loại, tính phi kim
- Kim loại là những nguyên tố dễ mất electron để trở thành ion dương
- Phi kim là những nguyên tố dễ nhận electron để trở thành ion âm.
-
Kim loại càng mạnh khi khả năng mất electron càng lớn.
-
Phi kim càng mạnh khi khả năng nhận electron càng lớn.
1.1.1. Sự biến đổi tính chất trong một chu kì
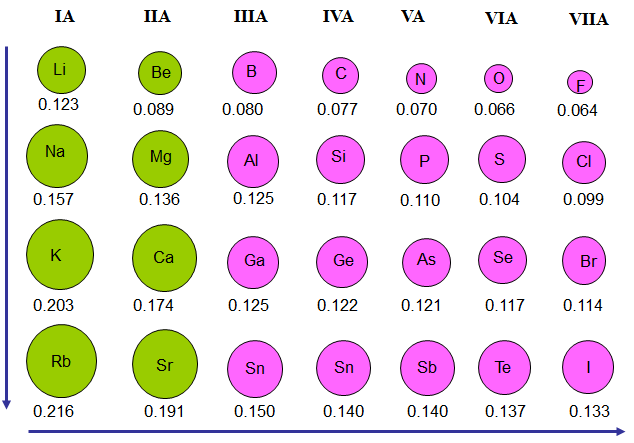
Hình 1: Bán kính nguyên tử của một số nguyên tố
Trong mỗi chu kì, bán kính nguyên tử giảm từ trái qua phải
Trong mỗi nhóm A, bán kính nguyên tử tăng từ trên xuống dưới
- Trong chu kì tính kim loại giảm dần, tính phi kim tăng dần.
-
Theo chiều tăng dần của điện tích hạt nhân thì điện tích hạt nhân tăng dần, số lớp electron không đổi, lực hút giữa hạt nhân và electron lớp ngoài cùng tăng, làm cho bán kính nguyên tử giảm khả năng mất electron giảm, khả năng nhận electron tăng.
1.1.2. Sự biến đổi tính chất trong một nhóm A
-
Tính kim loại tăng dần, tính phi kim giảm dần.
-
Theo chiều tăng dần của điện tích hạt nhân trong nhóm A, số lớp electron tăng dần, làm cho bán kính nguyên tử tăng, lực hút giữa hạt nhân và electron lớp ngoài cùng giảm, khả năng mất electron tăng, khả năng nhận electron giảm.
-
Trong nhóm A theo chiều tăng dần của điện tích hạt nhân, tính kim loại của các nguyên tố tăng dần đồng thời tính phi kim giảm dần.
1.1.3. Độ âm điện
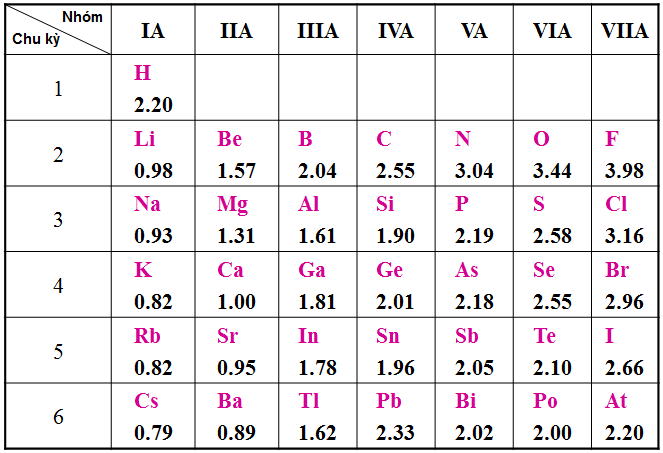
Hình 2: Giá trị Độ âm điện của một số nguyên tố nhóm A trong Bảng tuần hoàn theo Pau-linh
-
Độ âm điện của một nguyên tử càng lớn thì tính phi kim của nó càng mạnh và ngược lại.
-
Trong chu kì theo chiều tăng dần của điện tích hạt nhân giá trị độ âm điện tăng dần.
-
Trong nhóm A theo chiều tăng dần của diện tích hạt nhân, giá trị độ âm điện giảm dần.
-
Sự biến đổi giá trị độ âm điện và tính kim loại, tính phi kim phù hợp với nhau.
-
Độ âm điện của một nguyên tố càng lớn thì tính phi kim càng mạnh, tính kim loại càng giảm và ngược lại.
1.2. Hóa trị của các nguyên tố
-
Trong chu kì 3 đi từ đi từ trái sang phải, hóa trị cao nhất của các nguyên tố đối với oxi tăng từ 1 đến 7 còn hóa trị trong hợp chất khí đối với hiđro giảm từ 4 đến 1
-
Trong chu kì hóa trị cao nhất của các nguyên tố đối với oxi tăng dần và hiđro giảm dần.
| Nhóm | I A | II A | III A | IV A | V A | VI A | VII A |
| Hợp chất với Oxi | Na2O R2O | MgO RO | Al2O3 R2O3 | SiO2 RO2 | P2O5 R2O5 | SO3 RO3 | Cl2O7 R2O7 |
| Hóa trị cao nhất với Oxi | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| Nhóm | I A | II A | III A | IV A | V A | VI A | VII A |
| Hợp chất với Hiidro | SiH4 RH4 | PH3 RH3 | H2S R2S | HCl HX | |||
| Hóa trị với Hidro | 4 | 3 | 2 | 1 |
1.3. Oxit và hiđroxit của các nguyên tố nhóm A
Tính bazơ của các oxit và hiđroxit giảm dần đồng thời tính axit của nó mạnh dần.
Na2O + H2O → 2NaOH
Cl2O7 + H2O \(\leftrightarrows\) 2HClO4
1.4. Định luật tuần hoàn
Tính chất của các nguyên tố và đơn chất cũng như thành phần và tính chất của các hợp chất tạo nên từ các nguyên tố đó biến đổi tuần hoàn theo chiều tăng dần của điện tích hạt nhân nguyên tử.
Bài tập minh họa
Bài 1:
Viết cấu hình electron của nguyên tử Mg (Z=12). Để đạt cấu hình electron của nguyên tử khí hiếm gần nhất trong bảng tuần hoàn, nguyên tử Mg nhận hay nhường bao nhiêu eletron? Magie thể hiện tính kim loại hay phi kim?
Hướng dẫn:
Cấu hình e của nguyên tử Mg (Z= 12) : 1s22s22p63s2
Do chỉ có 2e ở lớp ngoài cùng, để đạt cấu hình electron của nguyên tử khí hiếm gần nhất trong bảng tuần hoàn, nguyên tử Mg có xu hướng nhường 2e. Mg thể hiện tính kim loại.Mg → Mg2+ + 2e
(2, 8, 2) (2, 8)
3. Luyện tập Bài 9 Hóa học 10
Sau bài học cần nắm:
- Thế nào là tính kim loại, tính phi kim của các nguyên tố hóa học?
- Sự biến đổi tuần hoàn tính kim loại, tính phi kim? Khái niệm độ âm điện và sự biến đổi tuần hoàn độ âm điện.
- Sự biến đổi tuần hoàn hóa trị cao nhất đối với oxi của nguyên tố trong oxit và hóa trị cao nhất trong hợp chất khí đối với hiđro.
- Sự biến đổi tính chất oxit và hiđroxit của các nguyên tố nhóm A. Hiểu được định luật tuần hoàn.
3.1. Trắc nghiệm
Bài kiểm tra Trắc nghiệm Hóa học 10 Bài 9 có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
-
Câu 1:
Trong một chu kì, bán kính nguyên tử các nguyên tố
- A. Tăng theo chiều tăng dần của điện tích hạt nhân.
- B. Giảm theo chiều tăng của điện tích hạt nhân.
- C. Giảm theo chiều tăng của tính phi kim.
- D. B và C đều đúng.
-
Câu 2:
Trong một nhóm A, bán kính nguyên tử của các nguyên tố:
- A. Tăng theo chiều tăng của điện tích hạt nhân.
- B. Giảm theo chiều tăng của điện tích hạt nhân.
- C. Giảm theo chiều giảm của tính kim loại.
- D. A và C đều đúng
-
Câu 3:
Các nguyên tố halogen được xắp xếp theo chiều bán kính nguyên tử giảm dần (từ trái sang phải) như sau :
- A. I, Br, Cl, F.
- B. I, Br, F, Cl.
- C. F, Cl, Br, I.
- D. Br, I, Cl, F.
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
3.2. Bài tập SGK và Nâng cao
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 10 Bài 9.
Bài tập 1 trang 47 SGK Hóa học 10
Bài tập 2 trang 47 SGK Hóa học 10
Bài tập 3 trang 47 SGK Hóa học 10
Bài tập 4 trang 47 SGK Hóa học 10
Bài tập 5 trang 48 SGK Hóa học 10
Bài tập 6 trang 48 SGK Hóa học 10
Bài tập 7 trang 48 SGK Hóa học 10
Bài tập 8 trang 48 SGK Hóa học 10
Bài tập 9 trang 48 SGK Hóa học 10
Bài tập 9.1 trang 21 SBT Hóa học 10
Bài tập 9.2 trang 21 SBT Hóa học 10
Bài tập 9.3 trang 21 SBT Hóa học 10
Bài tập 9.4 trang 21 SBT Hóa học 10
Bài tập 9.5 trang 21 SBT Hóa học 10
Bài tập 9.6 trang 22 SBT Hóa học 10
Bài tập 9.7 trang 22 SBT Hóa học 10
Bài tập 9.8 trang 22 SBT Hóa học 10
Bài tập 9.9 trang 22 SBT Hóa học 10
Bài tập 9.10 trang 22 SBT Hóa học 10
Bài tập 9.11 trang 23 SBT Hóa học 10
Bài tập 9.12 trang 23 SBT Hóa học 10
Bài tập 9.13 trang 23 SBT Hóa học 10
Bài tập 9.14 trang 23 SBT Hóa học 10
Bài tập 9.15 trang 23 SBT Hóa học 10
Bài tập 9.16 trang 23 SBT Hóa học 10
Bài tập 9.17 trang 24 SBT Hóa học 10
Bài tập 9.18 trang 24 SBT Hóa học 10
Bài tập 9.19 trang 24 SBT Hóa học 10
Bài tập 9.20 trang 24 SBT Hóa học 10
Bài tập 9.21 trang 24 SBT Hóa học 10
Bài tập 9.22 trang 24 SBT Hóa học 10
Bài tập 1 trang 49 SGK Hóa học 10 nâng cao
Bài tập 2 trang 49 SGK Hóa học 10 nâng cao
Bài tập 3 trang 49 SGK Hóa học 10 nâng cao
Bài tập 4 trang 49 SGK Hóa học 10 nâng cao
Bài tập 5 trang 49 SGK Hóa học 10 nâng cao
Bài tập 6 trang 49 SGK Hóa học 10 nâng cao
Bài tập 7 trang 49 SGK Hóa học 10 nâng cao
Bài tập 1 trang 55 SGK Hóa học 10 nâng cao
Bài tập 2 trang 55 SGK Hóa học 10 nâng cao
Bài tập 3 trang 55 SGK Hóa học 10 nâng cao
Bài tập 4 trang 55 SGK Hóa học 10 nâng cao
Bài tập 5 trang 55 SGK Hóa học 10 nâng cao
Bài tập 6 trang 55 SGK Hóa học 10 nâng cao
Bài tập 7 trang 55 SGK Hóa học 10 nâng cao
4. Hỏi đáp về Bài 9 Chương 2 Hóa học 10
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa HOC247 thảo luận và trả lời nhé.
 NONE
NONE Bài học cùng chương
 Hoá học 10 Bài 7: Bảng tuần hoàn các nguyên tố hóa học
Hoá học 10 Bài 7: Bảng tuần hoàn các nguyên tố hóa học  Hoá học 10 Bài 8: Sự biến đổi tuần hoàn cấu hình electron nguyên tử của các nguyên tố hóa học
Hoá học 10 Bài 8: Sự biến đổi tuần hoàn cấu hình electron nguyên tử của các nguyên tố hóa học  Hoá học 10 Bài 10: Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
Hoá học 10 Bài 10: Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học  Hoá học 10 Bài 11: Luyện tập Bảng tuần hoàn, sự biến đổi tuần hoàn cấu hình electron nguyên tử và tính chất của các nguyên tố hóa học ADSENSE TRACNGHIEM
Hoá học 10 Bài 11: Luyện tập Bảng tuần hoàn, sự biến đổi tuần hoàn cấu hình electron nguyên tử và tính chất của các nguyên tố hóa học ADSENSE TRACNGHIEM  Bộ đề thi nổi bật
Bộ đề thi nổi bật  UREKA AANETWORK
UREKA AANETWORK 
XEM NHANH CHƯƠNG TRÌNH LỚP 10
Toán 10
Toán 10 Kết Nối Tri Thức
Toán 10 Chân Trời Sáng Tạo
Toán 10 Cánh Diều
Giải bài tập Toán 10 Kết Nối Tri Thức
Giải bài tập Toán 10 CTST
Giải bài tập Toán 10 Cánh Diều
Trắc nghiệm Toán 10
Ngữ văn 10
Ngữ Văn 10 Kết Nối Tri Thức
Ngữ Văn 10 Chân Trời Sáng Tạo
Ngữ Văn 10 Cánh Diều
Soạn Văn 10 Kết Nối Tri Thức
Soạn Văn 10 Chân Trời Sáng tạo
Soạn Văn 10 Cánh Diều
Văn mẫu 10
Tiếng Anh 10
Giải Tiếng Anh 10 Kết Nối Tri Thức
Giải Tiếng Anh 10 CTST
Giải Tiếng Anh 10 Cánh Diều
Trắc nghiệm Tiếng Anh 10 KNTT
Trắc nghiệm Tiếng Anh 10 CTST
Trắc nghiệm Tiếng Anh 10 CD
Giải Sách bài tập Tiếng Anh 10
Vật lý 10
Vật lý 10 Kết Nối Tri Thức
Vật lý 10 Chân Trời Sáng Tạo
Vật lý 10 Cánh Diều
Giải bài tập Lý 10 Kết Nối Tri Thức
Giải bài tập Lý 10 CTST
Giải bài tập Lý 10 Cánh Diều
Trắc nghiệm Vật Lý 10
Hoá học 10
Hóa học 10 Kết Nối Tri Thức
Hóa học 10 Chân Trời Sáng Tạo
Hóa học 10 Cánh Diều
Giải bài tập Hóa 10 Kết Nối Tri Thức
Giải bài tập Hóa 10 CTST
Giải bài tập Hóa 10 Cánh Diều
Trắc nghiệm Hóa 10
Sinh học 10
Sinh học 10 Kết Nối Tri Thức
Sinh học 10 Chân Trời Sáng Tạo
Sinh học 10 Cánh Diều
Giải bài tập Sinh 10 Kết Nối Tri Thức
Giải bài tập Sinh 10 CTST
Giải bài tập Sinh 10 Cánh Diều
Trắc nghiệm Sinh học 10
Lịch sử 10
Lịch Sử 10 Kết Nối Tri Thức
Lịch Sử 10 Chân Trời Sáng Tạo
Lịch Sử 10 Cánh Diều
Giải bài tập Lịch Sử 10 KNTT
Giải bài tập Lịch Sử 10 CTST
Giải bài tập Lịch Sử 10 Cánh Diều
Trắc nghiệm Lịch sử 10
Địa lý 10
Địa Lý 10 Kết Nối Tri Thức
Địa Lý 10 Chân Trời Sáng Tạo
Địa Lý 10 Cánh Diều
Giải bài tập Địa Lý 10 KNTT
Giải bài tập Địa Lý 10 CTST
Giải bài tập Địa Lý 10 Cánh Diều
Trắc nghiệm Địa lý 10
GDKT & PL 10
GDKT & PL 10 Kết Nối Tri Thức
GDKT & PL 10 Chân Trời Sáng Tạo
GDKT & PL 10 Cánh Diều
Giải bài tập GDKT & PL 10 KNTT
Giải bài tập GDKT & PL 10 CTST
Giải bài tập GDKT & PL 10 CD
Trắc nghiệm GDKT & PL 10
Công nghệ 10
Công nghệ 10 Kết Nối Tri Thức
Công nghệ 10 Chân Trời Sáng Tạo
Công nghệ 10 Cánh Diều
Giải bài tập Công nghệ 10 KNTT
Giải bài tập Công nghệ 10 CTST
Giải bài tập Công nghệ 10 CD
Trắc nghiệm Công nghệ 10
Tin học 10
Tin học 10 Kết Nối Tri Thức
Tin học 10 Chân Trời Sáng Tạo
Tin học 10 Cánh Diều
Giải bài tập Tin học 10 KNTT
Giải bài tập Tin học 10 CTST
Giải bài tập Tin học 10 Cánh Diều
Trắc nghiệm Tin học 10
Cộng đồng
Hỏi đáp lớp 10
Tư liệu lớp 10
Xem nhiều nhất tuần
Đề thi giữa HK2 lớp 10
Đề thi giữa HK1 lớp 10
Đề thi HK1 lớp 10
Đề thi HK2 lớp 10
Video bồi dưỡng HSG môn Toán
Toán 10 Chân trời sáng tạo Bài 2: Tập hợp
Toán 10 Kết nối tri thức Bài 1: Mệnh đề
Toán 10 Cánh Diều Bài tập cuối chương 1
Soạn bài Chữ người tử tù - Nguyễn Tuân - Ngữ văn 10 KNTT
Soạn bài Thần Trụ Trời - Ngữ văn 10 CTST
Soạn bài Ra-ma buộc tội - Ngữ văn 10 Tập 1 Cánh Diều
Văn mẫu về Bình Ngô đại cáo
Văn mẫu về Chữ người tử tù
Văn mẫu về Tây Tiến
Văn mẫu về Cảm xúc mùa thu (Thu hứng)
YOMEDIA YOMEDIA ×Thông báo
Bạn vui lòng đăng nhập trước khi sử dụng chức năng này.
Bỏ qua Đăng nhập ×Thông báo
Bạn vui lòng đăng nhập trước khi sử dụng chức năng này.
Đồng ý ATNETWORK ON QC Bỏ qua >>
QC Bỏ qua >> 
Từ khóa » Hoá Lớp 10 Bài 9
-
Giải Hóa 10 Bài 9: Sự Biến đổi Tuần Hoàn Tính Chất Của Các Nguyên ...
-
Giải Hóa 10 Bài 9: Sự Biến đổi Tuần Hoàn Tính Chất Của ...
-
Lý Thuyết Hóa 10: Bài 9. Sự Biến đổi Tuần Hoàn Tính Chất Của Các ...
-
Bài 9. Sự Biến đổi Tuần Hoàn Tính Chất Của Các Nguyên Tố Hóa Học ...
-
Bài 9 Trang 76 SGK Hóa Học 10
-
Giải Bài Tập Hóa 10 Bài 9: Sự Biến đổi Tuần Hoàn Tính Chất Của Các ...
-
Hóa Học Lớp 10 - Bài 9 - Sự Biến đổi Tuần Hoàn Tính Chất Của Các ...
-
Giải Bài Tập Hóa Học 10 - Bài 9: Sự Biến đổi Tuần Hoàn Tính Chất ...
-
Trắc Nghiệm Hóa Học 10 Bài 9: Sự Biến đổi Tuần Hoàn Tính Chất Của ...
-
Bài 9: Sự Biến đổi Tuần Hoàn Tính Chất Của Các Nguyên Tó Hóa Học
-
Giải Bài Tập Hóa 10 Bài 9 Sự Biến đổi Tuần Hoàn Tính Chất Của Các ...
-
Giải Bài 9 Hóa Học 10: Sự Biến đổi Tuần Hoàn Tính Chất Của Các ...
-
Bài 9 Trang 90 Sgk Hóa 10, Bài 9. Cân Bằng Các Phương Trình Phản ...
-
Soạn Hoá Học 10 Bài 9: Sự Biến đổi Tuần Hoàn Tính Chất Của Các ...