Hoá Học 11 Bài 1: Sự điện Li - HOC247
Có thể bạn quan tâm
Bài giảng đi vào tìm hiểu Sự điện li là gì? Chất điện li là gì? Rèn luyện khả năng quan sát thí nghiệm rút ra được kết luận về tính dẫn điện của dung dịch chất điện li, Phân biệt được chất điện li, chất không điện li, chất điện li mạnh, chất điện li yếu, Viết được phương trình điện li của chất điện li mạnh, chất điện li yếu.
ATNETWORK YOMEDIA1. Tóm tắt lý thuyết
1.1. Hiện tượng Điện li
1.2. Phân loại các chất điện li
2. Bài tập minh hoạ
3. Luyện tập Bài 1 Hóa học 11
3.1. Trắc nghiệm
3.2. Bài tập SGK và Nâng cao Chương 1 Bài 1
4. Hỏi đáp về Bài 1: Sự điện li

Tóm tắt lý thuyết
1.1. Hiện tượng Điện li
1.1.1. Thí nghiệm
- Trong SGK trình bày cách tiến hành thí nghiệm đồng loạt bằng nguồn điện và hóa chất là NaCl khan, NaOH khan, sacarozơ, nước cất, dd NaCl , dd NaOH , dd sacarozo, ancol etylic.
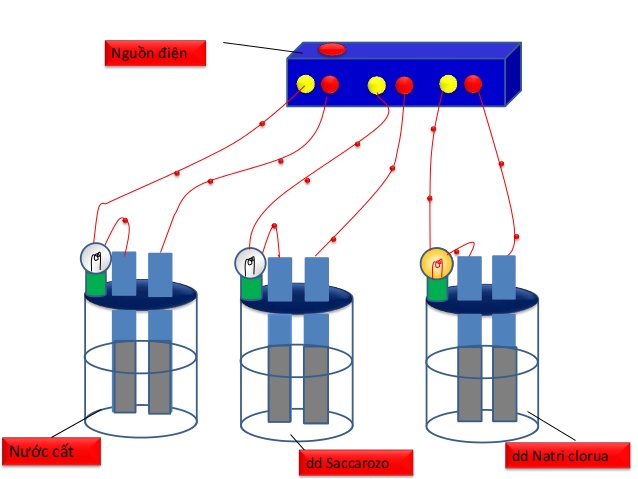
Hình 1: Bộ dụng cụ chứng minh sự dẫn điện của dung dịch
- Tuy nhiên, thí nghiệm này dụng cụ tiến hành thí nghiệm hơi rườm rà nên khi tiến hành cho học sinh quan sát, GV thường sử dụng thiết bị thử tính dẫn điện đơn giản như sau:
Video 1: Thí nghiệm Sự điện li
- Hiện tượng: Dd NaCl, HCl, NaOH, … làm đèn sáng. Dd saccarozơ, rượu etylic … không làm đèn phát sáng
- Giải thích: Cho dụng cụ thử tính dẫn điện vào lần lượt các cốc đựng các chất khác nhau. Bóng đèn phát sáng chứng tỏ chất đựng trong cốc đó có tính dẫn điện.
- Kết luận: Dung dịch Axit, bazơ và muối đều dẫn điện
1.1.2. Nguyên nhân tính dẫn điện của các dd axit, bazơ, muối trong nước.
- Các muối, axít, bazơ khi tan trong nước phân li ra các ion làm cho dd của chúng dẫn điện.
- Quá trình phân li các chất trong H2O ra ion là sự điện li.
- Những chất tan trong H2O phân li thành các ion gọi là chất điện li.
- Sự điện li được biểu diễn bằng pt điện li: NaCl → Na+ + Cl-
HCl → H+ + Cl-
NaOH → Na+ + OH-
1.2. Phân loại các chất điện li
1.2.1. Thí nghiệm
- Tiến hành thí nghiệm với chất điện li mạnh như dung dịch NaOH và chất điện li yếu như CH3COOH
Video 2: Tính dẫn điện của dung dịch chất điện li mạnh
Video 3: Tính dẫn điện của dung dịch chất điện li yếu
- Hiện tượng: Cả hai dung dịch đều làm bóng đèn phát sáng. Bóng đèn ở dung dịch axit axetic sáng mờ hơn ở dung dịch NaOH rất nhiều
- Giải thích: ở cùng nồng độ thì NaOH phân li ra ion nhiều hơn CH3COOH. Lượng ion càng nhiều thì tính dẫn điện càng tăng nên bóng đèn ở dung dịch NaOH sáng hơn.
- Nhận xét: Dựa vào mức độ phân li thành ion của các chất điện li khác nhau, người ta chia thành chất điện mạnh và chất điện li yếu.
1.2.2. Chất điện li mạnh, chất điện li yếu
*Chất điện li mạnh:
- Khái niệm: Chất điện li mạnh là chất khi tan trong nước, các phân tử hoà tan đều phân li ra ion.
- Phương trình điện li NaCl: (chú ý sử dụng mũi tên một chiều)
NaCl → Na+ + Cl-
100 ptử → 100 ion Na+ và 100 ion Cl-
- Bao gồm:
- Các axít mạnh HCl, HNO3, H2SO4…
- Các bazơ mạnh:NaOH, KOH, Ba(OH)2
- Hầu hết các muối.
- Ví dụ: Tính nồng độ của ion Na+ và SO42- trong dung dịch muối Na2SO4 0,1M
Dung dịch muối Na2SO4 là dung dịch chất điện li mạnh nên ta có phương trình ion như sau:
Na2SO4 → 2Na+ + SO42-
0,1M→ 0,2M → 0,1 M
Vậy nồng độ của ion Na+ là 0,2M; của ion SO42- là 0,1M
*Chất điện li yếu:
- Khái niệm: Chất điện li yếu là chất khi tan trong nước, chỉ có 1 phần số phân tử hoà tan phân li ra ion, phần còn lại vẫn tồn tại dưới dạng phân tử trong dung dịch.
- Phương trình điện li: (chú ý sử dụng 2 mũi tên ngược chiều nhau)
CH3COOH \(\leftrightarrows\) CH3COO- + H+
Ví dụ trong dung dịch CH3COOH cứ 100 phân tử hòa tan thì có 2 phân tử phân li thành ion, 98 phân tử còn lại không phân li.
- Ví dụ:
- Các axít yếu: H2S, HClO, CH3COOH, HF, H2SO3, HNO2, H3PO4, H2CO3, ...
- Bazơ yếu: Mg(OH)2, Bi(OH)3...
- Lưu ý: Quá trình phân li của chất điện li yếu là quá trình cân bằng động, tuân theo nguyên lí Lơ Satơliê.
Bài tập minh họa
Bài 1:
Xác định chất điện li mạnh, điện li yếu và viết phương trình điện li của các chất sau: HNO3, Mg(OH)2, Ba(OH)2, HCl, H2SO4, H2S
Hướng dẫn:
- Chất điện li mạnh là: HNO3, Ba(OH)2, HCl, H2SO4
HNO3 → H+ + NO3-
Ba(OH)2 → Ba2+ + 2OH-
HCl → H+ + Cl-
H2SO4 → 2H+ + SO42-
- Chất điện li yếu là: Mg(OH)2, H2S
Mg(OH)2 là bazơ ở dạng kết tủa nên phân li yếu. Mg(OH)2 \(\leftrightarrows\) Mg2+ + 2OH-
H2S là axit yếu nên phân li cũng yếu theo 2 nấc như sau:
H2S \(\leftrightarrows\) H+ + HS-
HS-\(\leftrightarrows\) H+ + S2-
Bài 2:
Tính nồng độ các ion trong các dung dịch sau
a. dd NaOH 0,1M b. dd BaCl2 0,2 M c. dd Ba(OH)2 0,1M
Hướng dẫn:
a. Phương trình điện li:
NaOH → Na+ + OH-
0,1M → 0,1M → 0,1 M
Vậy nồng độ của ion Na+ và OH- đều là 0,1 M
b. Phương trình điện li:
BaCl2 → Ba2+ + 2Cl-
0,1 M → 0,1 M → 0,2 M
Vậy nồng độ của ion Ba2+ là 0,1M và ion Cl- là 0,2M
c. Phương trình điện li:
Ba(OH)2 → Ba2+ + 2OH-
0,1M → 0,1M → 0,2 M
Bài 3:
Một dung dịch chứa 0,02 mol Cu2+, 0,03 mol K+, x mol Cl- và y mol SO42-. Tổng khối lượng muối tan có trong dung dịch là 5,435 gam. Xác định giá trị của x và y
Hướng dẫn:
Các ion trong dịch tồn tại cùng nhau vì ghép các ion không tạo kết tủa.
Áp dụng định luật bảo toàn điện tích ta có:
(1) 0,02.2 + 0,03.1 = x + 2y
Áp dụng định luật bảo toàn khối lượng thành phần ta có:
(2) 0,02.64 + 0,03.39 + 35,5x + 96.y = 5,435
Kết hợp (1) và (2) ta có hệ phương trình:
\(\left\{ \begin{array}{l} x + 2y = 0,07\\ 35,5x + 96y = 2,985 \end{array} \right. \Rightarrow \left\{ \begin{array}{l} x = 0,03(mol)\\ y = 0,02(mol) \end{array} \right.\)
Vậy số mol của ion Cl- là 0,03 mol; số mol của ion SO42- là 0,02 mol
3. Luyện tập Bài 1 Hóa học 11
Sau bài học cần nắm:
- Rèn luyện khả năng quan sát thí nghiệm rút ra được kết luận về tính dẫn điện của dung dịch chất điện li
- Phân biệt được chất điện li, chất không điện li, chất điện li mạnh, chất điện li yếu
- Viết được phương trình điện li của chất điện li mạnh, chất điện li yếu.
3.1. Trắc nghiệm
Bài kiểm tra Trắc nghiệm Hóa học 11 Bài 1 có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
-
Câu 1:
Dung dịch chất điện li dẫn điện được là do trong dd có chứa:
- A. Các electron chuyển động tự do.
- B. Các cation và anion chuyển động tự do.
- C. Các ion H+ và OH- chuyển động tự do.
- D. Các ion được gắn cố định tại các nút mạng.
-
Câu 2:
Chất nào sau đây không dẫn điện?
- A. KCl rắn, khan.
- B. CaCl2 nóng chảy.
- C. NaOH nóng chảy.
- D. HBr hòa tan trong nước.
-
Câu 3:
Câu nào sau đây đúng khi nói về sự điện li?
- A. Sự điện li là sự hoà tan một chất vào nước thành dung dịch.
- B. Sự điện li là sự phân li một chất dưới tác dụng của dòng điện.
- C. Sự điện li là sự phân li một chất thành ion khi tan trong nước hay ở trạng thái nóng chảy.
- D. Sự điện li là quá trình oxi hoá - khử.
-
Câu 4:
Cho dãy các chất: KAl(SO4)2.12H2O, C2H5OH, C12H22O11 (saccarozơ), SO2, CH3COOH, N2O5, CuO, Ca(OH)2, CH3COONH4. Số chất điện li là
- A. 3.
- B. 4.
- C. 5.
- D. 2.
-
Câu 5:
Trong dung dịch axit axetic (CH3COOH) có những phần tử nào sau đây:
- A. H+, CH3COO- .
- B. CH3COOH, H+, CH3COO-, H2O.
- C. H+, CH3COO-, H2O.
- D. CH3COOH, CH3COO-, H+.
-
Câu 6:
Trong các chất sau: K3PO4, H2SO4, HClO, HNO2, NH4Cl, HgCl2, Sn(OH)2. Các chất điện li yếu là:
- A. HClO, HNO2, HgCl2, Sn(OH)2.
- B. HClO, HNO2, K3PO4, H2SO4.
- C. HgCl2, Sn(OH)2, NH4Cl, HNO2.
- D. HgCl2, Sn(OH)2, HNO2, H2SO4.
-
Câu 7:
Chọn dãy các chất điện ly mạnh trong số các chất sau :
a. NaCl. b. Ba(OH)2. c. HNO3. d. HgCl2. e. Cu(OH)2. f. MgSO4.
- A. a, b, c, f.
- B. a, d, e, f.
- C. b, c, d, e.
- D. a, b, c, e.
Câu 8-20: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
3.2. Bài tập SGK và Nâng cao Chương 1 Bài 1
Bài tập 1 trang 7 SGK Hóa học 11
Bài tập 2 trang 7 SGK Hóa học 11
Bài tập 3 trang 7 SGK Hóa học 11
Bài tập 4 trang 7 SGK Hóa học 11
Bài tập 5 trang 7 SGK Hóa học 11
Bài tập 1.1 trang 3 SBT Hóa học 11
Bài tập 1.2 trang 3 SBT Hóa học 11
Bài tập 1.3 trang 3 SBT Hóa học 11
Bài tập 1.4 trang 3 SBT Hóa học 11
Bài tập 1.5 trang 3 SBT Hóa học 11
Bài tập 1.6 trang 3 SBT Hóa học 11
Bài tập 1.7 trang 4 SBT Hóa học 11
Bài tập 1 trang 7 SGK Hóa học 11 nâng cao
Bài tập 2 trang 7 SGK Hóa học 11 nâng cao
Bài tập 3 trang 7 SGK Hóa học 11 nâng cao
Bài tập 4 trang 7 SGK Hóa học 11 nâng cao
Bài tập 5 trang 7 SGK Hóa học 11 nâng cao
Bài tập 6 trang 7 SGK Hóa học 11 nâng cao
Bài tập 7 trang 7 SGK Hóa học 11 nâng cao
4. Hỏi đáp về Bài 1: Sự điện li
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa HOC247 thảo luận và trả lời nhé.
 NONE
NONE Bài học cùng chương
 Hoá học 11 Bài 2: Axit, bazơ và muối
Hoá học 11 Bài 2: Axit, bazơ và muối  Hoá học 11 Bài 3: Sự điện li của nước - pH và Chất chỉ thị axit-bazơ
Hoá học 11 Bài 3: Sự điện li của nước - pH và Chất chỉ thị axit-bazơ  Hoá học 11 Bài 4: Phản ứng trao đổi ion trong dung dịch các chất điện li
Hoá học 11 Bài 4: Phản ứng trao đổi ion trong dung dịch các chất điện li  Hoá học 11 Bài 5: Luyện tập Axit, bazơ và muối và Phản ứng trao đổi ion trong dung dịch các chất điện li
Hoá học 11 Bài 5: Luyện tập Axit, bazơ và muối và Phản ứng trao đổi ion trong dung dịch các chất điện li  Hoá học 11 Bài 6: Bài thực hành 1 Tính axit-bazơ và Phản ứng trao đổi ion trong dung dịch các chất điện li ADSENSE TRACNGHIEM
Hoá học 11 Bài 6: Bài thực hành 1 Tính axit-bazơ và Phản ứng trao đổi ion trong dung dịch các chất điện li ADSENSE TRACNGHIEM  Bộ đề thi nổi bật
Bộ đề thi nổi bật  UREKA AANETWORK
UREKA AANETWORK 
XEM NHANH CHƯƠNG TRÌNH LỚP 11
Toán 11
Toán 11 Kết Nối Tri Thức
Toán 11 Chân Trời Sáng Tạo
Toán 11 Cánh Diều
Giải bài tập Toán 11 KNTT
Giải bài tập Toán 11 CTST
Trắc nghiệm Toán 11
Ngữ văn 11
Ngữ Văn 11 Kết Nối Tri Thức
Ngữ Văn 11 Chân Trời Sáng Tạo
Ngữ Văn 11 Cánh Diều
Soạn Văn 11 Kết Nối Tri Thức
Soạn Văn 11 Chân Trời Sáng Tạo
Văn mẫu 11
Tiếng Anh 11
Tiếng Anh 11 Kết Nối Tri Thức
Tiếng Anh 11 Chân Trời Sáng Tạo
Tiếng Anh 11 Cánh Diều
Trắc nghiệm Tiếng Anh 11 KNTT
Trắc nghiệm Tiếng Anh 11 CTST
Tài liệu Tiếng Anh 11
Vật lý 11
Vật lý 11 Kết Nối Tri Thức
Vật Lý 11 Chân Trời Sáng Tạo
Vật lý 11 Cánh Diều
Giải bài tập Vật Lý 11 KNTT
Giải bài tập Vật Lý 11 CTST
Trắc nghiệm Vật Lý 11
Hoá học 11
Hoá học 11 Kết Nối Tri Thức
Hoá học 11 Chân Trời Sáng Tạo
Hoá Học 11 Cánh Diều
Giải bài tập Hoá 11 KNTT
Giải bài tập Hoá 11 CTST
Trắc nghiệm Hoá học 11
Sinh học 11
Sinh học 11 Kết Nối Tri Thức
Sinh Học 11 Chân Trời Sáng Tạo
Sinh Học 11 Cánh Diều
Giải bài tập Sinh học 11 KNTT
Giải bài tập Sinh học 11 CTST
Trắc nghiệm Sinh học 11
Lịch sử 11
Lịch Sử 11 Kết Nối Tri Thức
Lịch Sử 11 Chân Trời Sáng Tạo
Giải bài tập Sử 11 KNTT
Giải bài tập Sử 11 CTST
Trắc nghiệm Lịch Sử 11
Địa lý 11
Địa Lý 11 Kết Nối Tri Thức
Địa Lý 11 Chân Trời Sáng Tạo
Giải bài tập Địa 11 KNTT
Giải bài tập Địa 11 CTST
Trắc nghiệm Địa lý 11
GDKT & PL 11
GDKT & PL 11 Kết Nối Tri Thức
GDKT & PL 11 Chân Trời Sáng Tạo
Giải bài tập KTPL 11 KNTT
Giải bài tập KTPL 11 CTST
Trắc nghiệm GDKT & PL 11
Công nghệ 11
Công nghệ 11 Kết Nối Tri Thức
Công nghệ 11 Cánh Diều
Giải bài tập Công nghệ 11 KNTT
Giải bài tập Công nghệ 11 Cánh Diều
Trắc nghiệm Công nghệ 11
Tin học 11
Tin học 11 Kết Nối Tri Thức
Tin học 11 Cánh Diều
Giải bài tập Tin học 11 KNTT
Giải bài tập Tin học 11 Cánh Diều
Trắc nghiệm Tin học 11
Cộng đồng
Hỏi đáp lớp 11
Tư liệu lớp 11
Xem nhiều nhất tuần
Đề thi HK1 lớp 11
Đề thi HK2 lớp 12
Đề thi giữa HK1 lớp 11
Đề thi giữa HK2 lớp 11
Video bồi dưỡng HSG môn Toán
Công nghệ 11 Bài 16: Công nghệ chế tạo phôi
Đây thôn Vĩ Dạ
Từ ấy
Cấp số nhân
Văn mẫu và dàn bài hay về bài thơ Đây thôn Vĩ Dạ
Cấp số cộng
YOMEDIA YOMEDIA ×Thông báo
Bạn vui lòng đăng nhập trước khi sử dụng chức năng này.
Bỏ qua Đăng nhập ×Thông báo
Bạn vui lòng đăng nhập trước khi sử dụng chức năng này.
Đồng ý ATNETWORK ON QC Bỏ qua >>
QC Bỏ qua >> 
Từ khóa » Chất điện Li Là Gì Lớp 11
-
Sự điện Li Hóa 11 - Lý Thuyết Và Một Số Dạng Bài Tập
-
Lý Thuyết Về Sự điện Li. | SGK Hóa Lớp 11
-
Sự điện Li, Chất điện Li Là Gì
-
Sự điện Li, Chất điện Li Là Gì?
-
Các Dạng Bài Tập Hoá 11 Chương Sự Điện Li Cần Nắm Vững
-
Sự điện Li Là Gì, Phân Loại Chất điện Ly Mạnh Và Chất điện Li Yếu
-
Bài 2 Trang 7 SGK Hóa Học 11. Sự điện Li, Chất điện Li Là Gì
-
Lý Thuyết Hóa 11: Bài 1. Sự điện Li - Toploigiai
-
Bài 2 Trang 7 Sgk Hóa 11, Sự điện Li, Chất điện Li Là Gì ?
-
Giải Bài 1: Sự điện Li | Hoá Học 11
-
Sự điện Li - Hóa Học Lớp 11 - Baitap123
-
Câu 1 Trang 10 SGK Hóa Học 11 Nâng Cao, Độ điện Li Là Gì ? Thế ...
-
Sự điện Li
-
Sự điện Li, Chất điện Li Là Gì - Giải Bài Tập Hóa Học Lớp 11