Hoá Học 12 Bài 31: Sắt
Có thể bạn quan tâm
Nội dung bài học trình bày cụ thể, tỉ mỉ về nguyên tố rất phố biến trong đời sống và sản xuất chính là Sắt. Thông qua bài học các em học sinh biết được vị trí của Sắt trong Bảng hệ thống tuần hoàn các nguyên tố hóa học; cấu tạo nguyên tử, tính chất vật lí - hóa học và phương pháp điều chế. Biết được tính chất và ứng dụng của một số hợp chất quan trọng của Sắt.
ATNETWORK YOMEDIA1. Video bài giảng
2. Tóm tắt lý thuyết
2.1. Vị trí trong Bảng tuần hoàn, cấu hình e nguyên tử
2.2. Tính chất vật lí
2.3. Tính chất hóa học
2.4. Ứng dụng
3. Bài tập minh hoạ
3.1. Bài tập Cơ bản
3.2. Bài tập Nâng cao
4. Luyện tập bài 31 Hóa học 12
4.1. Trắc nghiệm
4.2. Bài tập SGK & Nâng cao
5. Hỏi đáp về Bài 31 Chương 7 Hoá học 12

Tóm tắt lý thuyết
2.1. Vị trí trong Bảng tuần hoàn, cấu hình electron nguyên tử
- Cấu hình electron: 1s22s22p63s23p63d64s2 hay [Ar]3d64s2
- Ô thứ 26, nhóm VIIIB, chu kì 4
- Sắt dễ nhường 2 electron ở phân lớp 4s trở thành ion Fe2+ và có thể nhường thêm 1 electron ở phân lớp 3d để trở thành ion Fe3+.
2.2. Tính chất vật lí
Quan sát Con cá Sắt giúp ngăn ngừa bệnh thiếu máu

- Sắt là kim loại màu trắng hơi xám
- Có khối lượng riêng lớn (d = 8,9 g/cm3), nóng chảy ở 15400C.
- Sắt có tính dẫn điện, dẫn nhiệt tốt và có tính nhiễm từ.
2.3. Tính chất hóa học
- Là kim loại có tính khử trung bình.
- Với chất oxi hoá yếu: Fe → Fe2+ + 2e
- Với chất oxi hoá mạnh: Fe → Fe3+ + 3e
a. Tác dụng với Phi kim
Thí nghiệm: Sắt phản ứng với Lưu huỳnh: \(Fe+S\overset{t^{0}}{\rightarrow}FeS\)
Thí nghiệm: Sắt cháy trong Oxi: \(Fe+O_{2}\overset{t^{0}}{\rightarrow}Fe_{3}O_{4}\)
Thí nghiệm: Sắt tác dụng với Clo: \(2Fe+3Cl_{2}\overset{t^{0}}{\rightarrow}2FeCl_{3}\)
b. Tác dụng với axit
- Với dung dịch HCl, H2SO4 loãng: Fe đưa về sắt (II), H+ chuyển thành H2
Thí nghiệm của Sắt trong dung dịch sunfuric loãng: \(Fe + H_{2}SO_{4}\rightarrow FeSO_{4}+H_{2}\uparrow\)
- Với dung dịch HNO3 và H2SO4 đặc, nóng: Fe khử \(N^{+5}\) hoặc \(S^{+6}\) trong HNO3 hoặc H2SO4 đặc, nóng đến số oxi hoá thấp hơn, còn Fe bị oxi hoá thành \(Fe^{3+}\).
Thí nghiệm: Sắt trong dung dịch HNO3 loãng: \(Fe+4HNO_{3}\rightarrow Fe(NO_{3})_{3}+NO\uparrow+2H_{2}O\)
Lưu ý: Fe bị thụ động bởi các axit HNO3 đặc, nguội hoặc H2SO4 đặc, nguội.
c. Tác dụng với dung dịch muối
- Sắt có thể khử được các ion của các kim loại đứng sau nó trong dãy điện hóa.
Thí nghiệm: Sắt phản ứng với dung dịch Đồng(II) sunfat \(Fe+CuSO_{4}\rightarrow FeSO_{4}+Cu\downarrow\)
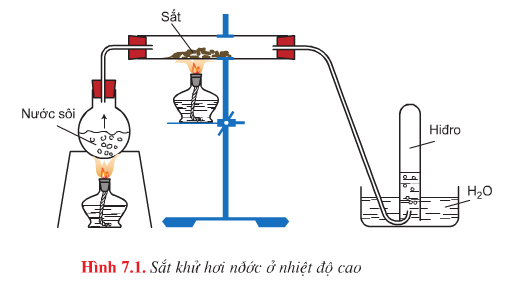
d. Tác dụng với nước
- Hình vẽ mô phỏng thí nghiệm: Sắt khử hơi nước ở nhiệt độ cao
- Phương trình hóa học:
\(3Fe+4H_{2}O\overset{t^{0}<570^{0}C}{\rightarrow}Fe_{3}O_{4}+4H_{2}\uparrow\)
\(Fe+H_{2}O\overset{t^{0}>570^{0}C}{\rightarrow}FeO+H_{2}\uparrow\)
2.4. Ứng dụng
- Chiếm khoảng 5% khối lượng vỏ trái đất, đứng hàng thứ hai trong các kim loại (sau Al).
- Trong tự nhiên sắt chủ yếu tồn tại dưới dạng hợp chất có trong các quặng:
+ Quặng manhetit (Fe3O4)
+ Quặng hematit đỏ (Fe2O3)
+ Quặng hematit nâu (Fe2O3.nH2O)
+ Quặng xiđerit (FeCO3)
+ Quặng pirit (FeS2)
- Có trong hemoglobin (huyết cầu tố) của máu
- Có trong các thiên thạch.
Bài tập minh họa
3.1. Bài tập Sắt - Cơ bản
Bài 1:
Cho m gam kim loại Fe tác dụng với dung dịch HNO3 dư, sau phản ứng thu được 3,36 lít khí NO đo ở đktc (sản phẩm khử duy nhất). Giá trị m là:
Hướng dẫn:
Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O 0,15 0,15 ⇒ m Fe = 0,15. 56 = 8,4 gam
Bài 2:
Cho 4,368 gam bột Fe tác dụng với m gam bột S. Sau phản ứng được rắn X. Toàn bộ X tan hết trong dung dịch HNO3 loãng dư được sản phẩm khử duy nhất là 0,12 mol NO. Giá trị m là:
Hướng dẫn:
Coi hỗn hợp X gồm Fe và S phản ứng với HNO3 Fe → Fe3+ + 3e S → S6+ + 6e N5+ + 3e → N2+ Bảo toàn e: 3nFe + 6nS = 3nNO ⇒ nS = 0,021 mol ⇒ m = 0,672g
Bài 3:
Cho m gam Fe vào bình đựng dung dịch H2SO4 và HNO3 thu được dung dịch X và 1,12 lít khí NO. Thêm tiếp H2SO4 dư vào bình được 0,448 lít NO và dung dịch Y. Trong cả 2 trường hợp đều có NO là sản phẩm khử duy nhất ở kiện tiêu chuẩn. Dung dịch Y hòa tan vừa hết 2,08 gam Cu không tạo sản phẩm khử N+5. Các phản ứng đều hoàn toàn. Giá trị m là:
Hướng dẫn:
Tổng số mol khí NO sau các phản ứng là: 0,07 mol Giả sử trong Y có Fe3+ và Fe2+ ⇒ bảo toàn e: 3nFe3+ + 2nFe2+ = 3nNO Lại có: 2Fe3+ + Cu → Cu2+ + 2Fe2+ (Y hòa tan Cu nhưng không có sản phẩm khử của N+5) ⇒ nFe3+ = 2nCu = 0,065 mol ⇒ nFe2+ = 0,0075 mol ⇒ m = 56.(0,065 + 0,0075) = 4,06g
Bài 4:
Cho 6,72 gam bột Fe tác dụng với 384 ml dung dịch AgNO3 1M sau khi phản ứng kết thúc thu được dung dịch A và m gam chất rắn. Dung dịch A tác dụng được với tối đa bao nhiêu gam bột Cu?
Hướng dẫn:
nFe = 0,12 mol; \(n_{AgNO_{3}}\) = 0,384 mol Fe + 2Ag+ → Fe2+ + 2Ag Fe2+ + Ag+ → Fe3+ + Ag ⇒ Dung dịch sau có: 0,12 mol Fe3+; 0,024 mol Ag+ ⇒ 2nCu = nFe3+ + nAg+ ⇒ nCu = 0,072 mol ⇒ mCu = 4,608g
3.2. Bài tập Sắt - Nâng cao
Bài 1:
Đốt cháy hỗn hợp gồm 2,4g Mg; 4,48g Fe với hỗn hợp X gồm có Cl2 và O2; sau phản ứng chỉ thu được hỗn hợp Y gồm các oxit và muối clorua (không có khí dư). Hòa tan Y vào lượng vừa đủ 120 ml HCl 2M thu được dung dịch Z. Cho AgNO3 dư vào Z thu được 61,01g kết tủa. Phần trăm V của O2 trong X là:
Hướng dẫn:
nMg = 0,1 mol; nFe = 0,08 và nHCl = 0,24. \(\begin{matrix} Mg & - & 2e & \rightarrow & Mg^{2+}\\ 0,1 & & 0,2 & & \\ Fe & - & 3e & \rightarrow & Fe^{3+}\\ 0,08 & & 0,24 & & \\ Cl_2 & + & 2e & \rightarrow & 2Cl^-\\ a & & 2a & & 2a\\ O_2 & + & 4e & \rightarrow & 2O^{2-}\\ b & & 4b & & 2b\\ Ag^+ & + & e & \rightarrow & Ag\\ x & & x & & x\\ 2H^+ & + & O^{2-} & \rightarrow & H_2O\\ 0,24 & & 0,12 & & \end{matrix}\) nO = 2b = 0,12 ⇒ b = 0,06 Bảo toàn mol e: 2a + 4b + x = 0,2 + 0,24 = 0,44 ⇒ 2a + x = 0,2 Kết tủa gồm: AgCl (2a + 0,24) mol và Ag x mol ⇒ 143,5(2a + 0,24) + 108x = 61,01 ⇒ 287a + 108x = 26,57 ⇒ a = 0,07 và x = 0,06 ⇒ X gồm 0,07 mol Cl2 và 0,06 mol O2 \(\Rightarrow \%V_{O_2} = 46,15\%\)
4. Luyện tập Bài 31 Hóa học 12
Sau bài học cần nắm:
- Vị trí của Sắt trong Bảng hệ thống tuần hoàn các nguyên tố hóa học
- Cấu tạo nguyên tử, tính chất vật lí - hóa học và phương pháp điều chế.
- Biết được tính chất và ứng dụng của một số hợp chất quan trọng của Sắt.
4.1. Trắc nghiệm
Bài kiểm tra Trắc nghiệm Hoá học 12 Bài 31 có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
-
Câu 1:
Cho phản ứng hoá học: Fe + CuSO4 → FeSO4 + Cu. Trong phản ứng trên xảy ra
- A. sự khử Fe2+ và sự oxi hoá Cu.
- B. sự khử Fe2+ và sự khử Cu2+.
- C. sự khử Fe2+ và sự khử Cu2+.
- D. sự oxi hoá Fe và sự khử Cu2+.
-
Câu 2:
Thực hiện các thí nghiệm sau:
(1) Cho Fe vào dung dịch HCl (4) Đốt dây sắt trong khí clo
(2) Cho Fe dư vào dd HNO3 loãng (5)Cho Fe vào dung dịch AgNO3 dư
(3) Cho Fe vào dd KHSO4.
Số thí nghiệm tạo ra muối sắt (II) là:
- A. 2.
- B. 3.
- C. 4.
- D. 5.
-
Câu 3:
Kim loại Fe có thể khử được ion nào sau đây?
- A. Mg2+.
- B. Zn2+.
- C. Cu2+.
- D. Al3+.
-
Câu 4:
Cho bột Fe vào dung dịch AgNO3 dư, sau khi phản ứng xảy ra hoàn toàn, thu được dung dịch gồm các chất tan:
- A. Fe(NO3)2 , Fe(NO3)3 , AgNO3.
- B. Fe(NO3)2, AgNO3.
- C. Fe(NO3)3, AgNO3.
- D. Fe(NO3)2, Fe(NO3)3.
-
Câu 5:
Cho hỗn hợp Fe, Cu phản ứng với dung dịch HNO3 loãng. Sau khi phản ứng hoàn toàn, thu được dung dịch chỉ chứa một chất tan và kim loại dư. Chất tan đó là:
- A. Cu(NO3)2.
- B. Fe(NO3)3.
- C. Fe(NO3)2.
- D. HNO3.
-
Câu 6:
Cho bột Fe vào dung dịch gồm AgNO3 và Cu(NO3)2 . Sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch X gồm 2 muối và chất rắn Y gồm 2 kim loại. Hai muối trong X và 2 kim loại trong Y lần lượt là:
- A. Cu(NO3)2, Fe(NO3)2 và Cu, Fe.
- B. Cu(NO3)2, Fe(NO3)2 và Ag, Cu.
- C. Fe(NO3)2, Fe(NO3)3 và Cu, Ag.
- D. Cu(NO3)2, AgNO3 và Cu, Ag
-
Câu 7:
Hòa tan hoàn toàn 8,4gam Fe bằng dung dịch H2SO4 loãng, dư thu được dung dịch X. Dung dịch X phản ứng vừa đủ với V ml dung dịch KMnO4 0,5M. Giá trị của V là:
- A. 90.
- B. 120.
- C. 30.
- D. 60.
Câu 8-20: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
4.2. Bài tập SGK và Nâng cao
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hoá học 12 Bài 31.
Bài tập 1 trang 141 SGK Hóa học 12
Bài tập 2 trang 141 SGK Hóa học 12
Bài tập 3 trang 141 SGK Hóa học 12
Bài tập 4 trang 141 SGK Hóa học 12
Bài tập 5 trang 141 SGK Hóa học 12
Bài tập 1 trang 189 SGK Hóa học 12 nâng cao
Bài tập 2 trang 189 SGK Hóa học 12 nâng cao
Bài tập 3 trang 198 SGK Hóa 12 Nâng cao
Bài tập 4 trang 198 SGK Hóa 12 Nâng cao
Bài tập 5 trang 198 SGK Hóa 12 Nâng cao
Bài tập 31.1 trang 71 SBT Hóa học 12
Bài tập 31.2 trang 71 SBT Hóa học 12
Bài tập 31.3 trang 71 SBT Hóa học 12
Bài tập 31.4 trang 71 SBT Hóa học 12
Bài tập 31.5 trang 71 SBT Hóa học 12
Bài tập 31.6 trang 71 SBT Hóa học 12
Bài tập 31.7 trang 72 SBT Hóa học 12
Bài tập 31.8 trang 72 SBT Hóa học 12
Bài tập 31.9 trang 72 SBT Hóa học 12
Bài tập 31.10 trang 72 SBT Hóa học 12
Bài tập 31.11 trang 72 SBT Hóa học 12
Bài tập 31.12 trang 73 SBT Hóa học 12
Bài tập 31.13 trang 73 SBT Hóa học 12
Bài tập 31.14 trang 73 SBT Hóa học 12
Bài tập 31.15 trang 73 SBT Hóa học 12
Bài tập 31.16 trang 74 SBT Hóa học 12
Bài tập 31.17 trang 74 SBT Hóa học 12
Bài tập 31.18 trang 74 SBT Hóa học 12
Bài tập 31.20 trang 74 SBT Hóa học 12
Bài tập 31.21 trang 74 SBT Hóa học 12
Bài tập 31.19 trang 74 SBT Hóa học 12
5. Hỏi đáp về Bài 31 Chương 7 Hoá học 12
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa HOC247 thảo luận và trả lời nhé.
 NONE
NONE Bài học cùng chương
 Hoá học 12 Bài 32: Hợp chất của sắt
Hoá học 12 Bài 32: Hợp chất của sắt  Hoá học 12 Bài 33: Hợp kim của sắt
Hoá học 12 Bài 33: Hợp kim của sắt  Hoá học 12 Bài 34: Crom và hợp chất của Crom
Hoá học 12 Bài 34: Crom và hợp chất của Crom  Hoá học 12 Bài 35: Đồng và hợp chất của Đồng
Hoá học 12 Bài 35: Đồng và hợp chất của Đồng  Hoá học 12 Bài 36: Sơ lược về niken, kẽm, chì, thiếc
Hoá học 12 Bài 36: Sơ lược về niken, kẽm, chì, thiếc  Hoá học 12 Bài 37: Luyện tập Tính chất hóa học của sắt và hợp chất của sắt ADSENSE TRACNGHIEM
Hoá học 12 Bài 37: Luyện tập Tính chất hóa học của sắt và hợp chất của sắt ADSENSE TRACNGHIEM  Bộ đề thi nổi bật
Bộ đề thi nổi bật  UREKA AANETWORK
UREKA AANETWORK 
XEM NHANH CHƯƠNG TRÌNH LỚP 12
Toán 12
Lý thuyết Toán 12
Giải bài tập SGK Toán 12
Giải BT sách nâng cao Toán 12
Trắc nghiệm Toán 12
Hình học 12 Chương 3
Ngữ văn 12
Lý thuyết Ngữ Văn 12
Soạn văn 12
Soạn văn 12 (ngắn gọn)
Văn mẫu 12
Soạn Ai đã đặt tên cho dòng sông
Tiếng Anh 12
Giải bài Tiếng Anh 12
Giải bài Tiếng Anh 12 (Mới)
Trắc nghiệm Tiếng Anh 12
Unit 9 Lớp 12 Deserts
Tiếng Anh 12 mới Unit 5
Vật lý 12
Lý thuyết Vật Lý 12
Giải bài tập SGK Vật Lý 12
Giải BT sách nâng cao Vật Lý 12
Trắc nghiệm Vật Lý 12
Ôn tập Vật lý 12 Chương 3
Hoá học 12
Lý thuyết Hóa 12
Giải bài tập SGK Hóa 12
Giải BT sách nâng cao Hóa 12
Trắc nghiệm Hóa 12
Hoá Học 12 Chương 5
Sinh học 12
Lý thuyết Sinh 12
Giải bài tập SGK Sinh 12
Giải BT sách nâng cao Sinh 12
Trắc nghiệm Sinh 12
Sinh Học 12 Chương 2 Tiến hóa
Lịch sử 12
Lý thuyết Lịch sử 12
Giải bài tập SGK Lịch sử 12
Trắc nghiệm Lịch sử 12
Lịch Sử 12 Chương 3 Lịch Sử VN
Địa lý 12
Lý thuyết Địa lý 12
Giải bài tập SGK Địa lý 12
Trắc nghiệm Địa lý 12
Địa Lý 12 VĐSD và BVTN
GDCD 12
Lý thuyết GDCD 12
Giải bài tập SGK GDCD 12
Trắc nghiệm GDCD 12
GDCD 12 Học kì 1
Công nghệ 12
Lý thuyết Công nghệ 12
Giải bài tập SGK Công nghệ 12
Trắc nghiệm Công nghệ 12
Công nghệ 12 Chương 3
Tin học 12
Lý thuyết Tin học 12
Giải bài tập SGK Tin học 12
Trắc nghiệm Tin học 12
Tin học 12 Chương 2
Cộng đồng
Hỏi đáp lớp 12
Tư liệu lớp 12
Xem nhiều nhất tuần
Video: Vợ nhặt của Kim Lân
Đề cương HK1 lớp 12
Video ôn thi THPT QG môn Sinh
Video ôn thi THPT QG môn Văn
Video ôn thi THPT QG môn Vật lý
Video ôn thi THPT QG Tiếng Anh
Video ôn thi THPT QG môn Hóa
Video ôn thi THPT QG môn Toán
Khái quát văn học Việt Nam từ đầu CMT8 1945 đến thế kỉ XX
Người lái đò sông Đà
Đất Nước- Nguyễn Khoa Điềm
Đàn ghi ta của Lor-ca
Ai đã đặt tên cho dòng sông
Tây Tiến
Quá trình văn học và phong cách văn học
YOMEDIA YOMEDIA ×Thông báo
Bạn vui lòng đăng nhập trước khi sử dụng chức năng này.
Bỏ qua Đăng nhập ×Thông báo
Bạn vui lòng đăng nhập trước khi sử dụng chức năng này.
Đồng ý ATNETWORK ON QC Bỏ qua >>
QC Bỏ qua >> 
Từ khóa » Hóa Học 12 Bài Sắt
-
Lý Thuyết Hóa 12: Bài 31. Sắt - TopLoigiai
-
Soạn Hoá Học 12 Bài 31: Sắt | Học Cùng
-
Giải Hóa 12 Bài 31: Sắt
-
Bài 31. Sắt
-
Giải Bài Tập Hóa 12 Bài 31: Sắt
-
Giải Bài Tập Hóa Học 12 - Bài 31: Sắt
-
Giải Hoá 12 Bài 31: Sắt SGK Trang 141 đầy đủ Nhất
-
Giải Bài 31 Hóa Học 12: Sắt - Tech12h
-
Hoá Học 12 Bài 31: Sắt
-
Bài 31: Lí Thuyết Và Giải Bài Tập Về Sắt
-
Giáo án Hóa Học Lớp 12 - Bài 31: Sắt
-
Giải Bài Tập Hóa 12 Bài 31: Sắt
-
Hóa Học 12 Bài 31: Sắt - Trường THPT Số 2 Đức Phổ
-
Bài 31: Sắt.pdf (giáo án Hoá Học 12) | Tải Miễn Phí