Hoá Học 8 Bài 23: Bài Luyện Tập 4
Có thể bạn quan tâm
Nội dung Bài luyện tập 4 củng cố lại các khái niệm: mol, khối lượng mol, thể tích mol chất khí, tỉ khối của chất khí... Tổng kết lại mối quan hệ giữa khối lượng chất, thể tích khí; Vận dụng kiến thức giải bài tập và hiểu các hiện tượng trong thực tế.
ATNETWORK YOMEDIA1. Tóm tắt lý thuyết
1.1. Mol
1.2. Khối lượng mol
1.3. Thể tích mol chất khí
1.4. Tỉ khối của chất khí
2. Bài tập minh hoạ
3. Luyện tập Bài 23 Hóa học 8
3.1. Trắc nghiệm
3.2. Bài tập SGK và Nâng cao
4. Hỏi đáp về Bài 23 Chương 3 Hóa học 8

Tóm tắt lý thuyết
1.1. Mol
| Các cụm từ sau có nghĩa thế nào ? | Ý nghĩa |
| 1 mol nguyên tử Cu | 1N nguyên tử Cu hay 6.1023 nguyên tử Cu |
| 1,5 mol nguyên tử H | 1,5 N nguyên tử H hay 1,5.6.1023 nguyên tử H (9.1023) |
| 2 mol phân tử H2 | 2N phân tử H2 hay 2.6.1023 phân tử H2 (12.1023) |
| 0,15 mol phân tử H2O | 0,15N phân tử H2O hay 0,15.6.1023 phân tử H2O (0,9.1023) |
1.2. Khối lượng mol
| Các câu sau có nghĩa thế nào ? | Ý nghĩa |
| Khối lượng mol của nước là 18 g/mol | Khối lượng N phân tử nước là 18 g. Kí hiệu là \({M_{{H_2}O}}\) = 18g/mol |
| Khối lượng mol nguyên tử H là 1g/mol | Khối lượng N nguyên tử H là 1 g. Kí hiệu là MH = 1g/mol |
| Khối lượng mol phân tử H2 là 2 g/mol | Khối lượng N phân tử hiđro là 2 g. Kí hiệu là \({M_{{H_2}}}\) = 2g/mol |
1.3. Thể tích mol chất khí
| Ở cùng điều kiện nhiệt độ và áp suất thể tích mol của khí CO2, O2, H2. | \({V_{C{O_2}}} = {V_{{O_2}}} = {V_{{H_2}}}\) |
| Ở ( đktc) Thể tích mol các chất khí CO2, O2, H2 | \({V_{C{O_2}}} = {V_{{O_2}}} = {V_{{H_2}}} = 22,4(lit)\) |
| Thể tích mol của những chất khí khác nhau, ở cùng điều kiện nhiệt độ và áp suất. | Bằng nhau |
| Thể tích mol của những chất khí khác nhau, ở cùng điều kiện nhiệt độ 0oC và áp suất 1 atm. | Bằng nhau và bằng 22,4 lit |
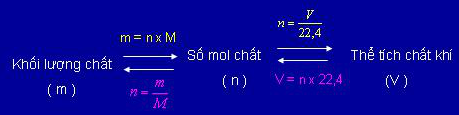
Hình 1: Sự chuyển đổi giữa lượng chất (số mol) - khối lượng chất - thể tích chất khí (đktc)
1.4. Tỉ khối của chất khí
| Tỉ khối của khí A đối với khí B ( dA/B = 1,5) | Khí A nặng hơn khí B 1,5 lần |
| Tỉ khối của khí CO2 đối với không khí bằng 1,52 | khí CO2 nặng hơn không khí 1,52 lần. |
Bài tập minh họa
Bài 1:
Trong phòng thí nghiệm, người ta cho 4,6 gam Natri (Na) phản ứng với khí clo (Cl2) sau phản ứng thu được muối Natri clorua (NaCl)
2Na + Cl2 .PNG)
a, Tính thể tích khí clo (ở đktc) cần dùng để phản ứng hết số Natri trên?
b, Tính khối lượng muối Natriclorua tạo thành?
c, Khí clo nặng hay nhẹ hơn không khí bao nhiêu lần?
Hướng dẫn:
a) Số mol Natri tham gia phản ứng là:
\({n_{Na}} = \frac{{{m_{Na}}}}{M} = \frac{{4,6}}{{23}} = 0,2(mol)\)
Phương trình phản ứng:
2Na + Cl2 .PNG)
2 mol 1 mol 2 mol
0,2 mol → ? mol ? mol
Số mol clo dùng để phản ứng hết lượng Natri là:
\({n_{C{l_2}}} = \frac{{0,2 \times 1}}{2} = 0,1(mol)\)
Thể tích khí Clo cần dùng là:
\({V_{C{l_2}}} = {n_{C{l_2}}} \times 22,4 = 0,1 \times 22,4 = 2,24(lit)\)
b) Số mol muối Natri tạo thành là: 0,2 mol
Khối lượng muối Natri tạo thành là:
\({{\rm{m}}_{{\rm{Na}}}}{\rm{ = }}{{\rm{n}}_{{\rm{Na}}}}{\rm{.M = 0,2}}{\rm{.23 = 4,6(g)}}\)
c) Khí Clo nặng hơn không khí số lần là:
\({d_{C{l_2}/KK}} = \frac{{{M_{C{l_2}}}}}{{29}} = \frac{{35,5 \times 2}}{{29}} \approx 2,45\)
3. Luyện tập Bài 23 Hóa học 8
Sau bài học cần nắm:
- Khái niệm: mol, khối lượng mol, thể tích mol chất khí, tỉ khối của chất khí...
- Tổng kết lại mối quan hệ giữa khối lượng chất, thể tích khí
- Vận dụng kiến thức giải bài tập và hiểu các hiện tượng trong thực tế.
3.1. Trắc nghiệm
Bài kiểm tra Trắc nghiệm Hóa học 8 Bài 23 có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
-
Câu 1:
Khí X có tỷ khối so với không khí gần bằng 0,97; X là khí nào trong các chất sau:
- A. CO
- B. CO2
- C. CH4
- D. SO2
-
Câu 2:
Có điểm nào chung cho các lượng chất sau: 9,8 g H2SO4; 4g NaOH; 8g CuO
- A. Đều là đơn chất
- B. Đều có cùng số mol
- C. Đều có cùng số nguyên tử lưu huỳnh
- D. Đều có cùng số nguyên tử hidro
-
Câu 3:
Cho các chất : FeS, FeS2 , FeO, Fe2O3 . Chất có hàm lượng sắt lớn nhất là :
- A. FeS
- B. FeS2
- C. FeO
- D. Fe2O3
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
3.2. Bài tập SGK và Nâng cao
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 8 Bài 23.
Bài tập 1 trang 79 SGK Hóa học 8
Bài tập 2 trang 79 SGK Hóa học 8
Bài tập 3 trang 79 SGK Hóa học 8
Bài tập 4 trang 79 SGK Hóa học 8
Bài tập 5 trang 79 SGK Hóa học 8
Bài tập 23.1 trang 30 SBT Hóa học 8
Bài tập 23.2 trang 30 SBT Hóa học 8
Bài tập 23.3 trang 31 SBT Hóa học 8
Bài tập 23.4 trang 31 SBT Hóa học 8
Bài tập 23.5 trang 31 SBT Hóa học 8
Bài tập 23.6 trang 31 SBT Hóa học 8
Bài tập 23.7 trang 31 SBT Hóa học 8
Bài tập 23.8 trang 31 SBT Hóa học 8
4. Hỏi đáp về Bài 23 Chương 3 Hóa học 8
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa HOC247 thảo luận và trả lời nhé.
 NONE
NONE Bài học cùng chương
 Hoá học 8 Bài 18: Mol
Hoá học 8 Bài 18: Mol  Hoá học 8 Bài 19: Chuyển đổi giữa khối lượng, thể tích và lượng chất
Hoá học 8 Bài 19: Chuyển đổi giữa khối lượng, thể tích và lượng chất  Hoá học 8 Bài 20: Tỉ khối của chất khí
Hoá học 8 Bài 20: Tỉ khối của chất khí  Hoá học 8 Bài 21: Tính theo công thức hóa học
Hoá học 8 Bài 21: Tính theo công thức hóa học  Hoá học 8 Bài 22: Tính theo phương trình hóa học ADSENSE TRACNGHIEM
Hoá học 8 Bài 22: Tính theo phương trình hóa học ADSENSE TRACNGHIEM  Bộ đề thi nổi bật
Bộ đề thi nổi bật  UREKA AANETWORK
UREKA AANETWORK 
XEM NHANH CHƯƠNG TRÌNH LỚP 8
Toán 8
Toán 8 Kết Nối Tri Thức
Toán 8 Chân Trời Sáng Tạo
Toán 8 Cánh Diều
Giải bài tập Toán 8 KNTT
Giải bài tập Toán 8 CTST
Giải bài tập Toán 8 Cánh Diều
Trắc nghiệm Toán 8
Ngữ văn 8
Ngữ Văn 8 Kết Nối Tri Thức
Ngữ Văn 8 Chân Trời Sáng Tạo
Ngữ Văn 8 Cánh Diều
Soạn Văn 8 Kết Nối Tri Thức
Soạn Văn 8 Chân Trời Sáng Tạo
Soạn Văn 8 Cánh Diều
Văn mẫu 8
Tiếng Anh 8
Tiếng Anh 8 Kết Nối Tri Thức
Tiếng Anh 8 Chân Trời Sáng Tạo
Tiếng Anh 8 Cánh Diều
Trắc nghiệm Tiếng Anh 8 KNTT
Trắc nghiệm Tiếng Anh 8 CTST
Trắc nghiệm Tiếng Anh 8 Cánh Diều
Tài liệu Tiếng Anh 8
Khoa học tự nhiên 8
Khoa học tự nhiên 8 KNTT
Khoa học tự nhiên 8 CTST
Khoa học tự nhiên 8 Cánh Diều
Giải bài tập KHTN 8 KNTT
Giải bài tập KHTN 8 CTST
Giải bài tập KHTN 8 Cánh Diều
Trắc nghiệm Khoa học tự nhiên 8
Lịch sử và Địa lý 8
Lịch sử & Địa lí 8 KNTT
Lịch sử & Địa lí 8 CTST
Lịch sử & Địa lí 8 Cánh Diều
Giải bài tập LS và ĐL 8 KNTT
Giải bài tập LS và ĐL 8 CTST
Giải bài tập LS và ĐL 8 Cánh Diều
Trắc nghiệm Lịch sử và Địa lí 8
GDCD 8
GDCD 8 Kết Nối Tri Thức
GDCD 8 Chân Trời Sáng Tạo
GDCD 8 Cánh Diều
Giải bài tập GDCD 8 KNTT
Giải bài tập GDCD 8 CTST
Giải bài tập GDCD 8 Cánh Diều
Trắc nghiệm GDCD 8
Công nghệ 8
Công Nghệ 8 KNTT
Công Nghệ 8 CTST
Công Nghệ 8 Cánh Diều
Trắc nghiệm Công Nghệ 8
Giải bài tập Công Nghệ 8 KNTT
Giải bài tập Công Nghệ 8 CTST
Giải bài tập Công Nghệ 8 CD
Tin học 8
Tin Học 8 Kết Nối Tri Thức
Tin Học 8 Chân Trời Sáng Tạo
Trắc nghiệm Tin học 8
Giải bài tập Tin học 8 CD
Tin Học 8 Cánh Diều
Cộng đồng
Hỏi đáp lớp 8
Tư liệu lớp 8
Xem nhiều nhất tuần
Đề thi giữa HK1 lớp 8
Đề thi HK1 lớp 8
Đề thi giữa HK2 lớp 8
Đề thi HK2 lớp 8
5 bài văn mẫu hay về bài thơ Nhớ rừng
Ngắm trăng
Quê hương
Tiếng Anh Lớp 8 Unit 9
Khi con tu hú
Tiếng Anh Lớp 8 Unit 10
Nhớ rừng
Video Toán Nâng cao lớp 8- HK1
Video Toán Nâng cao lớp 8- HK Hè
Video Toán Nâng cao lớp 8- HK2
YOMEDIA YOMEDIA ×Thông báo
Bạn vui lòng đăng nhập trước khi sử dụng chức năng này.
Bỏ qua Đăng nhập ×Thông báo
Bạn vui lòng đăng nhập trước khi sử dụng chức năng này.
Đồng ý ATNETWORK ON QC Bỏ qua >>
QC Bỏ qua >> 
Từ khóa » Học 8 Bài 23 Bài Luyện Tập 4
-
Giải Hóa 8 Bài 23: Bài Luyện Tập 4
-
Bài 23. Bài Luyện Tập 4
-
Giải Hóa 8 Bài 23: Bài Luyện Tập 4
-
Giải Bài Tập Hóa Học 8 - Bài 23: Bài Luyện Tập 4
-
Hóa Học Lớp 8 - Bài 23 - Bài Luyện Tập 4 - YouTube
-
Hóa Học 8 - Bài 23 - Luyện Tập 4 - Cô Nguyễn Thị Thu (HAY NHẤT)
-
Bài Luyện Tập 4 - Bài 23 - Hóa 8 - Cô Nguyễn Thu (DỄ HIỂU NHẤT)
-
Giải Bài 23 Hóa Học 8: Bài Luyện Tập 4 - Tech12h
-
Giải Hóa 8 Bài 23: Bài Luyện Tập 4
-
Bài 23. Bài Luyện Tập 4 - - Thư Viện Bài Giảng điện Tử
-
Bài 23: Bài Luyện Tập 4 - CoLearn.VN
-
Bài 23: Bài Luyện Tập 4 | Vở Bài Tập Hoá Học 8 - SoanVan.NET
-
Giải Hoá Học 8 Bài 23: Bài Luyện Tập 4 Trang 79 SGK
-
Hóa 8 Bài 23: Bài Luyện Tập 4 - Haylamdo