Liên Kết Ion Là Gì? Sự Hình Thành Liên Kết Ion Như Thế Nào?
Có thể bạn quan tâm
Trong phản ứng hóa học, khi nguyên tử, phân tử thêm hoặc mất bớt electron nó sẽ tạo thành các phần tử mang điện gọi là ion. Các ion trái dấu hút nhau bằng lực hút tĩnh điện tạo thành hợp chất chứa liên kết ion. Trong bài viết này, Marathon Education sẽ chia sẻ những kiến thức giúp các em nắm vững những lý thuyết cơ bản như liên kết ion là gì, ví dụ minh họa, sự hình thành, tính chất, dấu hiệu nhận biết loại liên kết này. Các em hãy theo dõi bài viết dưới đây.

Liên Kết Ion Là Gì? Sự Hình Thành Liên Kết Ion
Liên kết ion là gì?
Liên kết ion (hay liên kết điện tích) là một liên kết hóa học có bản chất là lực hút tĩnh điện giữa 2 ion mang điện tích trái dấu. Liên kết này thường là liên kết giữa các nguyên tử nguyên tố phi kim với các nguyên tử nguyên tố kim loại.
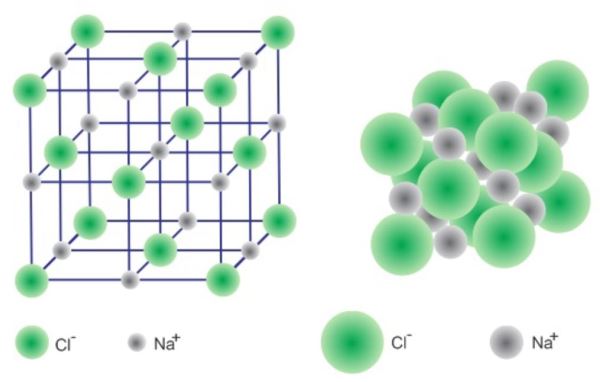
Liên kết ion là gì? (Nguồn: Internet)
Ví dụ về liên kết ion: Sự kết hợp giữa natri (Na+) và clorua (Cl–) tạo thành natri clorua (NaCl):
Na+ + Cl– → NaCl
Khái niệm cation và anion

Các nguyên tử kim loại (có 1, 2, 3 electron lớp ngoài cùng) có độ âm điện nhỏ, dễ mất electron tạo ra ion dương (cation). Các nguyên tử phi kim (có 5, 6, 7 electron lớp ngoài cùng) có độ âm điện lớn, dễ nhận electron để tạo ra ion âm (anion).
Tóm lại, ion được chia thành cation và anion:
- Cation: Ion dương
- Anion: Ion âm
Cation
- Cation là những ion mang điện tích dương. Chúng được hình thành khi một kim loại mất electron. Kim loại mất một hoặc nhiều hơn một electron và không mất bất kỳ proton nào.
- Ký hiệu của một cation là ký hiệu nguyên tố hoặc công thức phân tử, theo sau là ký hiệu của điện tích. Số điện tích được đưa ra đầu tiên, sau đó là một biểu tượng dấu cộng.
- Cation có thể là ion của nguyên tử hoặc phân tử.
Ví dụ cách nhận biết và ký hiệu của cation:
- Ag+ (kim loại bạc mang 1 điện tích dương).
- Al3+ (kim loại nhôm mang 3 điện tích dương).
- NH4+ (phân tử amoni có 4 điện tích dương).
Anion
- Anion là các ion mang điện tích âm. Chúng được hình thành khi các nguyên tử phi kim giành được các electron. Chúng thu được một hoặc nhiều hơn một electron và không mất đi bất kỳ proton nào. Do đó chúng sở hữu một điện tích thuần âm.
Ví dụ:
- I– (Nguyên tố phi kim iot mang 1 điện tích âm).
- Cl– (Clo là nguyên tố anion đặc trưng).
- OH– (Nhóm hydroxyl có điện tích âm là 1).
Ion đơn nguyên tử và ion đa nguyên tử
Ion đơn nguyên tử
Ion đơn nguyên tử là các ion được tạo thành từ một nguyên tử.
Ví dụ: Na+, Li+, Mg2+…
Ion đa nguyên tử
Ion đa nguyên tử hay ion phân tử là một nhóm 2 nguyên tử trở lên liên kết cộng hóa trị với nhau.
Ví dụ: cation amoni NH4+, anion hidroxit OH–, anion sunfat SO42-…

Sự hình thành liên kết ion
Để hình thành liên kết ion cần phải có các điều kiện sau:
- Liên kết được hình thành giữa các nguyên tố có tính chất khác hẳn nhau (kim loại điển hình và phi kim điển hình).
- Quy ước hiệu độ âm điện giữa hai nguyên tử liên kết ≥ 1,7 là liên kết ion (trừ một số trường hợp).
Dấu hiệu nhận biết liên kết ion:
- Phân tử hợp chất được hình thành từ kim loại điển hình (kim loại nhóm IA, IIA) và phi kim điển hình (phi kim nhóm VIIA và Oxi).
Ví dụ: Các phân tử NaCl, MgCl2, BaF2,… đều chứa liên kết ion, là liên kết được hình thành giữa các cation kim loại và anion phi kim.
- Phân tử hợp chất muối chứa cation hoặc anion đa nguyên tử.
Ví dụ: Các phân tử NH4Cl, MgSO4, AgNO3,… đều chứa liên kết ion, là liên kết được hình thành giữa cation kim loại hoặc amoni và anion gốc axit.
Tính chất của liên kết ion là gì?
Liên kết ion có các tính chất chung như sau:
- Các ion được sắp xếp theo cấu trúc mạng tinh thể.
- Chất rắn ion là tinh thể tồn tại ở nhiệt độ phòng.
- Đây là liên kết có lực hút tĩnh điện mạnh. Điều này có nghĩa là các hợp chất ion thường cứng và có điểm nóng chảy và điểm sôi cao.
Ví dụ: Nhiệt độ nóng chảy của NaCl là 800oC, của MgO là 2800oC.
- Các hợp chất ion dễ vỡ và liên kết bị phá vỡ dọc theo các mặt phẳng khi hợp chất bị đặt dưới áp lực.
- Tinh thể rắn không dẫn điện, nhưng dung dịch ion thì dẫn điện được.
Cấu trúc mạng tinh thể của liên kết ion
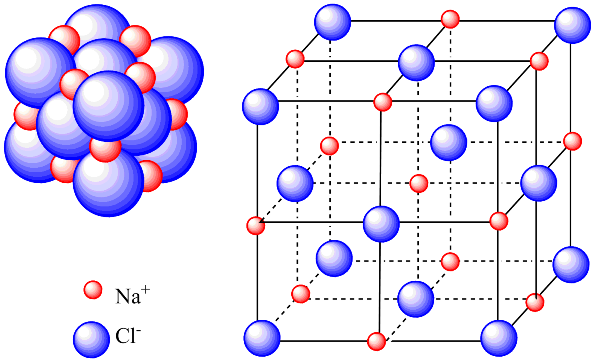
Liên kết ion thực sự là sự kết hợp của rất nhiều ion liên kết với nhau thành một phân tử khổng lồ. Sự sắp xếp các ion trong một cấu trúc hình học thông thường được gọi là mạng tinh thể.
Xeton là gì? Tìm hiểu A-Z về xenton - Hóa học lớp 11Ví dụ như NaCl, thực tế NaCl không chứa một ion Na và một ion Cl, nhiều ion của chúng tạo thành mạng tinh thể với tỉ lệ 1:1.
So sánh liên kết ion và liên kết cộng hóa trị
| Loại liên kết | Liên kết ion | Liên kết cộng hóa trị |
| Định nghĩa | Là liên kết giữa các ion mang điện tích trái dấu hình thành bởi lực hút tĩnh điện | Là liên kết hình thành giữa hai nguyên tử sử dụng chung một hoặc nhiều cặp electron |
| Bản chất của liên kết | Sự chuyển electron từ nguyên tử này sang nguyên tử khác | Sử dụng một hoặc nhiều cặp electron chung |
| Hiệu độ âm điện | ∆x ≥ 1,7 | 0 < ∆x < 1,7 |
Gia sư Online Học Online Toán 12 Học Online Hóa 10 Học Online Toán 11 Học Online Toán 6 Học Online Toán 10 Học Online Toán 7 Học Online Lý 10 Học Online Lý 9 Học Online Toán 8 Học Online Toán 9 Học Tiếng Anh 6 Học Tiếng Anh 7Tham khảo ngay các khoá học online của Marathon Education
Hy vọng với những kiến thức mà Marathon Education đã chia sẻ trong bài viết trên sẽ giúp các em sẽ nắm vững những lý thuyết cơ bản như liên kết ion là gì, sự hình thành liên kết ion, cation, anion, dấu hiệu nhận biết liên kết ion cũng như sự khác biệt giữa liên kết này và liên kết cộng hóa trị. Các em có thể học online trực tuyến thêm các kiến thức bổ ích của các môn học Toán Lý Hoá tại website Marathon Education. Chúc các em học tập tốt!
Từ khóa » Khi Na Và Cl Tác Dụng Với Nhau Tạo Hợp Chất Hóa Học Thì Năng Lượng
-
Khi Na Và Cl Tác Dụng Với Nhau Tạo Hợp Chất Hóa Học Thì - Hoc24
-
Khi Kali Và Clo Tác Dụng Với Nhau Tạo Ra Hợp Chất Hóa Học Thì:
-
C1: Tìm định Nghĩa Sai Về Liên Kết Ion - Hóa Học
-
Chương III LIÊN KẾT HOÁ HỌC Flashcards | Quizlet
-
Sự điện Ly Của Các Chất
-
Liên Kết Ion Là Gì, được Hình Thành Như Thế Nào? Giải đáp Chi Tiết Nhất
-
Tính Chất Hóa Học Của Clo – Ứng Dụng Và Điều Chế Clo
-
CLO Là Gì? Tính Chất, Công Dụng & Cách điều Chế CLO
-
Liên Kết Ion – Wikipedia Tiếng Việt
-
Cách Tính đương Lượng Gam Các Chất Hóa Học H3PO4, Na2CO3
-
Năng Lượng Liên Kết – Wikipedia Tiếng Việt
-
Những Nguyên Tắc Quan Trọng Khi Thi Trắc Nghiệm Môn Hóa
-
[PDF] Chương II. LIÊN KẾT VÀ SỰ BIẾN ĐỔI LIÊN KẾT Ở HCHC Thời Lượng
-
Điều Hòa Toan - Kiềm - Rối Loạn Nội Tiết Và Chuyển Hóa - MSD Manuals