Lý Thuyết Hóa 10: Bài 1. Thành Phần Nguyên Tử - Top Lời Giải
Có thể bạn quan tâm
Tóm tắt Lý thuyết Hóa học 10 Kết nối tri thức Bài 1: Thành phần nguyên tử theo chương trình Sách mới ngắn gọn nhất. Tổng hợp lý thuyết Hóa học 10 trọn bộ chi tiết, đầy đủ.
Bài 1: Thành phần nguyên tử
Mục lục nội dung I. Các loại hạt cấu tạo nên nguyên tửII. Kích thước và khối lượng nguyên tử1. Kích thước2. Khối lượngIII. Điện tích hạt nhân và số khốiI. Các loại hạt cấu tạo nên nguyên tử
- Năm 1897, J.J.Thomson (người Anh) thực hiện phóng điện qua không khí loãng đã phát hiện ra chùm tia phát ra từ cực âm và bị hút lệch về phía cực dương của điện trường, chứng tỏ chúng mang điện tích âm. Đó chính là chùm các hạt electron, electron là một thành phần của nguyên tử
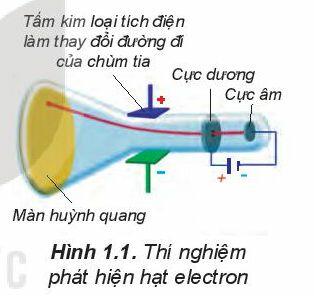
- Năm 1911, E. Rutherford đã tiến hành bắn phá một chùm hạt alpha lên một lá vàng siêu mỏng và quan sát đường đi của chúng sau khi bắn phá bằng màn huỳnh quang. Kết quả cho thấy nguyên tử có cấu tạo rỗng, ở tâm chứa một hạt nhân mang điện tích dương và có kích thước rất nhỏ so với kích thước nguyên tử.
- Năm 1918, khi bắn phá hạt nhân nguyên tử nitrogen bằng các hạt α, Rutherford đã phát hiện ra hạt proton.
- Năm 1932, J.Chadwick (người Anh), cộng sự của Rutherford đã phát hiện ra hạt neutron khi bắn phá beryllium bằng các hạt α
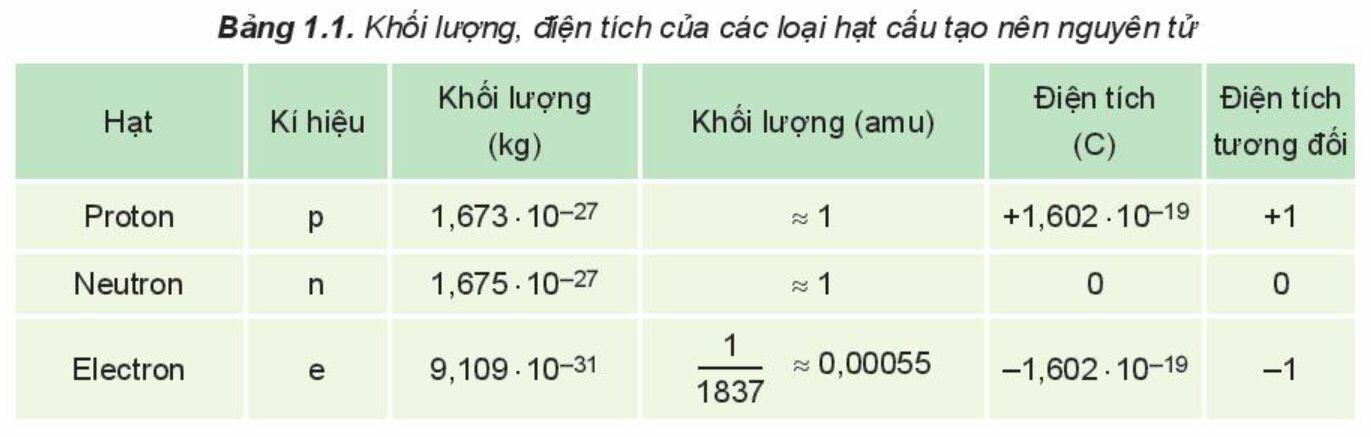
Kết luận:
Thành phần cấu tạo của nguyên tử gồm:
- Hạt nhân: ở tâm của nguyên tử, chứa các proton mang điện tích dương và các neutron không mang điện (trừ trường hợp 11H)
- Vỏ nguyên tử: chứa các electron mang điện tích âm, chuyển động rất nhanh xung quanh hạt nhân.
II. Kích thước và khối lượng nguyên tử
1. Kích thước
Kích thước của nguyên tử rất nhỏ nên thường được biểu diễn bằng đơn vị picomet (pm) hay Angstrom (Å).
1 pm = 10-12 m; 1Å = 10-10 m
Hạt nhân nguyên tử có kích thước vô cùng nhỏ so với nguyên tử.
2. Khối lượng
- Bằng tổng khối lượng các hạt proton, neutron và electron có trong nguyên tử
- Khối lượng nguyên tử rất nhỏ nên một lượng một lượng chất rất nhỏ cũng chứa tới hàng tỉ tỉ nguyên tử
- Đơn vị khối lượng nguyên tử (amu)
III. Điện tích hạt nhân và số khối
- Số proton trong hạt nhân nguyên tử bằng số đơn vị điện tích hạt nhân, kí hiệu là Z.
Ví dụ: Hạt nhân nguyên tử Na có 11 proton nên số đơn vị điện tích hạt nhân là Z = 11.
- Tổng số proton và neutron trong hạt nhân của một nguyên tử được gọi là số khối (hay số nucleon), kí hiệu là A.
A = Z + số neutron
- Ví dụ:
Nguyên tử sodium (Na) có 11 proton, 12 neutron. Suy ra:
+ Nguyên tử sodium có số đơn vị điện tích hạt nhân = số proton = 11.
+ Số khối A = 11 + 12 = 23.
>>> Xem toàn bộ:
- Lý thuyết Hóa 10 Kết nối tri thức
- Soạn Hóa 10 Kết nối tri thức
- Sơ đồ tư duy Hóa 10 Kết nối tri thức
- Trắc nghiệm Hóa 10 Kết nối tri thức
-------------------------------------------
Trên đây Toploigiai đã cùng các bạn Tóm tắt Lý thuyết Hóa học 10 Kết nối tri thức Bài 1: Thành phần nguyên tử theo chương trình Sách mới ngắn gọn nhất. Mời các bạn hãy click ngay vào trang chủ Toploigiai để tham khảo và chuẩn bị bài cho năm học mới Lớp 10 nhé. Chúc các bạn học tốt.
Từ khóa » Cấu Tạo Của Nguyên Tử Lớp 10
-
Lý Thuyết Thành Phần Nguyên Tử, Kích Thước Và Khối Lượng Hóa ...
-
Cấu Tạo Nguyên Tử - Hóa Học Lớp 10 - Baitap123
-
Lý Thuyết Thành Phần Nguyên Tử | SGK Hóa Lớp 10
-
Hoá Học 10 Bài 1: Thành Phần Nguyên Tử - Lý Thuyết - HOC247
-
Hóa 10 Bài Thành Phần Nguyên Tử
-
Lý Thuyết Cấu Tạo Vỏ Nguyên Tử Hóa 10 Và Bài Tập Vận Dụng
-
Cấu Tạo Vỏ Nguyên Tử - Lý Thuyết Và Các Dạng Bài Tập Thường Gặp
-
Thành Phần Cấu Tạo Nguyên Tử Là Gì? Bài Tập Cấu Tạo ... - VietChem
-
Soạn Hoá Học 10 Bài 1: Thành Phần Nguyên Tử
-
Hoá Học 10 Bài 1: Thành Phần Nguyên Tử - Dạy Học Mới
-
Tất Tần Tật Lý Thuyết Cấu Tạo Vỏ Nguyên Tử Chuẩn Nhất - CungHocVui
-
Tóm Tắt Lý Thuyết Hóa Học 10 - Chương 1: Nguyên Tử
-
Hóa Học 10 Bài 4: Cấu Tạo Vỏ Nguyên Tử