Lý Thuyết Về Sự điện Li. | SGK Hóa Lớp 11
Có thể bạn quan tâm
I. ĐỊNH NGHĨA
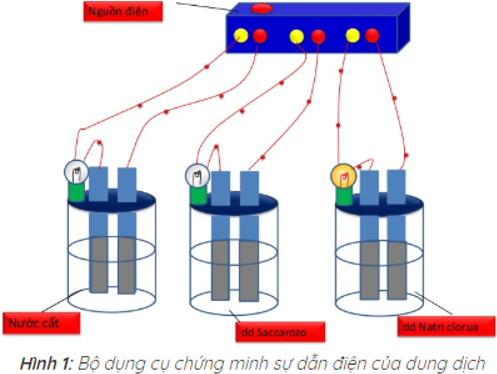
=> Kết quả thí nghiệm cho thấy chỉ có bóng đèn ở cốc đựng dung dịch NaCl sáng. Vậy dung dịch NaCl dẫn điện, còn nước cất và dung dịch saccarozo không dẫn điện.
- Sự điện li là quá trình phân li các chất trong nước hoặc khi nóng chảy thành ion.
- Dung dịch (dd) dẫn điện được là do trong dung dịch của chúng có các hạt mang điện tích chuyển động tự do được gọi là các ion.
- Chất điện li là những chất khi tan trong nước phân li ra ion.
- Axit, bazơ, muối đều là những chất điện li.
II. PHÂN LOẠI
1.Chất điện li mạnh
- Là chất khi tan trong nước, các phân tử hòa tan phân li hoàn toàn.
VD:
Na2SO4 → 2Na+ + SO42-
KOH → K+ + OH-
HNO3 → H+ + NO3–
- Các axit mạnh, bazơ mạnh và hầu hết các muối là chất điện li mạnh.
2. Chất điện li yếu
- Là chất khi tan trong nước, số phân tử hòa tan phân li một phần, phần còn lại vẫn tồn tại dưới dạng phân tử trong dung dịch. Các axit yếu, bazơ yếu và một số muối là chất điện li yếu.
VD: CH3COOH ↔ CH3COO- + H+
3. Chất không điện li
- Là những chất khi tan trong nước không phân li ra ion.
VD: Dung dịch đường, dung dịch rượu, ...
III. CÂN BẰNG ĐIỆN LI
- Sự phân li của các chất điện li yếu là quá trình thuận nghịch. Khi tốc độ phân li của phân tử chất điện li (phản ứng thuận) bằng tốc độ kết hợp giữa các ion thành phân tử chất điện li (phản ứng nghịch) thì cân bằng của quá trình điện li được thiết lập.
Độ điện li: (α) : α = \(\frac{n}{{{n_o}}}\) = \(\frac{C}{{{C_o}}}\)
Với : n là số phân tử phân li ra ion, nolà số phân tử hòa tan.
C là nồng độ mol chất tan phân li thành ion, Co là nồng độ mol chất hòa tan.
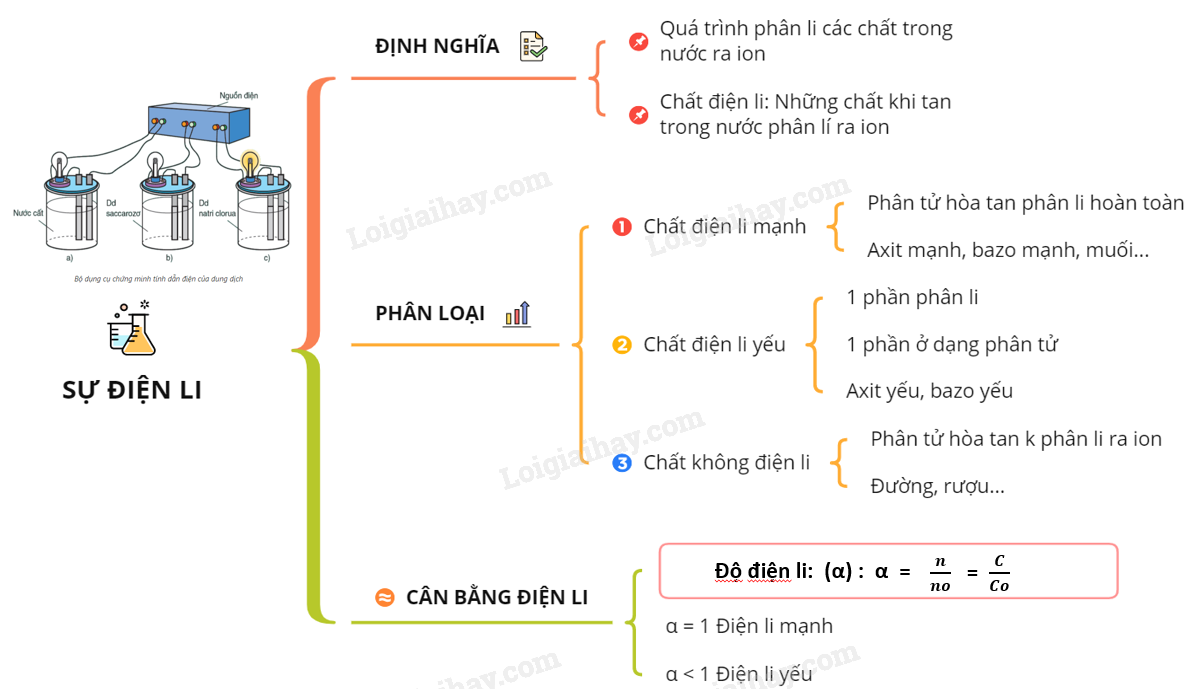
Sơ đồ tư duy: Sự điện li.
Từ khóa » Chất điện Li
-
Chất điện Li – Wikipedia Tiếng Việt
-
Điện Li – Wikipedia Tiếng Việt
-
Sự điện Li Là Gì? Lý Thuyết Và Giải Bài Tập Chi Tiết - Monkey
-
Chất điện Li Là Gì? Sự điện Li, Hóa Học Phổ Thông
-
Các Dạng Bài Tập Hoá 11 Chương Sự Điện Li Cần Nắm Vững
-
Lý Thuyết Sự điện Li - Thầy Dũng Hóa
-
Bài Tập Sự điện Li - Thầy Dũng Hóa
-
KHÁI NIỆM VỀ CHẤT ĐIỆN LI, SỰ ĐIỆN LI. PHÂN LOẠI CHẤT ĐIỆN ...
-
Phương Trình điện Li Là Gì ? Phương Trình Của Chất điện Li Mạnh, Chất ...
-
Sự điện Li – Phân Loại Chất điện Li – GV Đặng Xuân Chất – Hóa 11
-
Sự điện Li Hóa 11 - Lý Thuyết Và Một Số Dạng Bài Tập
-
I. Hiện Tượng điện Li - Củng Cố Kiến Thức
-
Chất Nào Sau đây Là Chất điện Li Mạnh? - Luật Hoàng Phi
-
Sự điện Li: Phân Loại Chất điện Li Mạnh, Chất điện Li Yếu - Hóa 11 Bài 1