Một Dung Dịch Có [H ] = 0,01 OM. Tính [OH-] Và PH Của Dung ... - Hoc24
Có thể bạn quan tâm
HOC24
Lớp học Học bài Hỏi bài Giải bài tập Đề thi ĐGNL Tin tức Cuộc thi vui Khen thưởng- Tìm kiếm câu trả lời Tìm kiếm câu trả lời cho câu hỏi của bạn
Lớp học
- Lớp 12
- Lớp 11
- Lớp 10
- Lớp 9
- Lớp 8
- Lớp 7
- Lớp 6
- Lớp 5
- Lớp 4
- Lớp 3
- Lớp 2
- Lớp 1
Môn học
- Toán
- Vật lý
- Hóa học
- Sinh học
- Ngữ văn
- Tiếng anh
- Lịch sử
- Địa lý
- Tin học
- Công nghệ
- Giáo dục công dân
- Tiếng anh thí điểm
- Đạo đức
- Tự nhiên và xã hội
- Khoa học
- Lịch sử và Địa lý
- Tiếng việt
- Khoa học tự nhiên
- Hoạt động trải nghiệm
- Hoạt động trải nghiệm, hướng nghiệp
- Giáo dục kinh tế và pháp luật
Chủ đề / Chương
Bài học
HOC24
 Khách vãng lai Đăng nhập Đăng ký Khám phá Hỏi đáp Đề thi Tin tức Cuộc thi vui Khen thưởng
Khách vãng lai Đăng nhập Đăng ký Khám phá Hỏi đáp Đề thi Tin tức Cuộc thi vui Khen thưởng - Tất cả
- Toán
- Vật lý
- Hóa học
- Sinh học
- Ngữ văn
- Tiếng anh
- Lịch sử
- Địa lý
- Tin học
- Công nghệ
- Giáo dục công dân
- Tiếng anh thí điểm
- Hoạt động trải nghiệm, hướng nghiệp
- Giáo dục kinh tế và pháp luật
Câu hỏi
Hủy Xác nhận phù hợp Chọn lớp Tất cả Lớp 12 Lớp 11 Lớp 10 Lớp 9 Lớp 8 Lớp 7 Lớp 6 Lớp 5 Lớp 4 Lớp 3 Lớp 2 Lớp 1 Môn học Toán Vật lý Hóa học Sinh học Ngữ văn Tiếng anh Lịch sử Địa lý Tin học Công nghệ Giáo dục công dân Tiếng anh thí điểm Đạo đức Tự nhiên và xã hội Khoa học Lịch sử và Địa lý Tiếng việt Khoa học tự nhiên Hoạt động trải nghiệm Hoạt động trải nghiệm, hướng nghiệp Giáo dục kinh tế và pháp luật Mới nhất Mới nhất Chưa trả lời Câu hỏi hay
- Park 24
Một dung dịch có [H+] = 0,01 OM. Tính [OH-] và pH của dung dịch. Môi trường của dung dịch này là axit, trung tính hay kiềm ? Hãy cho biết màu của quỳ tím trong dung dịch này.
Xem chi tiết Lớp 11 Hóa học Chương 1. Sự điện li 1 0 Gửi Hủy
Gửi Hủy  Chipu khánh phương 28 tháng 6 2016 lúc 16:17
Chipu khánh phương 28 tháng 6 2016 lúc 16:17 [H+] = 0,01M = 10-2M => pH = 2[OH-] = 10-14 / 10-2M =10-12Dung dịch có pH = 2 < 7 => môi trường axit, quỳ tím có màu đỏ.
Đúng 1 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Bài 2
Một dung dịch có [H+] = 0,01 OM. Tính [OH-] và pH của dung dịch. Môi trường của dung dịch này là axit, trung tính hay kiềm ? Hãy cho biết màu của quỳ tím trong dung dịch này.
Xem chi tiết Lớp 11 Hóa học Bài 5: Luyện tập về axit-bazo-muối; phản ứng trao... 2 0 Gửi Hủy
Gửi Hủy  Hai Binh 17 tháng 4 2017 lúc 18:07
Hai Binh 17 tháng 4 2017 lúc 18:07  Gửi Hủy
Gửi Hủy  Nguyễn Đinh Huyền Mai 18 tháng 4 2017 lúc 17:29
Nguyễn Đinh Huyền Mai 18 tháng 4 2017 lúc 17:29  Gửi Hủy
Gửi Hủy 
- Nguyễn Hoàng Nam
Một dung dịch có [H+] = 0,010 M. Tính [OH-] và pH của dung dịch. Môi trường của dung dịch này là axit, trung tính hay kiềm? Hãy cho biết màu của quỳ trong dung dịch này?
Xem chi tiết Lớp 11 Hóa học 1 0 Gửi Hủy
Gửi Hủy  Ngô Quang Sinh
Ngô Quang Sinh  6 tháng 6 2018 lúc 7:20
6 tháng 6 2018 lúc 7:20 [H+] = 0,010M = 10-2M ⇒ pH = -log[H+] = -log(1,0.10-2) = 2
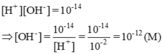
Môi trường của dung dịch này là axit (pH < 7)
Cho quỳ tím vào dung dịch này quỳ sẽ chuyển thành màu đỏ
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Bình Trần Thị
-
một dung dịch có \(\left[H^+\right]=0,010M\) . Tính \(\left[OH^-\right]\) và pH của dung dịch . Môi trường của dung dịch là axit , trung tính hay kiềm ? hãy cho biết màu của quỳ tím trong dung dịch này .
Xem chi tiết Lớp 11 Hóa học Chương 1. Sự điện li 1 0 Gửi Hủy
Gửi Hủy  Vũ Thị Thương 18 tháng 9 2016 lúc 16:08
Vũ Thị Thương 18 tháng 9 2016 lúc 16:08 [OH-]=1.10^-14/0.01=10^-12 (M) tính Ph=log[H+] từ kết quả của Ph xem nó lớn hơn 7 hay j xong suy ra môi trường ,môi trường axit thì quỳ đỏ môi trường kiềm quy xanh trung tính ko màu
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Đây Nie
a,Tính pH của dung dịch NaOH 0,01 (M). Dung dịch này làm quỳ tím và phenolphtalein chuyển sang màu gì?
b, Tính pH của dung dịch HCl 0,01 (M). Dung dịch này làm quỳ tím và phenolphtalein đổi sang màu gì
Xem chi tiết Lớp 11 Hóa học Bài 3: Sự điện li của H2O - pH - Chất chỉ thị axit... 1 0 Gửi Hủy
Gửi Hủy  hnamyuh
hnamyuh  2 tháng 1 2021 lúc 17:35
2 tháng 1 2021 lúc 17:35 a)
\([OH^-] = C_{M_{NaOH}} = 0,01M\\ [H^+] = \dfrac{10^{-14}}{[OH^-]} = 10^{-12}M\\ \Rightarrow pH = -log([H^+]) = 12\)
Dung dịch này làm quỳ tím hóa xanh, làm dung dịch phenolphtalein chuyển sang màu đỏ.
b)
\([H^+] = C_{M_{HCl}} = 0,01M\\ \Rightarrow pH = -log([H^+]) = -log(0,01) = 2\)
Dung dịch này làm quỳ tím hóa đỏ, không làm đổi màu dung dịch phenolphtalein.
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Diệu 11c4 Thái Thi
Một dung dịch có [H+] = 0,020 M.
a. Tính [OH-] và pH của dung dịch.
b. Hãy cho biết màu của quỳ trong dung dịch này. Giải thích?
Xem chi tiết Lớp 11 Hóa học Bài 13: Luyện tập tính chất của nitơ, photpho và h... 0 0 Gửi Hủy
Gửi Hủy 
- Bình Trần Thị
-
một dung dịch có \(\left[OH^-\right]=1,5\times10^{-5}M\) . Môi trường của dung dịch này là axit , trung tính hay kiềm ?
Xem chi tiết Lớp 11 Hóa học Chương 1. Sự điện li 1 0 Gửi Hủy
Gửi Hủy  Tsunayoshi Trần 9 tháng 9 2016 lúc 16:54
Tsunayoshi Trần 9 tháng 9 2016 lúc 16:54 Mình không chắc lắm, bạn tham khảo thử nhé!
pOH = -log(1,5x10-5) = 4,8
pH = 14 - 4,8 = 9,2 → môi trường của dung dịch là kiềm
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Nguyễn Hoàng Nam
Một dung dịch có [OH- ]= 1,5.10-5. Môi trường của dung dịch này là:
A. Axit ; C. Kiềm
B. Trung tính ; D. Không xác định được
Xem chi tiết Lớp 11 Hóa học 1 0 Gửi Hủy
Gửi Hủy  Ngô Quang Sinh
Ngô Quang Sinh  9 tháng 4 2019 lúc 4:23
9 tháng 4 2019 lúc 4:23 - Đáp án C
- Từ [OH-]= 1,5.10-5 (M) suy ra:
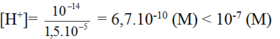
Vậy môi trường của dung dịch là kiềm.
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Ngọcc Ly
Một dung dịch có [OH-] = 1,0.10 -5 M. Môi trường của dung dịch này là: A. Axit B. Không xác định được C. Trung tính D. Kiềm
Xem chi tiết Lớp 11 Hóa học 2 0 Gửi Hủy
Gửi Hủy  ๖ۣۜDũ๖ۣۜN๖ۣۜG
๖ۣۜDũ๖ۣۜN๖ۣۜG  22 tháng 12 2021 lúc 14:10
22 tháng 12 2021 lúc 14:10 Có [OH-] = 10-5
=> pH = 14 - 5 = 9 > 7
=> Môi trường dung dịch là kiềm
=>D
Đúng 1 Bình luận (0) Gửi Hủy
Gửi Hủy  Nguyễn Lê Phước Thịnh CTV
Nguyễn Lê Phước Thịnh CTV  22 tháng 12 2021 lúc 14:07
22 tháng 12 2021 lúc 14:07 Chọn C
Đúng 1 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Dương Thanh Chúc
1 dung dịch có nồng độ ion OH- = 0,001 m cho biết dung dịch trên là acid base hay trung tính, màu của quỳ tím trong dung dịch
Xem chi tiết Lớp 11 Hóa học Bài 3: Sự điện li của H2O - pH - Chất chỉ thị axit... 1 0 Gửi Hủy
Gửi Hủy  GV Nguyễn Trần Thành Đạt Giáo viên 4 tháng 11 2023 lúc 9:18
GV Nguyễn Trần Thành Đạt Giáo viên 4 tháng 11 2023 lúc 9:18 \(\left[OH^-\right]=0,001M\\ \Rightarrow pH=14-pOH=14+log\left[OH^-\right]=14+log\left[0,001\right]=14-3=11\)
Đúng 2 Bình luận (3) Gửi Hủy
Gửi Hủy Từ khóa » Nồng độ Oh- Của Dung Dịch Có H+ = 0 0001m Là
-
Một Dung Dịch Có [H+] = 0,001 M. Tính [OH–] Và PH Của Dung Dịch?
-
Một Dd Có Nồng độ H+ Bằng 0001M Thì PH Và [OH-] Của Dd Này L
-
Một Dung Dịch Có Nồng độ Ion H+ Là 0001 (M) Ta Tính PH Của Dung Dịch
-
Một Dung Dịch Có [H+] = 0010 M. Tính [OH-] Và PH Của ... - Khóa Học
-
Một Dung Dịch Có [H+] = 0001 M. Tính [OH–] Và PH Của Dung Dịch?
-
Nồng độ Oh- Của Dung Dịch Có H+ = 0 0001m Là
-
Một Dung Dịch Có [H + ] = 0001 M. Tính [OH
-
Một Dung Dich Có Nồng độ H+ Bằng 0,001M Thì PH Và ... - MTrend
-
Bài Tập Hóa Học Lớp 11 - Lazi
-
Một Dung Dịch Có Nồng độ Ion H+ Là 0001 (M) Ta Tính PH Của Dung Dịch
-
Công Thức Tính PH Và Hướng Dẫn Giải Bài Tập Về độ PH
-
Một Dung Dịch Có Nồng độ Ion H+ Là 0001 (M) Ta Tính PH Của Dung Dịch
-
Dung Dịch X Có H+ 0,001M PH Của Dung Dịch X Là - Hỏi Đáp