Có thể bạn quan tâm
Nội dung
chuyển sang thanh bên ẩn- Đầu
- Bài viết
- Thảo luận
- Đọc
- Sửa đổi
- Sửa mã nguồn
- Xem lịch sử
- Đọc
- Sửa đổi
- Sửa mã nguồn
- Xem lịch sử
- Các liên kết đến đây
- Thay đổi liên quan
- Liên kết thường trực
- Thông tin trang
- Trích dẫn trang này
- Tạo URL rút gọn
- Tải mã QR
- Tạo một quyển sách
- Tải dưới dạng PDF
- Bản để in ra
- Wikimedia Commons
- Khoản mục Wikidata
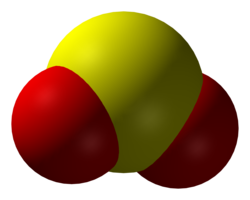
| Lưu huỳnh dioxide | |
|---|---|
 | |
 | |
| Tên khác | Sulfur dioxideLưu huỳnh(IV) OxideSunfurơ anhydride |
| Nhận dạng | |
| Số CAS | 7446-09-5 |
| PubChem | 1119 |
| Số EINECS | 231-195-2 |
| KEGG | D05961 |
| MeSH | Sulfur+dioxide |
| ChEBI | 18422 |
| ChEMBL | 1235997 |
| Số RTECS | WS4550000 |
| Ảnh Jmol-3D | ảnh |
| SMILES | đầy đủ
|
| InChI | đầy đủ
|
| Tham chiếu Beilstein | 3535237 |
| Tham chiếu Gmelin | 1443 |
| UNII | 0UZA3422Q4 |
| Thuộc tính | |
| Công thức phân tử | SO2 |
| Khối lượng mol | 64,0648 g/mol |
| Bề ngoài | khí không màu |
| Khối lượng riêng | 2,551 g/L, khí |
| Điểm nóng chảy | −72,4 °C (200,8 K; −98,3 °F) |
| Điểm sôi | −10 °C (263 K; 14 °F) |
| Độ hòa tan trong nước | 9,4 g/100 mL (25 ℃) |
| Độ axit (pKa) | 1,81 |
| Cấu trúc | |
| Hình dạng phân tử | Bent 120°[1] |
| Mômen lưỡng cực | 1,63 D |
| Các nguy hiểm | |
| Phân loại của EU | độc hại |
| NFPA 704 |
|
| Chỉ dẫn R | R23 R34 |
| Chỉ dẫn S | (S1/2) S9 S26 S36/37/39 S45 |
| Điểm bắt lửa | không cháy |
| Các hợp chất liên quan | |
| Hợp chất liên quan | Lưu huỳnh monoxideLưu huỳnh trioxide |
| Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). Tham khảo hộp thông tin | |
Lưu huỳnh dioxide (hay còn gọi là anhydride sunfurơ, lưu huỳnh(IV) Oxide, sulfur dioxide) là một hợp chất hóa học với công thức SO2. Chất khí này là sản phẩm chính của sự đốt cháy hợp chất lưu huỳnh và nó là một mối lo môi trường rất đáng kể. SO2 thường được mô tả là "mùi hôi của lưu huỳnh bị đốt cháy". Lưu huỳnh dioxide là một khí vô cơ không màu, nặng hơn không khí. Nó có khả năng làm vẩn đục nước vôi trong, làm mất màu dung dịch brom và làm mất màu cánh hoa hồng.
Tính chất hóa học
[sửa | sửa mã nguồn]Lưu huỳnh dioxide là một Oxide acid, tan trong nước tạo thành dung dịch acid yếu H2SO3.
S + O2 t0→ SO2 SO2 + H2O → H2SO3SO2 là chất khử khi tác dụng một chất oxy hóa mạnh:
SO2 + Br2 + 2H2O → 2HBr + H2SO4 (Phản ứng làm mất màu nước brom) 5SO2 + 2KMnO4 + 2H2O → K2SO4 + 2MnSO4 + 2H2SO4SO2 là chất oxy hóa khi tác dụng với chất khử mạnh hơn
SO2 + 2H2S → 3S + 2H2O SO2 + 2Mg → S + 2MgOTác hại
[sửa | sửa mã nguồn]Lưu huỳnh dioxide là một trong những chất gây ô nhiễm môi trường. Nó sinh ra như là sản phẩm phụ trong quá trình đốt cháy than đá, dầu, khí đốt.
Nó là một trong những chất gây ra mưa axít ăn mòn các công trình, phá hoại cây cối, biến đất đai thành hoang mạc.
Khí SO2 gây bệnh cho người như viêm phổi, đau mắt,viêm đường hô hấp...
Điều chế
[sửa | sửa mã nguồn]- Trong phòng thí nghiệm:
Na2SO3 + H2SO4 → Na2SO4 + H2O + SO2↑
- Trong công nghiệp:
- Đốt lưu huỳnh: S + O2 (t°) → SO2
- Đốt pyrit sắt (FeS2): 4FeS2 + 11O2 → 2Fe2O3 + 8SO2↑
Tham khảo
[sửa | sửa mã nguồn]- ^ "Table of Geometries based on VSEPR". Truy cập ngày 26 tháng 9 năm 2015.
| |
|---|---|
| |
Hợp chất hóa họcCổng thông tin:
|
Bài viết liên quan đến hóa học này vẫn còn sơ khai. Bạn có thể giúp Wikipedia mở rộng nội dung để bài được hoàn chỉnh hơn. |
- x
- t
- s
- Sơ khai hóa học
- Oxide acid
- Khí công nghiệp
- Chất bảo quản
- Hợp chất lưu huỳnh
- Oxide
- Tất cả bài viết sơ khai
Từ khóa » Nguyên Tử Khối So2
-
Hãy Tính Phân Tử Khối Của SO2 - Lê Minh Trí - Hoc247
-
Phân Tử Khối Của SO2 Là
-
Phân Tử Khối Của So2 Là
-
SO2 (Lưu Huỳnh Đioxit) Khối Lượng Mol - ChemicalAid
-
Phân Tử Khối Của Khí Lưu Huỳnh đioxit SO2 Bằng Bao Nhiêu đvC
-
Phân Tử Khối Của So2 Là
-
1Tính Số Phân Tử SO2,số Nguyên Tử S Và Số Nguyên Tử O Có Trong 12 ...
-
Công Thức Cách Tính Phân Tử Khối | Hóa Học Lớp 6 7 8 9 - Sáng Tạo Xanh
-
Lưu Huỳnh đioxit Có CTHH Là SO2. Ta Nói Thành Phần Phân Tử Của Lư
-
Tính Phân Tử Khối Của:H2 Nano3 So2 Naoh
-
1 Khí Sunfurơ SO2 Là Chất Gây ô Nhiễm Không Khí, Là Một Trong Các ...
-
Phân Tử Khối Của KMnO4 Là A. 158. B. 226. C. 256. D. 326. Câu 97
-
Câu Hỏi Cho Biết Cách Ghi So2 = 64 Diễn đạt ý Có 64 Phân Tử Khí
