Nguyên Tố Hóa Học Là Gì? Lý Thuyết Về Nguyên Tố Hóa Học
Có thể bạn quan tâm
Khi mới bắt đầu làm quen với môn Hóa thì các nguyên tố hóa học là một “chìa khóa” quan trọng mà tất cả các em học sinh đều phải ghi nhớ để học tốt hơn. Vậy nguyên tố hóa học là gì? Có bao nhiêu nguyên tố tồn tại được con người phát hiện? Các em hãy cùng Team Marathon Education tìm hiểu những nội dung này trong bài viết sau.
>>> Xem thêm: Lý Thuyết Bảng Nguyên Tố Hóa Học Và Bài Ca Hóa Trị
Nguyên tố hóa học là gì? Có bao nhiêu nguyên tố hóa học?

Định nghĩa
Nguyên tố hóa học là tập hợp các nguyên tử cùng loại, có cùng số proton trong hạt nhân. Mỗi nguyên tố được xác định theo số proton trong hạt nhân nguyên tử.
Nếu một nguyên tố được thêm nhiều proton hơn vào một nguyên tử thì có thể tạo ra nguyên tố mới. Đồng thời, các nguyên tử của cùng một nguyên tố sẽ có cùng số hiệu nguyên tử (ký hiệu là Z).
Có bao nhiêu nguyên tố hóa học?
Trong thời buổi khoa học ngày càng phát triển như hiện nay, con người đã tìm ra được rất nhiều nguyên tố khác nhau. Hiện nay, các nguyên tố hóa học được sắp xếp dựa theo chiều tăng dần số proton trong hạt nhân nguyên tử.
Bảng tuần hoàn hóa học hiện có 118 nguyên tố hóa học được công nhận và phân chia thành nhiều nhóm khác nhau như nhóm kim loại (có nhóm kim loại kiềm, nhóm kim loại kiềm thổ, nhóm kim loại chuyển tiếp,…), nhóm phi kim, nhóm khí hiếm và nhóm nguyên tố đất hiếm.
Phân loại nguyên tố hóa học
Nguyên tố kim loại
- Đây là những nguyên tố thường ở dạng đơn chất, thể rắn trong điều kiện thường (trừ một số chất là thủy ngân, gali và xeri ở thể lỏng).
- Hiện có tất cả 81 nguyên tố kim loại trong bảng tuần hoàn hóa học.
- Oxit của các nguyên tố kim loại thường là oxit bazơ hoặc oxit lưỡng tính hoặc oxit axit khi kim loại có mức oxi hóa cao.
- Nguyên tố kim loại thường có 1e đến 3e ở lớp ngoài cùng.
Nguyên tố phi kim
- Đây là những nguyên tố thường ở dạng đơn chất, thể khí.
- Các nguyên tố phi kim bao gồm F, Cl, Br, I, O, S, Se, N, P, C, He, Ne, Ar, Kr, Xe, Rn.
- Oxit của các nguyên tố phi kim là oxit axit hoặc oxit trung tính.
- Nguyên tố phi kim thường có 4e đến 7e ở lớp ngoài cùng, trừ các loại khí hiếm có 8e ở lớp ngoài cùng (trạng thái bền vững).
Nguyên tố á kim
- Đây là những nguyên tố thường ở dạng đơn chất và là những chất bán dẫn.
- Các nguyên tố á kim có tính chất trung gian của cả kim loại và phi kim.
- Các nguyên tố á kim bao gồm bo, silic, gemani, asen và telu.
- Oxit của các nguyên tố á kim là oxit lưỡng tính.
Ký hiệu hóa học

Mỗi nguyên tố hóa học được biểu diễn bằng 1 ký hiệu duy nhất gọi là kí hiệu hóa học. Các ký hiệu này do tổ chức quốc tế quy ước và thường lấy từ 1 – 2 chữ cái ở đầu tên nguyên tố. Đồng thời, các nguyên tố này có thể được phiên âm bằng tiếng La tinh, tiếng Anh hay sử dụng các ngôn ngữ khác như tiếng Đức, tiếng Pháp, tiếng Nga,…
Mỗi nguyên tố thường được biểu thị bằng tên, ký hiệu hoặc số nguyên tử của nguyên tố đó. Trong đó, các ký hiệu của một nguyên tố thường bắt đầu bằng chữ cái in hoa của nguyên tố đó như Kali (kí hiệu là K), Hidro (kí hiệu là H),… Nếu sau ký tự đầu tiên vẫn còn sử dụng chữ cái khác thì chữ cái này sẽ được viết thường.
Ví dụ:
- Nguyên tố có 1 chữ cái: Nitơ (N), Kali (K), Oxi (O),…
- Nguyên tố có 2 chữ cái: Đồng (Cu), Nhôm (Al), Sắt (Fe), Kẽm (Zn),…
Dưới đây là bảng ký hiệu hoá học các nguyên tố Tiếng Anh và Tiếng Việt đầy đủ và chi tiết giúp các em nắm được một số kí hiệu hóa học các nguyên tố.
| Tên Tiếng Anh | Tên Tiếng Việt | Kí hiệu nguyên tố | Số Proton |
| actinium | actini | Ac | 89 |
| americium | americi | Am | 95 |
| stibium | antimon | Sb | 51 |
| argonum | agon | Ar | 18 |
| arsenicum | asen | As | 33 |
| astatium | astatin | At | 85 |
| baryum | bari | Ba | 56 |
| berkelium | berkeli | Bk | 97 |
| beryllium | berylli | Be | 4 |
| bismuthum | bitmut | Bi | 83 |
| bohrium | bohri | Bh | 107 |
| borum | bo | B | 5 |
| bromum | brôm | Br | 35 |
| carboneum | cacbon | C | 6 |
| cerium | xeri | Ce | 58 |
| caesium | xêzi | Cs | 55 |
| stannum | thiếc | Sn | 50 |
| curium | curium | Cm | 96 |
| darmstadtium | darmstadti | Ds | 110 |
| kalium | kali | K | 19 |
| dubnium | dubni | Db | 105 |
| nitrogenium | nitơ | N | 7 |
| dysprosium | dysprosi | Dy | 66 |
| einsteinium | einsteini | Es | 99 |
| erbium | erbi | Er | 68 |
| europium | europi | Eu | 63 |
| fermium | fermi | Fm | 100 |
| fluorum | flo | F | 9 |
| phosphorus | phốtpho | P | 15 |
| francium | franxi | Fr | 87 |
| gadolinium | gadolini | Gd | 64 |
| gallium | galli | Ga | 31 |
| germanium | germani | Ge | 32 |
| hafnium | hafni | Hf | 72 |
| hassium | hassi | Hs | 108 |
| helium | heli | He | 2 |
| aluminium | nhôm | Al | 13 |
| holmium | holmi | Ho | 67 |
| magnesium | magiê | Mg | 12 |
| chlorum | clo | Cl | 17 |
| chromium | crom | Cr | 24 |
| indium | indi | In | 49 |
| iridium | iridi | Ir | 77 |
| iodum | iốt | I | 53 |
| cadmium | cadmi | Cd | 48 |
| californium | californi | Cf | 98 |
| cobaltum | coban | Co | 27 |
| krypton | krypton | Kr | 36 |
| silicium | silic | Si | 14 |
| oxygenium | ôxy | O | 8 |
| lanthanum | lantan | La | 57 |
| laurentium | lawrenci | Lr | 103 |
| lithium | liti | Li | 3 |
| lutetium | luteti | Lu | 71 |
| manganum | mangan | Mn | 25 |
| cuprum | đồng | Cu | 29 |
| meitnerium | meitneri | Mt | 109 |
| mendelevium | mendelevi | Md | 101 |
| molybdaenum | molypden | Mo | 42 |
| neodymium | neodymi | Nd | 60 |
| neon | neon | Ne | 10 |
| neptunium | neptuni | Np | 93 |
| niccolum | niken | Ni | 28 |
| niobium | niobi | Nb | 41 |
| nobelium | nobeli | No | 102 |
| plumbum | chì | Pb | 82 |
| osmium | osmi | Os | 76 |
| palladium | paladi | Pd | 46 |
| platinum | bạch kim | Pt | 78 |
| plutonium | plutoni | Pu | 94 |
| polonium | poloni | Po | 84 |
| praseodymium | praseodymi | Pr | 59 |
| promethium | promethi | Pm | 61 |
| protactinium | protactini | Pa | 91 |
| radium | radi | Ra | 88 |
| radon | radon | Rn | 86 |
| rhenium | rheni | Re | 75 |
| rhodium | rhodi | Rh | 45 |
| roentgenium | roentgeni | Rg | 111 |
| hydrargyrum | thủy ngân | Hg | 80 |
| rubidium | rubidi | Rb | 37 |
| ruthenium | rutheni | Ru | 44 |
| rutherfordium | rutherfordi | Rf | 104 |
| samarium | samari | Sm | 62 |
| seaborgium | seaborgi | Sg | 106 |
| selenium | selen | Se | 34 |
| sulphur | lưu huỳnh | S | 16 |
| scandium | scandi | Sc | 21 |
| natrium | natri | Na | 11 |
| strontium | stronti | Sr | 38 |
| argentum | bạc | Ag | 47 |
| tantalum | tantali | Ta | 73 |
| technetium | tecneti | Tc | 43 |
| tellurium | telua | Te | 52 |
| terbium | terbi | Tb | 65 |
| thallium | tali | Tl | 81 |
| thorium | thori | Th | 90 |
| thulium | thuli | Tm | 69 |
| titanium | titan | Ti | 22 |
| uranium | urani | U | 92 |
| vanadium | vanadi | V | 23 |
| calcium | canxi | Ca | 20 |
| hydrogenium | hiđrô | H | 1 |
| wolframium | volfram | W | 74 |
| xenon | xenon | Xe | 54 |
| ytterbium | ytterbi | Yb | 70 |
| yttrium | yttri | Y | 39 |
| zincum | kẽm | Zn | 30 |
| zirconium | zirconi | Zr | 40 |
| aurum | vàng | Au | 79 |
| ferrum | sắt | Fe | 26 |
Nguyên tử khối
Nguyên tử khối là khối lượng của một nguyên tử. Tổ chức Đo lường Thế giới lấy khối lượng của nguyên tử cacbon làm đơn vị đo của nguyên tử khối (thường gọi là đơn vị cacbon, ký hiệu là đvC).
Hướng dẫn cách tính theo công thức hóa học - lớp 8Vì mỗi nguyên tố hóa học khác nhau về số proton nên sẽ có khối lượng nguyên tử khác nhau.
- Đơn vị khối lượng nguyên tử được ký hiệu là u.
- Theo hệ đo lường quốc tế quy ước: 1u = 1/NA (gam) = 1/(1000 NA) kg (NA – Avogadro là số lượng nguyên tử có trong 12g đồng vị Cacbon 12 hay có thể gọi là số nguyên tử có trong 1 mol chất.
Như vậy, với cách tính trên các em có được:
- C = 12 đvC
- O = 16 đvC
- H = 1 đvC
- Na = 23 đvC
- K = 39 đvC
- Ca = 40 đvC
- …

Bảng các nguyên tố hóa học phổ biến
Bảng các nguyên tố hóa học thường gặp
| Ký hiệu | Tên nguyên tố | Số nguyên tử | Khối lượng nguyên tử |
| Fe | Sắt | 26 | 56 |
| Al | Nhôm | 13 | 27 |
| Cu | Đồng | 29 | 64 |
| Zn | Kẽm | 30 | 65 |
| Mn | Mangan | 25 | 55 |
| Ni | Niken | 28 | 59 |
| Cr | Crom | 24 | 52 |
| Ca | Canxi | 20 | 40 |
| K | kali | 19 | 39 |
| S | Lưu huỳnh | 16 | 32 |
| P | Phốt pho | 15 | 31 |
| Mg | Magiê | 12 | 24 |
| Na | Natri | 11 | 23 |
| O | Oxi | 8 | 16 |
| H | Hiđrô | 1 | 1 |
| C | Carbon | 6 | 12 |
| F | Flo | 9 | 19 |
| Cl | Clo | 17 | 35,5 |
| Br | Brôm | 35 | 80 |
| Ag | Bạc | 47 | 108 |
| Pb | Chì | 82 | 207 |
>>> Xem thêm: Lý Thuyết Về Tính Chất Hóa Học Của Oxi
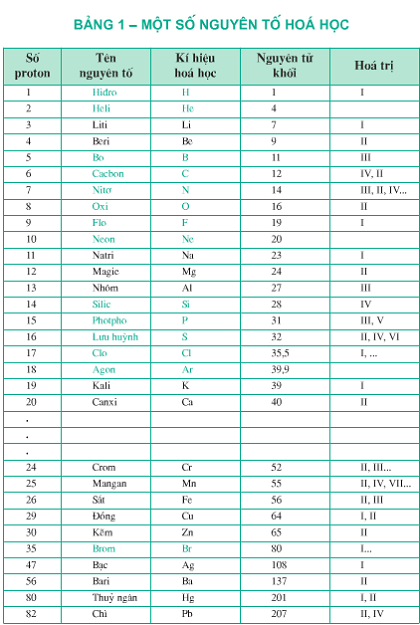
Bảng nguyên tố hóa học lớp 8
Bài tập vận dụng
Bài 1 Trang 20 SGK Hóa 8
Điền đầy đủ các từ hay cụm từ thích hợp.
a. Đáng lẽ nói những ….. loại này, những ….. loại kia, thì trong hóa học nói ….. hóa học này ….. hóa học kia.
Axeton Là Gì? Các Tính Chất Đặc Trưng Và Ứng Dụng Của Axetonb. Những nguyên tử có cùng ….. trong hạt nhân đều là ….. cùng loại, thuộc cùng một ….. hóa học.
Lời giải:
Đáng lẽ nói những nguyên tử loại này, những nguyên tử loại kia thì trong hóa học nói là nguyên tố hóa học này, nguyên tố hóa học kia.
b. Những nguyên tử có cùng số proton trong hạt nhân đều là nguyên tử cùng loại, thuộc cùng một nguyên tố hóa học.
Bài 2 Trang 20 SGK Hóa 8
a. Nguyên tố hóa học là gì?
b. Cách biểu diễn nguyên tố? Cho ví dụ minh họa
Lời giải:
a. Nguyên tố hóa học là tập hợp những nguyên tử cùng loại và có cùng số proton trong hạt nhân.
b. Mỗi nguyên tố hóa học thường được biểu diễn bằng một hoặc hai chữ cái đầu tiên trong tên latinh nguyên tố đó. Chữ cái đầu tiên được viết in hoa, còn được gọi là kí hiệu hóa học.
Ví dụ minh họa: H, Na, Ba, Ca, Al, Fe, Cu…
Bài 3 Trang 20 SGK Hóa 8
a. Các cách viết 2C, 5O, 3Ca có ý nghĩa gì?
b. Hãy diễn đạt các ý sau bằng chữ số và kí hiệu hóa học: ba nguyên tử nitơ, bảy nguyên tử canxi, bốn nguyên tử natri
Lời giải:
a.
- 2C: hai nguyên tử cacbon
- 5O: năm nguyên tử oxi
- 3Ca: ba nguyên tử canxi
b.
- ba nguyên tử nitơ: 3N
- bảy nguyên tử canxi: 7Ca
- bốn nguyên tử natri: 4Na
Bài 4 Trang 20 SGK Hoá 8
Lấy bao nhiêu phần khối lượng của nguyên tử cacbon làm đơn vị cacbon? Nguyên tử khối là gì?
Lời giải:
- Lấy 1/12 khối lượng của nguyên tử cacbon làm đơn vị cacbon.
- Nguyên tử khối được hiểu là khối lượng của một nguyên tử được tính bằng đơn vị cacbon.
Bài 5 Trang 20 SGK Hoá 8
Hãy so sánh nguyên tử magie nặng hay nhẹ hơn bao nhiêu lần so với
a. nguyên tử cacbon
b. nguyên tử lưu huỳnh
c. nguyên tử nhôm
Lời giải:
\begin{aligned} & \small \text{Ta so sánh nguyên tử khối của magie với các nguyên tử cacbon, lưu huỳnh, nhôm.} \\ & \small \text{a. Nguyên tử magie nặng hơn } \frac{24}{12} = 2 \text{ lần nguyên tử cacbon.} \\ & \small \text{b. Nguyên tử magie nhẹ hơn } \frac{24}{32} = \frac34 \text{ lần nguyên tử lưu huỳnh.} \\ & \small \text{c. Nguyên tử magie nhẹ hơn } \frac{24}{27} = \frac89 \text{ lần nguyên tử nhôm.} \end{aligned}Bài 6 Trang 20 SGK Hoá 8
Nguyên tử X nặng gấp 2 lần nguyên tử nitơ. Tính nguyên tử khối và cho biết X thuộc nguyên tố nào? Viết kí hiệu hóa học của nguyên tố đó.
Lời giải:
Nguyên tử khối của nguyên tử nitơ là 14 đvC
Nguyên tử X nặng gấp 2 lần nguyên tử nitơ nên nguyên tử khối của X là 28 đvC.
Vậy X là nguyên tố silic. Kí hiệu hóa học là Si.
Bài 7 Trang 20 SGK Hoá 8
a. Theo giá trị khối lượng tính bằng gam của nguyên tử cacbon trong bài học, hãy tính xem một đơn vị cacbon tương ứng với bao nhiêu gam?
b. Khối lượng tính bằng gam của nguyên tử nhôm là A, B, C hay D?
A. 5,324.10-23g
B. 6,023.10-23g
C. 4,482.10-23g
D. 3,990.10-23g
Lời giải:
\begin{aligned} & \small \text{a. } \\ & \small \text{Theo lý thuyết, khối lượng 1 nguyên tử cacbon (C) là } 1,9926.10^{-23} \ g \text{ và bằng } 12 \ đvC. \\ & \small \text{Vậy khối lượng 1 đvC là } 1 \ đvC = \frac{1,9926.10^{-23}}{12} = 1,66.10^{-24} \ g \\ & \small \text{b. } \\ & \small \text{Khối lượng tính bằng gam của nguyên tử nhôm:} \\ & \small M_{Al} = 27.1,66.10^{-24} = 44,82.10^{-24} \ g = 4,482.10^{-23} \ g \\ & \small \text{Vậy ta chọn đáp án C.} \end{aligned}Bài 8 Trang 20 SGK Hóa 8
Nhận xét sau đây bao gồm 2 ý: “Nguyên tử đơtêri thuộc cùng nguyên tố hóa học với nguyên tử hiđro vì chúng đều có 1 proton trong hạt nhân”. Cho sơ đồ thành phần cấu tạo của 2 nguyên tử như hình vẽ sau:
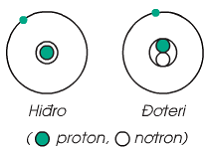
Chọn phương án đúng trong các phương án bên dưới:
A. Ý (1) đúng, ý (2) sai
B. Ý (1) sai, ý (2) đúng
C. Cả 2 đều sai
D. Cả 2 đều đúng
Lời giải:
D là đáp án đúng.
Gia sư Online Học Online Toán 12 Học Online Hóa 10 Học Online Toán 11 Học Online Toán 6 Học Online Toán 10 Học Online Toán 7 Học Online Lý 10 Học Online Lý 9 Học Online Toán 8 Học Online Toán 9 Học Tiếng Anh 6 Học Tiếng Anh 7Tham khảo ngay các khoá học online của Marathon Education
Trên đây là những lý thuyết cơ bản về khái niệm, ký hiệu, nguyên tử khối và phân loại nguyên tố hoá học. Đây là nền tảng để các em học lý thuyết cũng như giải các bài tập về xác định công thức của nguyên tố hoá học, viết phương trình hoá học, tính khối lượng nguyên tố hoá học… Thông qua bài viết, hy vọng rằng các em đã nắm vững những kiến thức cơ bản của nguyên tố hoá học trong bảng tuần hoàn hóa học. Chúc các em gặt hái được nhiều thành công trong học tập!
Hãy liên hệ ngay với Marathon để được tư vấn nếu các em có nhu cầu học online nâng cao kiến thức nhé! Marathon Education chúc các em được điểm cao trong các bài kiểm tra và kỳ thi sắp tới!
Từ khóa » Nguyên Tố Bằng Bao Nhiêu
-
Nguyên Tố Hóa Học – Wikipedia Tiếng Việt
-
Bảng Tuần Hoàn – Wikipedia Tiếng Việt
-
Bảng Nguyên Tử Khối Của Các Chất Thường Gặp Trong Hóa Học
-
Ý Nghĩa Của Bảng Tuần Hoàn Nguyên Tố Hóa Học Đầy Đủ Nhất
-
Bảng Nguyên Tử Khối Của Các Nguyên Tố Hóa Học Và Bài Tập ...
-
Có Bao Nhiêu Nguyên Tố Hóa Học?
-
Bảng Tuần Hoàn Các Nguyên Tố Hóa Học Lớp 8, 9, 10 Mới Nhất
-
Có Bao Nhiêu Nguyên Tố Hóa Học - Sieutonghop
-
Tổng Quan Kiến Thức Về Nguyên Tố Hóa Học - Monkey
-
Phân Tích Các Số Sau Ra Thừa Số Nguyên Tố 70, 115 - TopLoigiai
-
Hiện Nay Có Tất Cả Bao Nhiêu Nguyên Tố Hóa Học?
-
Cách Phân Tích Một Số Ra Thừa Số Nguyên Tố Và Các Dạng Bài Tập - VOH
-
Khi Phân Tích Ra Thừa Số Nguyên Tố 1000! Chứa Thừa Số Nguyên ... - Olm