Nguyên Tử Au Có Bán Kính Và Khối Lượng Mol Nguyên Tử Lần ... - Hoc24
Có thể bạn quan tâm
HOC24
Lớp học Học bài Hỏi bài Giải bài tập Đề thi ĐGNL Tin tức Cuộc thi vui Khen thưởng- Tìm kiếm câu trả lời Tìm kiếm câu trả lời cho câu hỏi của bạn
Lớp học
- Lớp 12
- Lớp 11
- Lớp 10
- Lớp 9
- Lớp 8
- Lớp 7
- Lớp 6
- Lớp 5
- Lớp 4
- Lớp 3
- Lớp 2
- Lớp 1
Môn học
- Toán
- Vật lý
- Hóa học
- Sinh học
- Ngữ văn
- Tiếng anh
- Lịch sử
- Địa lý
- Tin học
- Công nghệ
- Giáo dục công dân
- Tiếng anh thí điểm
- Đạo đức
- Tự nhiên và xã hội
- Khoa học
- Lịch sử và Địa lý
- Tiếng việt
- Khoa học tự nhiên
- Hoạt động trải nghiệm
- Hoạt động trải nghiệm, hướng nghiệp
- Giáo dục kinh tế và pháp luật
Chủ đề / Chương
Bài học
HOC24
 Khách vãng lai Đăng nhập Đăng ký Khám phá Hỏi đáp Đề thi Tin tức Cuộc thi vui Khen thưởng
Khách vãng lai Đăng nhập Đăng ký Khám phá Hỏi đáp Đề thi Tin tức Cuộc thi vui Khen thưởng - Tất cả
- Toán
- Vật lý
- Hóa học
- Sinh học
- Ngữ văn
- Tiếng anh
- Lịch sử
- Địa lý
- Tin học
- Công nghệ
- Giáo dục công dân
- Tiếng anh thí điểm
- Hoạt động trải nghiệm, hướng nghiệp
- Giáo dục kinh tế và pháp luật
Câu hỏi
Hủy Xác nhận phù hợp Chọn lớp Tất cả Lớp 12 Lớp 11 Lớp 10 Lớp 9 Lớp 8 Lớp 7 Lớp 6 Lớp 5 Lớp 4 Lớp 3 Lớp 2 Lớp 1 Môn học Toán Vật lý Hóa học Sinh học Ngữ văn Tiếng anh Lịch sử Địa lý Tin học Công nghệ Giáo dục công dân Tiếng anh thí điểm Đạo đức Tự nhiên và xã hội Khoa học Lịch sử và Địa lý Tiếng việt Khoa học tự nhiên Hoạt động trải nghiệm Hoạt động trải nghiệm, hướng nghiệp Giáo dục kinh tế và pháp luật Mới nhất Mới nhất Chưa trả lời Câu hỏi hay
- Nguyễn Hoàng Nam
Nguyên tử Au có bán kính và khối lượng mol nguyên tử lần lượt là 1,44. 10-10 và 197g/mol. Biết khối lượng riêng của Au là 19,36g/cm3 Hỏi các nguyên tử Au chiếm bao nhiêu phần trăm thể tích trong tinh thể
A . 25%
B . 68%
C . 76%
D. 74%
Xem chi tiết Lớp 0 Hóa học 1 0 Gửi Hủy
Gửi Hủy  Ngô Quang Sinh
Ngô Quang Sinh  22 tháng 3 2017 lúc 13:00
22 tháng 3 2017 lúc 13:00 
 Gửi Hủy
Gửi Hủy 
- Vũ Thảo Uyên Nhi
Nguyên tử Au có bán kính và khối lượng mol nguyên tử lần lượt là 1,44 Ao và 197 g/mol. Biết khối lượng riêng của Au là 19,36g /cm3. Hỏi các nguyên tử Au chiếm bao nhiêu phần trăm trong tinh thể?
Xem chi tiết Lớp 10 Hóa học Bài 1. Thành phần nguyên tử 1 0 Gửi Hủy
Gửi Hủy  Trần Hữu Tuyển
Trần Hữu Tuyển  18 tháng 7 2018 lúc 16:05
18 tháng 7 2018 lúc 16:05 Theo bài ra thể tích của 1 mol Au là \(\dfrac{197}{19,36}\) (g/cm3). Đặt x % là thể tích các nguyên tử Au trong tinh thể, thì thể tích thực của một nguyên tử Au: V=\(\dfrac{197}{19,36}\)×\(\dfrac{x}{100.6,02.10^{23}}\) Mặt khác với bán kính nguyên tử Au là 1,44 x 10−8 cm ta có: V=\(\dfrac{4}{3}.3,14.\left(1,44.10^{-8}\right)^3\left(cm^3\right)\) ⇒ x = 73,95%
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Nguyễn Hoàng Nam
Ở 20oC khối lượng riêng của Au là 19,32 g/cm3. Trong tinh thể Au, các nguyên tử Au là những hình cầu chiếm 75% thể tích toàn khối tinh thể, phần còn lại là các khe rỗng giữa các quả cầu. Khối lượng mol của Au là 196,97. Bán kính nguyên tử gần đúng của Au ở 20oC là:
A. 1,28.10-8 cm.
B. 1,44.10-8 cm.
C. 1,59.10-8 cm
D. 1,75.10-8 cm.
Xem chi tiết Lớp 10 Hóa học 1 0 Gửi Hủy
Gửi Hủy  Ngô Quang Sinh
Ngô Quang Sinh  21 tháng 5 2019 lúc 9:17
21 tháng 5 2019 lúc 9:17 
 Gửi Hủy
Gửi Hủy 
- Nguyễn Hoàng Nam
Ở 20 o C khối lượng riêng của Au là 19 , 32 g / c m 3 . Trong tinh thể Au, các nguyên tử Au là những hình cầu chiếm 75% thể tích toàn khối tinh thể, phần còn lại là các khe rỗng giữa các quả cầu. Khối lượng mol của Au là 196,97. Bán kính nguyên tử gần đúng của Au ở 20 o C là
A. 1 , 28 . 10 - 8 c m
B. 1 , 44 . 10 - 8 c m
C. 1 , 59 . 10 - 8 c m
D. 1 , 75 . 10 - 8 c m
Xem chi tiết Lớp 10 Hóa học 1 0 Gửi Hủy
Gửi Hủy  Ngô Quang Sinh
Ngô Quang Sinh  8 tháng 1 2017 lúc 18:14
8 tháng 1 2017 lúc 18:14 
 Gửi Hủy
Gửi Hủy 
- Nguyễn Hoàng Nam
Ở 20oC khối lượng riêng của Au là 19,32 g/cm3. Trong tinh thể Au, các nguyên tử Au là những hình cầu chiếm 75% thể tích toàn khối tinh thể, phần còn lại là các khe rỗng giữa các quả cầu. Khối lượng mol của Au là 196,97. Bán kính nguyên tử gần đúng của Au ở 20oC là:
A. 1,28.10-8 cm.
B. 1,44.10-8 cm.
C. 1,59.10-8 cm
D. 1,75.10-8 cm.
Xem chi tiết Lớp 10 Hóa học 1 0 Gửi Hủy
Gửi Hủy  Ngô Quang Sinh
Ngô Quang Sinh  4 tháng 6 2017 lúc 14:17
4 tháng 6 2017 lúc 14:17 Xét trong 1 mol Au.
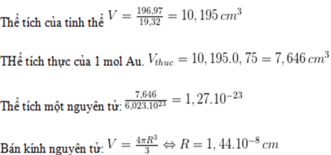
Đáp án B
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Nguyễn Hoàng Nam
Một loại tinh thể nguyên tử, có khối lượng riêng là 19,36g/ cm 3 . Trong đó, các nguyên tử chỉ chiếm 74% thể tích của tinh thể, còn lại là các khe rỗng. Bán kính của nguyên tử là 1,44Å. Tính khối lượng riêng của nguyên tử, từ đó suy ra khối lượng mol nguyên tử.
Xem chi tiết Lớp 10 Hóa học 1 0 Gửi Hủy
Gửi Hủy  Ngô Quang Sinh
Ngô Quang Sinh  8 tháng 2 2019 lúc 9:19
8 tháng 2 2019 lúc 9:19 Khối lượng riêng của nguyên tử là:
D = 19,36.100/74 = 26,16(g/ cm 3 )
Khối lượng của 1 mol nguyên tử :
M = V.D.N = 4/3π r 3 .D.N = 4/3. 3,14. 1 , 44 . 10 - 8 3 .26,16. 6,022. 10 23 ≈ 197 (g/mol)
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Thảo
Nguyên tử Canxi (Ca) có bán kính bằng 1,97×10^-8 cm ,khối lượng mol là 40,08 g/mol,khối lượng riêng 1,55 g/cm3.Trong tinh thể kim loại ,các nguyên tử chiếm bao nhiêu phần trăm thể tích ?
Xem chi tiết Lớp 10 Hóa học 1 0 Gửi Hủy
Gửi Hủy  Út Thảo
Út Thảo  31 tháng 7 2021 lúc 12:53
31 tháng 7 2021 lúc 12:53  bài giải đây nha!
bài giải đây nha!
 Gửi Hủy
Gửi Hủy 
- pham thi huyen tran
một loại tinh thể nguyên tử ,có khối lượng riêng là 19,36g/cm3.trong đó ,các nguyên tử chỉ chiếm 74%nthe63 tích của tinh thể ,còn lại các khe rỗng .bán kính nguyên tử là 1,44 angstrom.
a.tính khối lượng riêng của nguyên tử ,từ đó suy ra khối lượng mol nguyên tử.
b.hạt nhân nguyên tử có 118 no7tron nguyên tử khối được coi bằng tổng khối lượng proton và no7tron .tính số proton.![]()
 Gửi Hủy
Gửi Hủy 
- quangduy
Nguyên tử Au có bán kính và khối lượng mol nguyên tử lần lượt là 1,44Ao và 197 g/mol. Biết khối lượng riêng của Au là 19,36 g/cm3. Hỏi các nguyên tử Au chiếm bao nhiêu phần trăm thể tích trong tinh thể ?
Xem chi tiết Lớp 10 Hóa học Ôn tập cuối học kì II 2 0 Gửi Hủy
Gửi Hủy  Việt Hoa Nguyễn 5 tháng 3 2019 lúc 20:53
Việt Hoa Nguyễn 5 tháng 3 2019 lúc 20:53 73,95 %
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy  Diệu Huyền
Diệu Huyền  13 tháng 9 2019 lúc 18:51
13 tháng 9 2019 lúc 18:51 Theo bài ra thể tích của 1 mol Au là \(\frac{197}{19,36}\left(g/cm^3\right)\)
Đặt x % là thể tích các nguyên tử Au trong tinh thể, thì thể tích thực của một nguyên tử Au:
\(V=\frac{197}{19,36}\times\frac{x}{100\times6,02\times10^{23}}\)
Mặt khác với bán kính nguyên tử Au là 1,44 x 10−8 cm ta có:
\(V=\frac{4}{3}\times3,14\times\left(1,44\times10^{-8}\right)^3cm^3\)
⇒ x = 73,95%
Tham khảo nha !
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy 
- tranbem
Bán kính nguyên tử và khối lượng mol nguyên tử Fe lần lượt là 1,28Ǻ và 56g/mol. Tính khối lượng riêng của Fe biết trong tinh thể, các nguyên tử Fe chiếm 74% thể tích, còn lại là phần rỗng
Xem chi tiết Lớp 10 Hóa học Chương 1. Nguyên tử 1 0 Gửi Hủy
Gửi Hủy  Lê Nguyên Hạo
Lê Nguyên Hạo  13 tháng 8 2016 lúc 6:55
13 tháng 8 2016 lúc 6:55 hể tích của 1 phân tử Fe V(Fe) = 4π/3. r˄3 = 4π/3 . (1,28.10˄-8)˄3 = 8,78.10˄-24 cm˄3 Thể tích của 1 mol Fe: V = V(Fe).Na/74% = 8,78.10˄-24.6,022.10˄23/0,74 = 7,15cm˄3 Khối lượng riêng của Fe: d = 56/7,15 = 7,83g/cm˄3
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy Từ khóa » Khối Lượng Mol Của Au
-
Au (Vàng) Khối Lượng Mol - ChemicalAid
-
Nguyên Tử Au Có Bán Kính Và Khối Lượng Mol Nguyên Tử Lần Lượt Là
-
Nguyên Tử Au Có Bán Kính Và Khối Lượng Mol Là 1,44 A* Và 197 G ...
-
Nguyên Tử Au Có Bán Kính Và Khối Lượng Mol Nguyên ...
-
Khối Lương Nguyên Tử Của Vàng Là Bao Nhiêu? - Hoc247
-
Nguyên Tử Au Có Bán Kính Và Khối Lượng Mol Nguyên Tử Lần Lượt Là
-
[LỜI GIẢI] Nguyên Tử Au Có Bán Kính Và Khối Lượng Mol ... - Tự Học 365
-
Nguyên Tử Au Có Bán Kính Và Khối Lượng Mol Nguyên Tử ...
-
Nguyên Tử Au Có Bán Kính Và Khối Lượng Mol Nguyên Tử Lần Lượt Là...
-
Ở 20oC Khối Lượng Riêng Của Au Là 19,32 G/cm3. Trong Tinh Thể Au...
-
Môn Hóa Học Lớp 10 Nguyên Tử Au Có Bán Kính Và Khối Lượng Mol ...
-
Nguyên Tử Au Có Bán Kính Và Khối Lượng Mol ...
-
Ở 20$^{circ}$C Khối Lượng Riêng Của Au Là 19,32 G/cm$^{3}$. - LGH