Pha 300ml Dung Dịch NaOH 1M Với 200ml Dung Dịch NaOH 1,5 M ...
Có thể bạn quan tâm
HOC24
Lớp học Học bài Hỏi bài Giải bài tập Đề thi ĐGNL Tin tức Cuộc thi vui Khen thưởng- Tìm kiếm câu trả lời Tìm kiếm câu trả lời cho câu hỏi của bạn
Lớp học
- Lớp 12
- Lớp 11
- Lớp 10
- Lớp 9
- Lớp 8
- Lớp 7
- Lớp 6
- Lớp 5
- Lớp 4
- Lớp 3
- Lớp 2
- Lớp 1
Môn học
- Toán
- Vật lý
- Hóa học
- Sinh học
- Ngữ văn
- Tiếng anh
- Lịch sử
- Địa lý
- Tin học
- Công nghệ
- Giáo dục công dân
- Tiếng anh thí điểm
- Đạo đức
- Tự nhiên và xã hội
- Khoa học
- Lịch sử và Địa lý
- Tiếng việt
- Khoa học tự nhiên
- Hoạt động trải nghiệm
- Hoạt động trải nghiệm, hướng nghiệp
- Giáo dục kinh tế và pháp luật
Chủ đề / Chương
Bài học
HOC24
 Khách vãng lai Đăng nhập Đăng ký Khám phá Hỏi đáp Đề thi Tin tức Cuộc thi vui Khen thưởng
Khách vãng lai Đăng nhập Đăng ký Khám phá Hỏi đáp Đề thi Tin tức Cuộc thi vui Khen thưởng - Tất cả
- Toán
- Vật lý
- Hóa học
- Sinh học
- Ngữ văn
- Tiếng anh
- Lịch sử
- Địa lý
- Tin học
- Công nghệ
- Giáo dục công dân
- Tiếng anh thí điểm
- Hoạt động trải nghiệm, hướng nghiệp
- Giáo dục kinh tế và pháp luật
Câu hỏi
Hủy Xác nhận phù hợp Chọn lớp Tất cả Lớp 12 Lớp 11 Lớp 10 Lớp 9 Lớp 8 Lớp 7 Lớp 6 Lớp 5 Lớp 4 Lớp 3 Lớp 2 Lớp 1 Môn học Toán Vật lý Hóa học Sinh học Ngữ văn Tiếng anh Lịch sử Địa lý Tin học Công nghệ Giáo dục công dân Tiếng anh thí điểm Đạo đức Tự nhiên và xã hội Khoa học Lịch sử và Địa lý Tiếng việt Khoa học tự nhiên Hoạt động trải nghiệm Hoạt động trải nghiệm, hướng nghiệp Giáo dục kinh tế và pháp luật Mới nhất Mới nhất Chưa trả lời Câu hỏi hay anhlephuong 29 tháng 7 2020 lúc 21:25
anhlephuong 29 tháng 7 2020 lúc 21:25 Pha 300ml dung dịch NaOH 1M với 200ml dung dịch NaOH 1,5 M. Tính C%, CM biết khối lượng riêng là D =1,05g/ml
Lớp 8 Hóa học CHƯƠNG VI: DUNG DỊCH Những câu hỏi liên quan
- Nguyễn Bình Chi
Bài 3.
1. Trộn 300ml dung dịch NaOH 1M với 200ml dung dịch NaOH 1,5M. Hãy tính CM và C% của dung dịch thu được sau khi trộn, biết Ddd sau trộn = 1,05g/ml.
2. Cho dung dịch H2SO4 39,2%. Với những dụng cụ đã cho trong phòng thí nghiệm em hãy trình bày cách pha chế 200g dung dịch H2SO4 9,8%?
Xem chi tiết Lớp 8 Hóa học 0 0 Gửi Hủy
Gửi Hủy 
- Nguyễn Bình Chi
Bài 3.
1. Trộn 300ml dung dịch NaOH 1M với 200ml dung dịch NaOH 1,5M. Hãy tính CM và C% của dung dịch thu được sau khi trộn, biết Ddd sau trộn = 1,05g/ml.
2. Cho dung dịch H2SO4 39,2%. Với những dụng cụ đã cho trong phòng thí nghiệm em hãy trình bày cách pha chế 200g dung dịch H2SO4 9,8%?
Xem chi tiết Lớp 8 Hóa học 1 0 Gửi Hủy
Gửi Hủy  Kudo Shinichi
Kudo Shinichi  14 tháng 4 2022 lúc 6:24
14 tháng 4 2022 lúc 6:24 1, \(n_{NaOH}=0,3.1+1,5.0,2=0,6\left(mol\right)\)
\(V_{NaOH}=0,2+0,3=0,5\left(l\right)\)
\(\rightarrow\left\{{}\begin{matrix}C_{MNaOH}=\dfrac{0,6}{0,5}=1,2M\\C\%=1,2.\dfrac{40}{10.1,05}=4,57\%\end{matrix}\right.\)
2, \(m_{H_2SO_4}=200.9,8\%=19,6\left(g\right)\\ m_{ddH_2SO_4\left(39,2\%\right)}=\dfrac{19,6}{39,2\%}=50\left(g\right)\\ \rightarrow m_{H_2O\left(thêm\right)}=200-50=150\left(g\right)\)
Cách pha: ta cân lấy 50 g ddH2SO4 39,2% và 150 g H2O, rót nước vào bình ống nghiệm rồi từ từ rót ddH2SO4 vào rồi khuấy đều
Đúng 1 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Nguyễn Hoàng Nam
Cần dùng bao nhiêu ml dung dịch NaOH 3% có khối lượng riêng là 1,05g/ml và bao nhiêu mililit dung dịch NaOH 10% có khối lượng riêng là 1,12g/ml để pha chế được 2 lit dung dịch NaOH 8% có khối lượng riêng là 1,10g/ml.
Xem chi tiết Lớp 8 Hóa học 1 0 Gửi Hủy
Gửi Hủy  Ngô Quang Sinh
Ngô Quang Sinh  19 tháng 5 2018 lúc 15:37
19 tháng 5 2018 lúc 15:37 * Phần tính toán:
Khối lượng dung dịch NaOH: m d d = D.V = 1,1.2000=2200(g)
Khối lượng NaOH có trong 2 lit dung dịch:
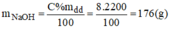
Gọi x(ml) là thể tích của dung dịch NaOH 3% ⇒ m d d = V.d = 1,05.x
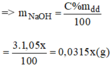
Gọi y(ml) là thể tích của dung dịch NaOH 10% ⇒ m d d = V.d = 1,12.y
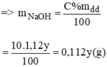
Ta có hệ phương trình sau: 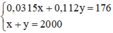
Giải hệ phương trình trên, ta được: 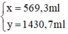
* Cách pha chế:
Đong lấy 569,3ml dung dịch NaOH 3% và 1430,7ml dung dịch NaOH 10% vào bình có dung dịch khoảng 3 lit. Trộn đều ta được 2 lit dung dịch NaOH 8% có khối lượng riêng 1,1g/ml.
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy 
- khuôn mặt lạnh lùng
trộn 300ml dung dich NaOH 1M với 200ml dung dịch NaOH 1,5M hãy tính nồng độ mol và nồng độ phần trăm của dung dịch thu được biết d=1,05g/ml
m.n làm chi tiết giùm e với và nhớ cho cả công thức tính nha
Xem chi tiết Lớp 8 Hóa học CHƯƠNG I: CHẤT - NGUYÊN TỬ - PHÂN TỬ 1 0 Gửi Hủy
Gửi Hủy  Nguyệt Trâm Anh 17 tháng 4 2018 lúc 20:02
Nguyệt Trâm Anh 17 tháng 4 2018 lúc 20:02 nNaOH (dd1M)=0,3mol; nNaOH (dd1,5M)=0,2.1,5=0,3mol;
nNaOH (dd sau)=nNaOH (dd1M) + nNaOH (dd1,5M)=0,3+0,3=0,6mol
Vdd sau= 300+200=500ml=0,5 lít
CM(ddsau)=0,6/0,5=1,2M
m dd sau=d.V(ddsau)=500.1,05=525g;
mNaOH=0,6 .40=24g
C% ddsau=24/525 .100% ~=4,57%
Đây bạn tham khảo nhé
Nhớ tick nha ![]()
 Gửi Hủy
Gửi Hủy 
- mimias
Trung hòa hết 200ml dung dịch H2SO4 1M bằng dung dịch NaOH 20%
a) Tính khối lượng muối thu được và dung dịch NaOH cần dùng
b) Nếu trung hòa dung dịch H2SO4 trên bằng dung dịch KOH 5,6%, có khối lượng riêng là 1,045g/ml , thì cần bao nhiêu ml dung dịch KOH
Xem chi tiết Lớp 9 Hóa học 2 0 Gửi Hủy
Gửi Hủy  Nguyễn Hoàng Minh
Nguyễn Hoàng Minh  17 tháng 12 2021 lúc 21:32
17 tháng 12 2021 lúc 21:32 \(n_{H_2SO_4}=1.0,2=0,2(mol)\\ PTHH:2NaOH+H_2SO_4\to Na_2SO_4+2H_2O\\ a,n_{NaOH}=0,4(mol);n_{Na_2SO_4}=0,2(mol)\\ \Rightarrow \begin{cases} m_{Na_2SO_4}=0,2.142=28,4(g)\\ m_{dd_{NaOH}}=\dfrac{0,4.40}{20\%}=80(g) \end{cases}\\ b,2KOH+H_2SO_4\to K_2SO_4+2H_2O\\ \Rightarrow n_{KOH}=0,4(mol)\\ \Rightarrow m_{dd_{KOH}}=\dfrac{0,4.56}{5,6\%}=400(g)\\ \Rightarrow V_{dd_{KOH}}=\dfrac{400}{1,045}=382,78(ml)\)
Đúng 1 Bình luận (0) Gửi Hủy
Gửi Hủy  Rhider
Rhider  17 tháng 12 2021 lúc 20:54
17 tháng 12 2021 lúc 20:54 Bước 1: nH2SO4 = VH2SO4 . CM H2SO4= 0,2 . 1 = 0,2mol
Bước 2:
PTHH: 2NaOH + H2SO4 → Na2SO4 + H2O
2 mol 1 mol
? mol 0,2mol
Đúng 1 Bình luận (0)  Gửi Hủy
Gửi Hủy 
- Nhã Linh
trung hòa 1000 ml dung dịch H2SO4 0,75 M bằng dung dịch KOH 25%. Tính:
a/ tính khối lượng dung dịch KOH
b/ Nếu trung hòa lượng axit trên bằng dung dịch NaOH 15% có khối lượng riêng = 1,05g/ml. Tính thể tích dung dịch NaOH cần dùng
Xem chi tiết Lớp 9 Hóa học Bài 13. Luyện tập chương I: Các loại hợp chất vô c... 1 0 Gửi Hủy
Gửi Hủy  Chan Nước Mắm Cơm 26 tháng 9 2016 lúc 20:41
Chan Nước Mắm Cơm 26 tháng 9 2016 lúc 20:41 nH2SO4=0.75(mol)
H2SO4+2KOH->K2SO4+2H2O
nKOH=2 nH2SO4->nKOH=1.5(mol)
mKOH=84(g)
mdd=84*100:25=336(g)
H2SO4+2NaOH->Na2SO4+2H2O
nNaOH=1.5(mol) ->mNaOH=60(g)
mdd NaOH=60*100:15=400(g)
V NaOH=400:1.05=381(ml)
Bạn xem lại xem 100 ml hay 1000 ml nhé ^^ tại mình thấy số mol hơi lớn
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Boun Prem
Câu 1 : Trung hoà 200ml dung dịch H2SO4 1M bằng dung dịch NaOH 20% .
a, Tính khối lượng dung dịch NaOH đã dùng?
b, Dùng dung dịch KOH 5,6% để trung hòa dung dịch axit trên.Tính thể tích dung dịch KOH phải dùng biết dung dịch có d= 1,045g/ml.
Câu 2: Trộn 1lít dung dịch NaOH 2M với lít dung dịch NaOH 1M thu được dung dịch mới có nồng độ bao nhiêu?
Câu 3: Trộn 1,5 lít dung dịch HCl 2M với a dung dịch HCl 1 M thu được dung dịch có nồng độ 1,5 M. Tìm ạ?
Xem chi tiết Lớp 8 Hóa học Bài 43. Pha chế dung dịch 0 0 Gửi Hủy
Gửi Hủy 
- phan gia bao
1) tính nồng độ NaOH sau khi trộn 200ml dung dịch NaOH 3M với 300ml dung dịch NaOH 1M biết sự pha trộn này không làm thay đổi thể tích dung dịch
Xem chi tiết Lớp 8 Hóa học Bài 42: Nồng độ dung dịch 1 0 Gửi Hủy
Gửi Hủy  Gia Hân Ngô
Gia Hân Ngô  15 tháng 6 2018 lúc 8:18
15 tháng 6 2018 lúc 8:18 ndd1 = 3 . 0,2 = 0,6 mol
ndd2 = 1 . 0,3 = 0,3 mol
CM dd thu được = \(\dfrac{0,6+0,3}{0,2+0,3}=1,8M\)
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Eminnie
Tính số mol các chất trong các trường hợp sau:
+ 4,48 lít khí oxi ở đktc
+ 150 g dung dịch NaOH 16%
+ 200 ml dung dịch HCl 0,2M
+ 150 ml dung dịch NaOH 16% , biết khối lượng riêng của dd NaOH là 1,25 g/ml
+ Trộn 100 ml dung dịch NaCl 1M với 200 ml dung dịch NaCl 0,5M
Xem chi tiết Lớp 9 Hóa học 1 0 Gửi Hủy
Gửi Hủy  Buddy
Buddy  10 tháng 9 2021 lúc 18:38
10 tháng 9 2021 lúc 18:38 
 Gửi Hủy
Gửi Hủy Khoá học trên OLM (olm.vn)
- Toán lớp 8 (Kết nối tri thức với cuộc sống)
- Toán lớp 8 (Cánh Diều)
- Toán lớp 8 (Chân trời sáng tạo)
- Ngữ văn lớp 8 (Kết nối tri thức với cuộc sống)
- Ngữ văn lớp 8 (Cánh Diều)
- Ngữ văn lớp 8 (Chân trời sáng tạo)
- Tiếng Anh lớp 8 (i-Learn Smart World)
- Tiếng Anh lớp 8 (Global Success)
- Khoa học tự nhiên lớp 8 (Kết nối tri thức với cuộc sống)
- Khoa học tự nhiên lớp 8 (Cánh diều)
- Khoa học tự nhiên lớp 8 (Chân trời sáng tạo)
- Lịch sử và địa lý lớp 8 (Kết nối tri thức với cuộc sống)
- Lịch sử và địa lý lớp 8 (Cánh diều)
- Lịch sử và địa lý lớp 8 (Chân trời sáng tạo)
- Giáo dục công dân lớp 8 (Kết nối tri thức với cuộc sống)
- Giáo dục công dân lớp 8 (Cánh diều)
- Giáo dục công dân lớp 8 (Chân trời sáng tạo)
- Công nghệ lớp 8 (Kết nối tri thức với cuộc sống)
Từ khóa » Khối Lượng Riêng Của Naoh 1m
-
Khối Lượng Riêng Naoh - VIETNAMNET.INFO
-
Tìm Khối Lượng Chất Tan Có Trong 250ml Dung Dịch NAOH 1M - Hoc24
-
Tính Khối Lượng NaOH Cần Thiết để Pha Chế được 50ml Dung Dịch ...
-
Khối Lượng Riêng Của NaOH Là Gì?
-
Để Trung Hòa 40 Ml Giấm ăn Cần 25 Ml Dung Dịch ... - Cungthi.online
-
Để Trung Hòa 40 Ml Giấm ăn Cần 25 Ml Dung Dịch NaOH ... - Khóa Học
-
Để Trung Hòa Hết 200ml Dung Dịch NaOH 1M Thi Cần Dùng Hết Bao ...
-
Trộn 300ml Dung Dịch NaOH 1M Với 200ml Dung Dịch NaOH 1,5M ...
-
Cách Tính Số Mol: Công Thức Tính Và Bài Tập Minh Họa - LabVIETCHEM
-
Cách Tính Nồng độ Mol - Thủ Thuật Phần Mềm
-
Tính Khối Lượng NaOH Có Trong 200 Gam Dung Dịch NaOH 15%
-
Thể Tích Dung Dịch NaOH 1M Cần để Trung Hòa Hoàn Toàn 200 Ml ...
-
Công Thức Tính Nồng độ đương Lượng