Phenol – Wikipedia Tiếng Việt
Có thể bạn quan tâm
Nội dung
chuyển sang thanh bên ẩn- Đầu
- Bài viết
- Thảo luận
- Đọc
- Sửa đổi
- Sửa mã nguồn
- Xem lịch sử
- Đọc
- Sửa đổi
- Sửa mã nguồn
- Xem lịch sử
- Các liên kết đến đây
- Thay đổi liên quan
- Liên kết thường trực
- Thông tin trang
- Trích dẫn trang này
- Tạo URL rút gọn
- Tạo một quyển sách
- Tải dưới dạng PDF
- Bản để in ra
- Wikimedia Commons
- Wikiquote
- Khoản mục Wikidata
| Phenol | |||
|---|---|---|---|
| |||
| |||
| Danh pháp IUPAC | Phenol | ||
| Tên khác | Carbolic Acid, Benzenol, Phenylic Acid, Hydroxybenzene, Phenic acid | ||
| Nhận dạng | |||
| Số CAS | 108-95-2 | ||
| PubChem | 996 | ||
| KEGG | D06536 | ||
| ChEMBL | 14060 | ||
| Số RTECS | SJ3325000 | ||
| Ảnh Jmol-3D | ảnh | ||
| SMILES | đầy đủ
| ||
| InChI | đầy đủ
| ||
| UNII | 339NCG44TV | ||
| Thuộc tính | |||
| Bề ngoài | White Crystalline Solid | ||
| Khối lượng riêng | 1.07 g/cm³ | ||
| Điểm nóng chảy | 40,5 °C (313,6 K; 104,9 °F) | ||
| Điểm sôi | 181,7 °C (454,8 K; 359,1 °F) | ||
| Độ hòa tan trong nước | 8.3 g/100 ml (20 °C) | ||
| Độ axit (pKa) | 9.95 (trong nước), 29.1 (in acetonitrile)[1] | ||
| Mômen lưỡng cực | 1.7 D | ||
| Các nguy hiểm | |||
| Phân loại của EU | Toxic (T)Muta. Cat. 3Corrosive (C) | ||
| NFPA 704 |
| ||
| Chỉ dẫn R | R23/R24/R25-R34-R48/R20/R21/R22-R68 | ||
| Chỉ dẫn S | (S1/2)-S24/S25-S26-S28-S36/S37/S39-S45 | ||
| Điểm bắt lửa | 79 °C | ||
| Các hợp chất liên quan | |||
| Hợp chất liên quan | Benzenethiol | ||
| Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |||
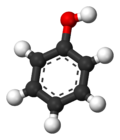
Phenol hay acid carbolic là một hợp chất hữu cơ thơm có công thức phân tử C6H5OH. Đây là một chất rắn tinh thể màu trắng dễ bay hơi. Phân tử bao gồm một nhóm phenyl (−C6H5) liên kết với một nhóm hydroxyl (-OH). Phenol hơi có tính acid. Phenol có thể gây bỏng nặng khi rơi vào da. Phenol lần đầu tiên được chiết xuất từ nhựa than đá, nhưng ngày nay được sản xuất trên quy mô lớn (khoảng 7 tỷ kg/năm) từ các nguyên liệu có nguồn gốc từ dầu mỏ. Đây là một mặt hàng công nghiệp quan trọng như là tiền thân của nhiều vật liệu và hợp chất hữu ích. Đây chủ yếu được sử dụng để tổng hợp nhựa và các vật liệu liên quan. Phenol và các dẫn xuất hóa học của nó rất cần thiết để sản xuất polycarbonat, epoxies, Bakelite, nylon, chất tẩy rửa, thuốc diệt cỏ như thuốc diệt cỏ phenoxy và nhiều loại dược phẩm.

Tính chất
[sửa | sửa mã nguồn]Phenol là một hợp chất hữu cơ hòa tan đáng kể trong nước, với khoảng 84,2 g hòa tan trong 1000 mL (khoảng 0,895 M) ở 25oC. Hỗn hợp đồng nhất của phenol và nước ở phenol nặng hơn tỷ trọng nước ~ 2,6 và có thể là cao hơn. Muối natri của phenol, natri phenoxide, hòa tan trong nước nhiều hơn. Phenol tan vô hạn ở nhiệt độ trên khoảng 66oC.
Tính axít
[sửa | sửa mã nguồn]Phenol có tính acid. Trong dung dịch nước có cân bằng:
Vì vậy, khác với rượu, phenol còn có thể tác dụng với base mạnh tạo muối phenolate:
Tuy nhiên, tính acid của phenol rất yếu Ka=10−10, yếu hơn acid cacbonic nên không làm đổi màu quỳ tím. Vì vậy, muối phenolat bị acid cacbonic tác dụng tạo lại phenol:
Phản ứng này được dùng để tái tạo phenol trong công nghiệp.
Tính chất như rượu
[sửa | sửa mã nguồn]Phenol có thể tác dụng được với Na như rượu nhưng khác với rượu, muối phenolat không bị nước phân hủy:
C6H5ONa + H2O ---> (Không phản ứng).
Phenol cũng tạo được ester như rượu nhưng khác với rượu có thể tác dụng trực tiếp với acid, phenol chỉ có thể tác dụng với Acetyl chloride hoặc anhydride acetic mới tạo được ester:
Điều này được giải thích do 2 nguyên nhân:
- Mật độ điện tích âm của O nhóm -OH vì có hệ liên hợp trong phân tử nên giảm hơn so với O nhóm -OH của rượu thông thường, dẫn đến phenol khó tấn công vào phân tử acid tạo ester hơn.
- Phenol có vòng thơm nên gây hiệu ứng không gian cản trở.
Tính chất của nhân thơm (Phản ứng thế H ở vòng benzen)
[sửa | sửa mã nguồn]Phenol phản ứng với dung dịch brom tạo kết tủa trắng, nếu Br2 dư cũng tạo kết tủa tan
Phenol phản ứng với HNO3 tạo kết tủa tan
Phenol tham gia phản ứng thế brom dễ hơn benzen do có nhóm OH đẩy e làm tăng mật độ electron trong vòng benzen
Phản ứng riêng
[sửa | sửa mã nguồn]
Ứng dụng
[sửa | sửa mã nguồn]Phenol được dùng trong nhiều lĩnh vực khác nhau:
- Công nghiệp chất dẻo: phenol là nguyên liệu để điều chế nhựa phenol formaldehyde.
- Công nghiệp tơ hóa học: Từ phenol tổng hợp ra tơ polyamide.
- Nông dược: Từ phenol điều chế được chất diệt cỏ dại và kích thích tố thực vật 2,4 - D (là muối natri của acid 2,4 dichlorphenoxyacetic).
- Phenol cũng là nguyên liệu để điều chế một số phẩm nhuộm, thuốc nổ (acid picric).
- Do có tính diệt khuẩn nên phenol được dùng để trực tiếp làm chất sát trùng, tẩy uế, hoặc để điều chế các chất diệt nấm mốc (ortho - và para - nitrophenol…)
Lịch sử
[sửa | sửa mã nguồn]Phenol được phát hiện vào năm 1834, khi nó được chiết xuất từ nhựa than đá, đó là nguồn chính sản xuất phenol cho đến khi ngành công nghiệp hóa dầu phát triển.
Các chất sát trùng mang đặc tính của phenol được sử dụng bởi Sir Joseph Lister (1827-1912) trong kỹ thuật phẫu thuật tiên phong của ông dùng chất khử trùng, mặc việc tiếp xúc liên tục với phenol gây kích ứng da. Lister đã phủ những vết thương với một miếng giẻ hoặc vải thô được ngâm trong acid carbolic (một tên khác của phenol).
Acid carbolic (phenol) cũng là thành phần hoạt chất trong một số thuốc giảm đau thường uống như Chloraseptic, đường xông hơi (phun) như Carmex. Đây cũng là thành phần chính của quả cầu khói Carbolic Ball, một thiết bị trên thị trường tại Luân Đôn vào thế kỷ XIX sử dụng để chống dịch bệnh cúm và các bệnh khác.
Vì rẻ tiền, dễ điều chế, gây ra cái chết nhanh chóng và êm dịu chỉ với 1 gram, phenol được sử dụng như một phương tiện giết người của Đức quốc xã trong thế chiến thứ hai từ năm 1939 đến những ngày cuối cùng của cuộc chiến. Thời kỳ đó, Zyklon-B, một phát minh của Gerhard Lenz, được sử dụng trong các phòng hơi ngạt để giết người với số lượng lớn, phát xít Đức còn dùng phenol tiêm cho từng nạn nhân để sát hại nhóm ít người như một biện pháp tiết kiệm kinh tế. Việc tiêm phenol được áp dụng với hàng ngàn người dân trong các trại tập trung, đặc biệt là ở Auschwitz-Birkenau.
Điều chế
[sửa | sửa mã nguồn]Nguồn phenol chủ yếu lấy từ sản phẩm chưng cất than đá
Ngoài ra có thể điều chế từ benzen.
Điều chế từ isopropylbenzen:
Sự kiện cá nục ở Quảng Trị nhiễm phenol năm 2016
[sửa | sửa mã nguồn]Tháng 6/2016 phenol được phát hiện có trong 30 tấn cá nục ở Quảng Trị, và Chi Cục VSATTP Quảng Trị công bố kết quả xét nghiệm xác định hàm lượng là 0,037 mg/kg.
Tuy nhiên Phó Cục trưởng Cục An toàn thực phẩm Bộ Y tế đã có những giải đáp xung quanh vấn đề này, khẳng định rằng ăn cá nục nhiễm phenol ở Quảng Trị không ảnh hưởng tới sức khỏe, và nói rằng phenol có ở khắp nơi quanh ta, cả trong thực phẩm khác.[2]
Tham khảo
[sửa | sửa mã nguồn]- ^ Kütt, A.; Movchun, V.; Rodima, T.; Dansauer, T.; Rusanov, E. B.; Leito, I.; Kaljurand, I.; Koppel, J.; Pihl, V.; Koppel, I.; Ovsjannikov, G.; Toom, L.; Mishima, M.; Medebielle, M.; Lork, E.; Röschenthaler, G.-V.; Koppel, I. A.; Kolomeitsev, A. A. Pentakis(trifluoromethyl)phenyl, a Sterically Crowded and Electron-withdrawing Group: Synthesis and Acidity of Pentakis(trifluoromethyl)benzene, -toluene, -phenol, and -aniline. J. Org. Chem. 2008, 73, 2607-2620. DOI: 10.1021/jo702513w
- ^ Bộ Y tế khẳng định ăn cá nục nhiễm Phenol ở Quảng Trị không ảnh hưởng tới sức khỏe. Công lý Online, 13/6/2016. Truy cập 14/07/2019.
| Cơ sở dữ liệu tiêu đề chuẩn | |
|---|---|
| Quốc tế |
|
| Quốc gia |
|
| Khác |
|
| |
|---|---|
| Dẫn xuất Acriđine | Etacriđin lactat · 9-Aminoacriđin · Euflavin |
| Các biguanit và amiđin | Đibrompropamiđin · Clohexiđin# · Propamiđin · Hexamiđin · Polihexanit |
| Phenol và các dẫn xuất | Hexaclophen · Policresulen · Phenol · Triclosan · Cloxilenol# · Biphenylol · Fenticlor |
| Các dẫn xuất Nitrofuran | Nitrofurazon |
| Các sản phẩm từ Iod | Iot/octylphenoxipoliglicolete · Povidone-iodine# · Điiothidroxipropan |
| Các dẫn xuất Quinolin | Dequalinium · Cloquinaldol · Oxiquinolin · Clioquinol |
| Hợp chất ammoni bậc bốn | Benzalkonium · Benzethonium clorua · Xetrimonium (bromua/clorua) · Xetylpiriđinium · Xetrimit · Benzoxonium clorua · Điđecylđimetylamonium clorua |
| Các sản phẩm từ Thủy ngân | Thủy ngân amiđoclorua · Phenylmercuric borat · Thủy ngân clorua · Mercurocrom · Thiomersal · Thủy ngân iođua |
| Các hợp chất của Bạc | Bạc nitrat |
| Ancol | Propanol (Propyl Alcohol) · Isopropanol (Isopropyl Ancol) · Ethanol (Ethyl Alcohol)# |
| Khác | Kali pemanganat · Natri hypoclorit · Hydro peoxit · Eosin · Tosylcloramit natri |
| #WHO-EM. ‡Thu hồi trên thị trường. Thử nghiệm lâm sàng: †Pha III. §Chưa bao giờ đến pha III | |
| |
|---|---|
| Antihemorrhoidals để sử dụng tại chỗ | corticosteroids (Hydrocortisone, Prednisolone, Betamethasone, Fluorometholone, Fluocortolone, Dexamethasone, Fluocinolone acetonide, Fluocinonide) local anesthetics (Lidocaine, Tetracaine, Benzocaine, Dibucaine, Procaine, Oxetacaine, Pramocaine) other (Tribenoside) |
| Antivaricose điều trị | heparins hoặc heparinoids để sử dụng tại chỗ (Organo-heparinoid, Sodium apolate, Heparin, Pentosan polysulfate) Các chất sclerosing cho tiêm chủng địa phương (sclerosing agents for local injection) (Monoethanolamine oleate, Polidocanol, Invert sugar, Sodium tetradecyl sulfate, Phenol) other (Calcium dobesilate) |
| Các tác nhân mao dẫn ổn định | bioflavonoids (Rutoside, Monoxerutin, Diosmin, Troxerutin, Hidrosmin) - other (Tribenoside, Etamsylate) |
| Bản mẫu:Vascular navs | |
| |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Dạng hít |
| ||||||||||
| Dạng tiêm |
| ||||||||||
| #WHO-EM. ‡Thu hồi trên thị trường. Thử nghiệm lâm sàng: †Pha III. §Chưa bao giờ đến pha III | |||||||||||
| |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Tổng quan |
| ||||||||||
| Phản ứng hữu cơ |
| ||||||||||
| Phương pháp phổ trong Hoá hữu cơ |
| ||||||||||
| Hydrocarbon |
| ||||||||||
| Dẫn xuất của Hidrocacbon |
| ||||||||||
| Hợp chất cơ - nguyên tố |
| ||||||||||
| Hợp chất dị vòng |
| ||||||||||
| Hợp chất cao phân tử |
| ||||||||||
- Lớp phenol
- Chất tẩy trùng
- Độc tố thần kinh
- Hóa chất hàng hóa
- Taxonbars without from parameter
- Trang thẻ đơn vị phân loại không có ID đơn vị phân loại tại Wikidata
- Thẻ đơn vị phân loại trên trang có thể không là đơn vị phân loại
Từ khóa » Ví Dụ Về Hợp Chất Phenol
-
Phenol Là Gì - Tất Tần Tật Các Thông Tin Về Phenol Hóa 11
-
Phenol Là Gì? Tính Chất, điều Chế, Công Dụng Và Lưu ý Khi Sử Dụng
-
Tính Chất Hóa Học ứng Dụng Và Cách điều Chế Phenol - VietChem
-
Thế Nào Là Phenol? Lấy 3 Ví Dụ Về Phenol Và Gọi Tên Công Thức đó?
-
Phenol Là Gì? Tính Chất Hóa Học Và Ứng Dụng Của Phenol
-
Tính Chất Vật Lý, Tính Chất Hóa Học Của Phenol, Điều Chế Và Ứng Dụng
-
KHÁI NIỆM, PHÂN LOẠI, TÍNH CHẤT HÓA HỌC, ĐIỀU CHẾ VÀ ...
-
Phenol
-
[CHUẨN NHẤT] Tính Chất Hóa Học Của Phenol - TopLoigiai
-
Phenol Là Gì, Công Thức Cấu Tạo Của Phenol ? - Đáp Án Chuẩn
-
Tất Tần Tật Về Phenol
-
Phenol (C₆H₅OH): Dung Môi Hoá Học - Nhà Thuốc Long Châu
-
Phenol Là Gì? Tính Chất, Cách điều Chế Và ứng Dụng Của Phenol?
-
Tính Chất Hóa Học Và Công Thức Cấu Tạo Của Phenol C6h5OH




![{\displaystyle {\mathrm {C} {\vphantom {A}}_{\smash[{t}]{6}}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{5}}\mathrm {OH} {}+{}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {O} {}\mathrel {\longrightleftharpoons } {}\mathrm {C} {\vphantom {A}}_{\smash[{t}]{6}}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{5}}\mathrm {O} {\vphantom {A}}^{-}{}+{}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{3}}\mathrm {O} {\vphantom {A}}^{+}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b62103afe77eb93befcdccd4a9d76d474833b879)
![{\displaystyle {\mathrm {C} {\vphantom {A}}_{\smash[{t}]{6}}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{5}}\mathrm {OH} {}+{}\mathrm {NaOH} {}\mathrel {\longrightarrow } {}\mathrm {C} {\vphantom {A}}_{\smash[{t}]{6}}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{5}}\mathrm {ONa} {}+{}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {O} }}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c484a4022e5c824aa79e97ee02dd492d647f5252)
![{\displaystyle {\mathrm {C} {\vphantom {A}}_{\smash[{t}]{6}}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{5}}\mathrm {ONa} {}+{}\mathrm {CO} {\vphantom {A}}_{\smash[{t}]{2}}{}+{}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {O} {}\mathrel {\longrightarrow } {}\mathrm {C} {\vphantom {A}}_{\smash[{t}]{6}}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{5}}\mathrm {OH} {}+{}\mathrm {NaHCO} {\vphantom {A}}_{\smash[{t}]{3}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0470e7804b0f4fd834bb360cf586830cfb4930b0)
![{\displaystyle {\mathrm {C} {\vphantom {A}}_{\smash[{t}]{6}}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{5}}\mathrm {OH} {}+{}\mathrm {CH} {\vphantom {A}}_{\smash[{t}]{3}}\mathrm {COCl} {}\mathrel {\longrightarrow } {}\mathrm {CH} {\vphantom {A}}_{\smash[{t}]{3}}\mathrm {COOC} {\vphantom {A}}_{\smash[{t}]{6}}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{5}}{}+{}\mathrm {HCl} }}](https://wikimedia.org/api/rest_v1/media/math/render/svg/fb0dd859fe61c79e6a4a5d1e9694753cab3dff7c)
![{\displaystyle {\mathrm {C} {\vphantom {A}}_{\smash[{t}]{6}}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{5}}\mathrm {OH} {}+{}(\mathrm {CH} {\vphantom {A}}_{\smash[{t}]{3}}\mathrm {CO} ){\vphantom {A}}_{\smash[{t}]{2}}\mathrm {O} {}\mathrel {\longrightarrow } {}\mathrm {CH} {\vphantom {A}}_{\smash[{t}]{3}}\mathrm {COOC} {\vphantom {A}}_{\smash[{t}]{6}}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{5}}{}+{}\mathrm {CH} {\vphantom {A}}_{\smash[{t}]{3}}\mathrm {COOH} }}](https://wikimedia.org/api/rest_v1/media/math/render/svg/231f44e0cd63978ef791c8fa4f66b4216b9fa859)
![{\displaystyle {\mathrm {C} {\vphantom {A}}_{\smash[{t}]{6}}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{5}}\mathrm {OH} {}+{}3\,\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}{}\mathrel {\xrightarrow[{\text{t°, p}}]{\mathrm {Ni} }} {}\mathrm {C} {\vphantom {A}}_{\smash[{t}]{6}}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{11}}\mathrm {OH} }}](https://wikimedia.org/api/rest_v1/media/math/render/svg/5fb90b79dc99859a9d99ac429b02871a53857f67)
![{\displaystyle {\mathrm {C} {\vphantom {A}}_{\smash[{t}]{6}}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{6}}{}+{}\mathrm {Br} {\vphantom {A}}_{\smash[{t}]{2}}{}\mathrel {\xrightarrow {\mathrm {t} {\vphantom {A}}^{o}} } {}\mathrm {C} {\vphantom {A}}_{\smash[{t}]{6}}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{5}}\mathrm {Br} {}+{}\mathrm {HBr} }}](https://wikimedia.org/api/rest_v1/media/math/render/svg/97db8ce96d83e142fa5f91f2505c361971c7561d)
![{\displaystyle {\mathrm {C} {\vphantom {A}}_{\smash[{t}]{6}}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{5}}\mathrm {Br} {}+{}2\,\mathrm {NaOH} {}\mathrel {\xrightarrow {\mathrm {t} {\vphantom {A}}^{o}{;}{\mkern {6mu}}\mathrm {p} } } {}\mathrm {C} {\vphantom {A}}_{\smash[{t}]{6}}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{5}}\mathrm {ONa} {}+{}\mathrm {NaBr} {}+{}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {O} }}](https://wikimedia.org/api/rest_v1/media/math/render/svg/67a82ed0893fc1d8063f111572f88e979f5fd70a)
![{\displaystyle {\mathrm {C} {\vphantom {A}}_{\smash[{t}]{6}}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{6}}{}+{}\mathrm {CH} {\vphantom {A}}_{\smash[{t}]{2}}{=}\mathrm {CH} {-}\mathrm {CH} {\vphantom {A}}_{\smash[{t}]{3}}{}+{}\mathrm {O} {\vphantom {A}}_{\smash[{t}]{2}}(\mathrm {kk} ){}\mathrel {\longrightarrow } {}\mathrm {C} {\vphantom {A}}_{\smash[{t}]{6}}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{5}}\mathrm {OH} {}+{}(\mathrm {CH} {\vphantom {A}}_{\smash[{t}]{3}}){\vphantom {A}}_{\smash[{t}]{2}}\mathrm {CO} }}](https://wikimedia.org/api/rest_v1/media/math/render/svg/671258ebc366bef277233863e5eec5b50b0bc456)