Quá Trình đẳng áp – Wikipedia Tiếng Việt
Có thể bạn quan tâm
| Nhiệt động lực học | |||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 Động cơ nhiệt Carnot cổ điển Động cơ nhiệt Carnot cổ điển | |||||||||||||||||||||
Các nhánh
| |||||||||||||||||||||
Nguyên lý
| |||||||||||||||||||||
Hệ thống nhiệt động
| |||||||||||||||||||||
Thuộc tính hệNote: Biến số liên hợp in italics
| |||||||||||||||||||||
Tính năng vật liệu
| |||||||||||||||||||||
Phương trình
| |||||||||||||||||||||
Thế nhiệt động
| |||||||||||||||||||||
| |||||||||||||||||||||
Nhà khoa học
| |||||||||||||||||||||
| Sách | |||||||||||||||||||||
|
Quá trình đẳng áp (tiếng Anh: isobaric process) là 1 quá trình nhiệt động lực học trong đó áp suất là 1 hằng số (không đổi theo thời gian). Theo nguyên lý 1 nhiệt động lực học:
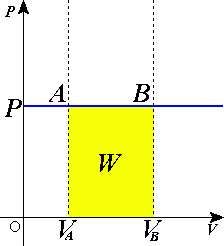
Theo định luật 1 về nhiệt động lực học, nếu thể tích của khí tăng lên thì công được sinh ra do sự dãn ra (tăng thể tích) của khí, cụ thể như sau:
Trong chất khi lý tưởng: trong đó n là số mol khí, R là hằng số khí lý tưởng
nên [1]
Vậy ta có được biểu thức
Liên hệ giữa nhiệt dung mol đẳng tích và đẳng áp
[sửa | sửa mã nguồn]Dựa vào quá trình đẳng tích, giữa quá trình không có sự truyền nhiệt của các phản ứng hóa học, ta thu được sự liên hệ giữa độ thay đổi nội năng phụ thuộc vào nhiệt độ như sau: với là nhiệt dung mol khi thể tích không đổi [2] Với là số bậc tự do của phân tử khí Khi áp suất không đổi, với là nhiệt dung mol khi áp suất không đổi.
Từ định luật 1 nhiệt động lực học ta có:
Tham khảo
[sửa | sửa mã nguồn]- ^ "Patana". Bản gốc lưu trữ ngày 4 tháng 7 năm 2011. Truy cập ngày 10 tháng 7 năm 2012. {{Chú thích web}}: Đã bỏ qua tham số không rõ |= (trợ giúp)
- ^ Principles of Physics, trang 621
Bài viết về chủ đề vật lý này vẫn còn sơ khai. Bạn có thể giúp Wikipedia mở rộng nội dung để bài được hoàn chỉnh hơn. |
- x
- t
- s
Từ khóa » Delta S Là Gì Delta T Là Gì
-
Delta T Là Gì
-
Bài 3. Chuyển động Thẳng Biến đổi đều - Tăng Giáp
-
Lý Thuyết động Lượng, Bảo Toàn động Lượng, Vật Lí Lớp 10
-
Delta T Trong Vật Lý Là Gì
-
Công Thức Vật Lý 10 Bài 3 | Dương Lê
-
Delta T Là Gì - Dòng Điện Không Đổi
-
Top 19 Delta S Trong Vật Lý Là Gì Mới Nhất 2022 - XmdForex
-
Delta T Là Gì
-
Gọi Delta T Là Khoảng Thời Gian - Làm Cha Cần Cả đôi Tay
-
Top 15 Delta S Là Gì Trong Vật Lý 10
-
Delta – Wikipedia Tiếng Việt
-
Delta T Trong Vật Lý Là Gì
-
Định Nghĩa Gia Tốc Là Gì? Cách Tính Gia Tốc?
-
Top 15 Delta T đơn Vị Là Gì
-
Delta T Là Gì - Cùng Hỏi Đáp
-
Kí Hiệu Δ Trong Vật Lí Là Gì - Hoc24
-
Dòng điện Không đổi. Nguồn điện - Vật Lý Lớp 11 - Baitap123






























