Tìm Hiểu Về Thuyết Michaelis-Menten
Có thể bạn quan tâm

HÓA HỌC VÀ SINH HỌC
-
QUẢNG CÁO
- KET SAT
Bài viết hay
-
 Lipoprotein – dạng lipid vận chuyển
Lipoprotein – dạng lipid vận chuyển -
 Quá trình thoái hóa glycogen
Quá trình thoái hóa glycogen -
 Sự tổng hợp glucose (con đường tân tạo glucose)
Sự tổng hợp glucose (con đường tân tạo glucose) -
 Sự Phosphoryl – Oxy hóa
Sự Phosphoryl – Oxy hóa -
 Con đường đường phân (glyeolysis)
Con đường đường phân (glyeolysis)
Tất cả bài viết
Tốc đô cực đai (Vmax) Với một nồng độ enzym thích hợp, nhiệt độ và pH thích hợp, khi nồng độ cơ chất tăng lên thì tốc độ phản ứng tăng lên. Khi các phân tử enzym đều bão hoà cơ chất thì tốc độ phản ứng đạt tốc độ tối đa (Vmax). Thuyết Michaelis-Menten Năm 1913, Michaelis và Menten đã đề ra giả thuyết về vai trò của nồng độ cơ chất trong việc hình thành phức hợp enzym – cơ chất ES. Sự liên quan nói chung giữa enzym, cơ chất và sản phẩm phản ứng được thể hiện bằng phương trình sau: kj k2 E + S->ES->E + P A-i Giả thuyết của Michaelis-Menten về sự liên quan giữa tốc độ phản ứng và nồng độ cơ chất được tính toán theo phương trình Michaelis-Menten: 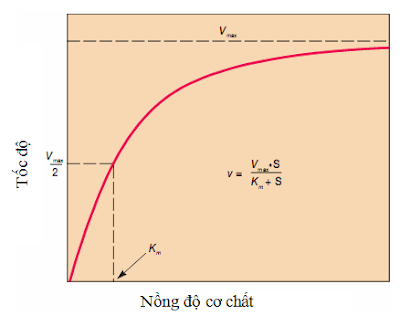 Ở đây v = tốc độ phản ứng vmax = tốc độ tối đa [S] = nồng độ cơ chất Km = hằng số Michaelis của enzym đối vối cơ chất. Khi nồng độ cơ chất thấp hơn KM rất nhiều, nghĩa là với số lượng enzym vượt quá số lượng cơ chất, trong phương trình Michaelis-Menten, ta có thể bỏ [S] ở mẫu số, phương trình trở thành dạng v=Vmax [S]/ KM, đây là phương trình tuyến tính dạng y = ax, nghĩa là tốc độ phản ứng chỉ phụ thuộc vào nồng độ cơ chất [S]. Lúc này phản ứng là phản ứng động học bậc 1 bởi vì tốc độ phản ứng tỷ lệ thuận với nồng độ cơ chất. Khi nồng độ cơ chất tăng lên đến mức đạt giá trị bằng giá trị KM thì phương trình Michaelis-Menten trở thành dạng V = Vmax/2, có nghĩa là tốc độ phản ứng bằng 1/2 tốc độ tối đa. Khi nồng độ cơ chất lớn hơn KM rất nhiều thì ta có thể bở KM ở mẫu số của phương trình Michaelis-Menten, và phương trình trở thành dạng V = Vmax, có nghĩa là tốc độ phản ứng đạt tốc độ tối đa (Vmax). Lúc này tất cả các phân tử enzym đều bão hoà cơ chất, phản ứng đạt động học “bậc không”, bởi vì, dù có tiếp tục tăng nồng độ cơ chất thì tốc độ phản ứng cũng không thay đổi và lúc này tốc độ phản ứng chỉ phụ thuộc vào nồng độ enzym. Ý nghĩa của các giá trị KM : - KM là hằng số tổng hợp của các hằng số tốc độ, có giá trị bằng nồng độ cơ chất cần thiết để tốc độ phản ứng đạt bằng 1/2 tốc độ tối đa. Như vậy, KM được tính bằng mol/L. Đọc thêm tại: http://hoahocvasinhhoc.blogspot.com/2015/06/tim-hieu-ve-ong-hoc-cua-enzym.html Từ khóa tìm kiếm nhiều: hóa học lớp 10
Ở đây v = tốc độ phản ứng vmax = tốc độ tối đa [S] = nồng độ cơ chất Km = hằng số Michaelis của enzym đối vối cơ chất. Khi nồng độ cơ chất thấp hơn KM rất nhiều, nghĩa là với số lượng enzym vượt quá số lượng cơ chất, trong phương trình Michaelis-Menten, ta có thể bỏ [S] ở mẫu số, phương trình trở thành dạng v=Vmax [S]/ KM, đây là phương trình tuyến tính dạng y = ax, nghĩa là tốc độ phản ứng chỉ phụ thuộc vào nồng độ cơ chất [S]. Lúc này phản ứng là phản ứng động học bậc 1 bởi vì tốc độ phản ứng tỷ lệ thuận với nồng độ cơ chất. Khi nồng độ cơ chất tăng lên đến mức đạt giá trị bằng giá trị KM thì phương trình Michaelis-Menten trở thành dạng V = Vmax/2, có nghĩa là tốc độ phản ứng bằng 1/2 tốc độ tối đa. Khi nồng độ cơ chất lớn hơn KM rất nhiều thì ta có thể bở KM ở mẫu số của phương trình Michaelis-Menten, và phương trình trở thành dạng V = Vmax, có nghĩa là tốc độ phản ứng đạt tốc độ tối đa (Vmax). Lúc này tất cả các phân tử enzym đều bão hoà cơ chất, phản ứng đạt động học “bậc không”, bởi vì, dù có tiếp tục tăng nồng độ cơ chất thì tốc độ phản ứng cũng không thay đổi và lúc này tốc độ phản ứng chỉ phụ thuộc vào nồng độ enzym. Ý nghĩa của các giá trị KM : - KM là hằng số tổng hợp của các hằng số tốc độ, có giá trị bằng nồng độ cơ chất cần thiết để tốc độ phản ứng đạt bằng 1/2 tốc độ tối đa. Như vậy, KM được tính bằng mol/L. Đọc thêm tại: http://hoahocvasinhhoc.blogspot.com/2015/06/tim-hieu-ve-ong-hoc-cua-enzym.html Từ khóa tìm kiếm nhiều: hóa học lớp 10
0 nhận xét:
Đăng nhận xét
Bài đăng Mới hơn Bài đăng Cũ hơn Trang chủ Đăng ký: Đăng Nhận xét (Atom) Copyright 2010 Hóa học và sinh học.Từ khóa » Vmax Là Gì
-
VMAX Là Gì? -định Nghĩa VMAX | Viết Tắt Finder
-
VMAX định Nghĩa: Điện áp Tối đa - Maximum Voltage
-
Liên Quan đến Động Học Enzyme Đơn Vị Km Và Vmax đại Diện Cho ...
-
VMAX Là Gì, Nghĩa Của Từ VMAX | Từ điển Viết Tắt
-
Công Thức Tính Vmax Trong Dao động điều Hòa.
-
VMAX Tiếng Việt Là Gì - Trong Tiếng Việt Dịch - Tr-ex
-
VMAX - VNPT VinaPhone
-
“Đại Dương Xanh” Của Vmax - Brands Vietnam
-
Km Của Phản ứng Enzyme Là Gì
-
SỰ KHÁC NHAU GIỮA MÁY HIFU VMAX VÀ CÁC HIFU KHÁC
-
2 Thẻ VMAX Mới Của Pokemon TCG Sword & Shield - NShop
-
VinaPhone Ngừng Triển Khai Gói Vmax - Dịch Vụ Di Động
-
7 đơn Vị CSS Có Thể Bạn Không Biết - Viblo
-
Đăng Ký Gói VMax Vinaphone để được Miễn Phí Cuộc Gọi Dưới 10 Phút




