Trong Phân Tử Kẽm Oxit ZnO Cứ 16 Phần Khối Lượng Của Oxi Thì Có 65 ...
Có thể bạn quan tâm
HOC24
Lớp học Học bài Hỏi bài Giải bài tập Đề thi ĐGNL Tin tức Cuộc thi vui Khen thưởng- Tìm kiếm câu trả lời Tìm kiếm câu trả lời cho câu hỏi của bạn
Lớp học
- Lớp 12
- Lớp 11
- Lớp 10
- Lớp 9
- Lớp 8
- Lớp 7
- Lớp 6
- Lớp 5
- Lớp 4
- Lớp 3
- Lớp 2
- Lớp 1
Môn học
- Toán
- Vật lý
- Hóa học
- Sinh học
- Ngữ văn
- Tiếng anh
- Lịch sử
- Địa lý
- Tin học
- Công nghệ
- Giáo dục công dân
- Tiếng anh thí điểm
- Đạo đức
- Tự nhiên và xã hội
- Khoa học
- Lịch sử và Địa lý
- Tiếng việt
- Khoa học tự nhiên
- Hoạt động trải nghiệm
- Hoạt động trải nghiệm, hướng nghiệp
- Giáo dục kinh tế và pháp luật
Chủ đề / Chương
Bài học
HOC24
 Khách vãng lai Đăng nhập Đăng ký Khám phá Hỏi đáp Đề thi Tin tức Cuộc thi vui Khen thưởng
Khách vãng lai Đăng nhập Đăng ký Khám phá Hỏi đáp Đề thi Tin tức Cuộc thi vui Khen thưởng - Tất cả
- Toán
- Vật lý
- Hóa học
- Sinh học
- Ngữ văn
- Tiếng anh
- Lịch sử
- Địa lý
- Tin học
- Công nghệ
- Giáo dục công dân
- Tiếng anh thí điểm
- Hoạt động trải nghiệm, hướng nghiệp
- Giáo dục kinh tế và pháp luật
Câu hỏi
Hủy Xác nhận phù hợp Chọn lớp Tất cả Lớp 12 Lớp 11 Lớp 10 Lớp 9 Lớp 8 Lớp 7 Lớp 6 Lớp 5 Lớp 4 Lớp 3 Lớp 2 Lớp 1 Môn học Toán Vật lý Hóa học Sinh học Ngữ văn Tiếng anh Lịch sử Địa lý Tin học Công nghệ Giáo dục công dân Tiếng anh thí điểm Đạo đức Tự nhiên và xã hội Khoa học Lịch sử và Địa lý Tiếng việt Khoa học tự nhiên Hoạt động trải nghiệm Hoạt động trải nghiệm, hướng nghiệp Giáo dục kinh tế và pháp luật Mới nhất Mới nhất Chưa trả lời Câu hỏi hay
- Hồ Thị Linh Chi
Trong phân tử kẽm oxit ZnO cứ 16 phần khối lượng của oxi thì có 65,38 phần khối lượng kẽm. Tìm nguyên tử khối của Zn
Mog các bn giúp giùm mk ạ
Xem chi tiết Lớp 8 Hóa học Bài 5: Nguyên tố hóa học 1 0 Gửi Hủy
Gửi Hủy  Luân Đào
Luân Đào  29 tháng 8 2018 lúc 19:41
29 tháng 8 2018 lúc 19:41 Ta có: NTK O = 16 đvC
Theo đề ta được:
\(\dfrac{M_O}{M_{Zn}}=\dfrac{16}{65,38}\)
\(\Leftrightarrow\dfrac{16}{M_{Zn}}=\dfrac{16}{65,38}\)
\(\Leftrightarrow M_{Zn}=65,38\)
Vậy......................
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Lương Gia Phúc
Một hợp chất A có phân tử gồm nguyên tử nguyên tố X liên kết với 4 nguyên tử H và nặng bằng nguyên tử O
a/ Tính nguyên tử khối, cho biết tên và kí hiệu hóa học của nguyên tố X.
b/ Tính phần trăm về khối lượng của nguyên tố X trong hợp chất A. Biết rằng phần trăm về khối lượng của một nguyên tố trong hợp chât bằng phần trăm về khối lượng của nguyên tố đó trong 1 phân tử
Xem chi tiết Lớp 8 Hóa học Ôn tập học kỳ II 1 0 Gửi Hủy
Gửi Hủy  Đinh Thị Phương Thảo 7 tháng 10 2016 lúc 10:28
Đinh Thị Phương Thảo 7 tháng 10 2016 lúc 10:28 jpkoooooooooooooooo
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy 
- tran huynh trieu man
1) tính khối lượng mol (M) của kali pemanganat
2) Tính số mol nguyên tử và khối lượng của mỗi nguyên tố hóa học có trong một mol kali pemanganat
3) Trong phân tử kali pemanganat, nguyên tố nào có thành phần phần trăm theo khối lượng lớn nhất? Tại sao?
Xem chi tiết Lớp 8 Hóa học Bài 21: Tính theo công thức hóa học 2 0 Gửi Hủy
Gửi Hủy  Hoàng Tuấn Đăng 3 tháng 10 2016 lúc 17:35
Hoàng Tuấn Đăng 3 tháng 10 2016 lúc 17:35 1/ MKMnO4 = 39 + 55 + 16 x 4 = 158 g/mol
2/ K : 1 nguyên tủ
Mn: 1 nguyên tử
O2 : 4 nguyên tử
3/ Trong phân tử KMnO4 , nguyên tố O có thành phần phần trăm theo khối lượng lớn nhất vì O chiếm khối lượng lớn nhất ( là 64 gam)
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy  Phan Thị Diễm Quỳnh 24 tháng 11 2017 lúc 21:09
Phan Thị Diễm Quỳnh 24 tháng 11 2017 lúc 21:09 bt chết liền
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy 
- phát 8a6 nhuận
Một hợp chất A có khối lượng mol phân tử là 58,5g/mol thành phần các nguyên tố theo khối lượng 39,32% Na và còn lại là Cl xác định công thức phân tử của hợp chất
Xem chi tiết Lớp 8 Hóa học Bài 21: Tính theo công thức hóa học 5 0 Gửi Hủy
Gửi Hủy  hnamyuh
hnamyuh  5 tháng 1 2022 lúc 18:11
5 tháng 1 2022 lúc 18:11 %Cl = 100% - 39,32% = 60,68%Gọi CTHH của A là $Na_xCl_y$
Ta có :
$\dfrac{23x}{39,32} = \dfrac{35,5y}{60,68} = \dfrac{58,5}{100}$
Suy ra : $x = 1 ; y = 1$
Vậy CTHH của hợp chất là NaCl
Đúng 4 Bình luận (0) Gửi Hủy
Gửi Hủy  Kudo Shinichi
Kudo Shinichi  5 tháng 1 2022 lúc 18:11
5 tháng 1 2022 lúc 18:11 \(m_{Na}=\%Na.M_A=39,32\%.58,5=23\left(g\right)\\ m_{Cl}=m_A-m_{Na}=58,5-23=35,5\left(g\right)\\ \Rightarrow n_{Na}=\dfrac{23}{23}=1\left(mol\right)\\ n_{Cl}=\dfrac{35,5}{35,5}=1\left(mol\right)\\ CTHH:NaCl\)
Đúng 1 Bình luận (0) Gửi Hủy
Gửi Hủy  hnamyuh
hnamyuh  5 tháng 1 2022 lúc 18:11
5 tháng 1 2022 lúc 18:11 %Cl = 100% - 39,32% = 60,68%Gọi CTHH của A là $Na_xCl_y$
Ta có :
$\dfrac{23x}{39,32} = \dfrac{35,5y}{60,68} = \dfrac{58,5}{100}$
Suy ra : $x = 1 ; y = 1$
Vậy CTHH của hợp chất là NaCl
Đúng 0 Bình luận (1) Gửi Hủy Xem thêm câu trả lời
Gửi Hủy Xem thêm câu trả lời 
- Lan Kiều
Phân tử nhôm bromua là hợp chất đc tạo nên từ 1 nguyên tử Al và 3 nguyên tử br tính thành phần phần trăm theo khối lượng của các nguyên tố có trong hợp chất
Xem chi tiết Lớp 8 Hóa học CHƯƠNG I: CHẤT - NGUYÊN TỬ - PHÂN TỬ 1 0 Gửi Hủy
Gửi Hủy  Đặng Yến Linh 6 tháng 10 2016 lúc 7:48
Đặng Yến Linh 6 tháng 10 2016 lúc 7:48 công thuc hoa hoc la AlBr3
nguyen tu khoi cua Br = 80
%Al = 27/(27+80.3) = 10%
%Br = 90%
Đúng 0 Bình luận (0)
 Gửi Hủy
Gửi Hủy 
- Nguyễn Huyền Diệu
Lập CTHH của 1 chất biết khối lượng phân tử hợp chất là 142. thành phần khối lượng của các nguyên tố là 32,39% Na, 22,54% S, 45,07% O.
Xem chi tiết Lớp 8 Hóa học Bài 9: Công thức hóa học 2 0 Gửi Hủy
Gửi Hủy  Lê Nguyên Hạo
Lê Nguyên Hạo  5 tháng 8 2016 lúc 10:33
5 tháng 8 2016 lúc 10:33 Tìm số mol mỗi chất - Na: 142x32,39%/23= 2 mol - S: 142x22,54%/32 = 1 mol - O: 142x45,07%/16=4 mol Tỉ lệ mol: Na:S:O=2:1:4 ===> công thức cần tìm là Na2SO4
Đúng 0 Bình luận (1) Gửi Hủy
Gửi Hủy  haphuong01 5 tháng 8 2016 lúc 12:17
haphuong01 5 tháng 8 2016 lúc 12:17 gọi công thức hóa học là : NaxSyOy
theo đề ta có : x:y:z=\(\frac{32,39}{23}:\frac{22,54}{32}:\frac{45,07}{16}\)=1:1:3
vậy công thức hóa học là :NaSO3
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Nguyễn Văn Gia Thịnh
-
Trong phân tử hợp chất X có 75% khối lượng là Aluminium,còn lại là Carbon,và khối lượng phân tử của hợp chất là 144amu.Tính phần nguyên tố Carbon trong hợp chất X?Xác định công thức hóa học của hợp chất X.Giúp mình làm câu này với😣😣😍😍
Xem chi tiết Lớp 7 Khoa học tự nhiên 1 1 Gửi Hủy
Gửi Hủy  『Kuroba ム Tsuki Ryoo...
『Kuroba ム Tsuki Ryoo...  3 tháng 1 2023 lúc 14:33
3 tháng 1 2023 lúc 14:33 Gọi ct chung: \(Al_xC_y\)
\(\%C=100\%-75\%=25\%\%\)
\(K.L.P.T=27.x+12.y=144< amu>.\)
\(\%Al=\dfrac{27.x.100}{144}=75\%\)
\(Al=27.x.100=75.144\)
\(Al=27.x.100=10800\)
\(Al=27.x=10800\div100\)
\(27.x=108\)
\(x=108\div27=4\)
Vậy, có 4 nguyên tử Al trong phân tử `Al_xC_y`
\(\%C=\dfrac{12.y.100}{144}=25\%\)
\(\Rightarrow y=3\) (cách làm tương tự phần trên nha).
Vậy, có 3 nguyên tử C trong phân tử trên.
\(\Rightarrow CTHH:Al_4C_3\)
Đúng 2 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Phạm Amanaki
1) tính khối lượng gam của các nguyên tố có trong 10g CuSO4
2) trong phân tử R2On (R là nguyên tố chưa biết; n chưa biết). trong phân tử trên, nguyên tố R chiếm 80% về khối lượng. tính % về khối lượng của các nguyên tố có trong phân tử R2(SO4)n
Xem chi tiết Lớp 8 Hóa học Bài 6: Đơn chất và hợp chất - Phân tử 1 0 Gửi Hủy
Gửi Hủy  Lê Mỹ Linh 26 tháng 10 2017 lúc 20:06
Lê Mỹ Linh 26 tháng 10 2017 lúc 20:06 1/ Số mol CuSO4 trong 10g CuSO4 là:
\(n_{CuSO_4}=\dfrac{m}{M}=\dfrac{10}{160}=0,0625\left(mol\right)\)
Vậy, \(m_{Cu}=0,0625\cdot64=4\left(g\right)\)
\(m_S=0,0625\cdot32=2\left(g\right)\)
\(m_O=0,0625\cdot4\cdot16=4\left(g\right)\)
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Nguyen Hoang Dieu
Bài 1: Hãy tính khối lượng riêng của 1 khối đồng (đồng pha kẽm) biết đồng có khối lượng là 17,8 kg; kẽm có khối lượng là 35,5 kg và khối lượng riêng của đồng là 8900 kg/m3, khối lượng riêng của kẽm là 7100 kg/m3.
Bài 2: Mỗi hòn gạch có 2 lỗ và có khối lượng là 1,6 kg; hòn gạch có thể tích là 1200 cm3, mỗi lỗ có thể tích là 192 cm3. Tính khối lượng riêng và trọng lượng riêng của hòn gạch.
Bài 3: Nếu dùng một cái chai đựng đầy nước thì khối lượng nước trong chai là 21,5 kg. Hỏi nếu dùng chai này đựng đầy thuỷ ngân thì khối lượng của thuỷ ngân trong chai là bao nhiêu? Biết khối lượng riêng của nước là 1000 kg/m3, khối lượng riêng của thuỷ ngân là 13600 kg/m3.
Xem chi tiết Lớp 6 Toán Câu hỏi của OLM 2 0 Gửi Hủy
Gửi Hủy  Trần Thị Loan
Trần Thị Loan  21 tháng 6 2015 lúc 19:59
21 tháng 6 2015 lúc 19:59 1) Thể tích của đồng là: 17, 8 : 8900 = 2 dm3
Thể tích của kẽm là : 35,5 : 7100 = 5 dm3
Thể tích của đồng và kẽm là: 2 + 5 = 7 dm3 = 0,007 m3
Khối lượng riêng của khối đồng pha kẽm là: (17 ,8 + 35,5 ) : 0,007 = 7614 kg/m3
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy  Trần Thị Loan
Trần Thị Loan  21 tháng 6 2015 lúc 20:06
21 tháng 6 2015 lúc 20:06 2) Thể tích hòn gạch có lỗ là: 1200 - (192 x 2) = 816 cm3
Khối lượng riêng là: 1,6 : 816 = 1,96 g/cm3
3) Thể tích của chai là: 21,5 : 1000 = 0, 0215 m3
Khối lương thủy ngân là: 0,0215 x 13 600 = 292,4 kg
Đúng 0 Bình luận (0) Gửi Hủy
Gửi Hủy 
- Hoàng Đức Long
Một lượng khí có khối lượng là 30 kg và chứa 11 , 28 . 10 26 phân tử. Phân tử khí này gồm các nguyên tử hiđrô và cacbon. Biết 1 mol khí có N A = 6 , 02 . 10 23 phân tử. Khối lượng của các nguyển tử cacbon và hiđrô trong khí này là
A. m C = 2 . 10 - 26 k g ; m H = 0 , 66 . 10 - 26 k g
B. m C = 4 . 10 - 26 k g ; m H = 1 , 32 . 10 - 26 k g
C. m C = 2 . 10 - 6 k g ; m H = 0 , 66 . 10 - 6 k g
D. m C = 4 . 10 - 6 k g ; m H = 1 , 32 . 10 - 6 k g
Xem chi tiết Lớp 10 Vật lý 1 0 Gửi Hủy
Gửi Hủy  Vũ Thành Nam
Vũ Thành Nam  26 tháng 10 2017 lúc 9:20
26 tháng 10 2017 lúc 9:20 Chọn A.
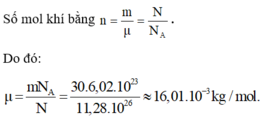
Trong khi có hiđrô và cacbon, chí CH4 có
μ = (12 + 4).10-3 kg/mol
Vì thế, khí đã cho là CH4. Khối lượng của 1 phân tử khí CH4 là 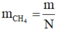
Khối lượng của nguyên tử hiđrô là:
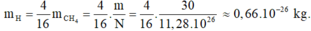
Khối lượng của nguyên tử cacbon là:
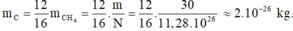
 Gửi Hủy
Gửi Hủy Từ khóa » Nguyên Tử Khối Zno
-
ZnO (Kẽm Ôxít) Khối Lượng Mol - ChemicalAid
-
Tìm Nguyên Tử Khối Của Zn? - Nguyễn Minh Hải - Hoc247
-
Các Chất Hóa Học Có Chứa Phân Tử ZnO
-
Kẽm Oxide – Wikipedia Tiếng Việt
-
Viết Công Thức Hóa Học Và Tính Phân Tử Khối Của Các Hợp Chất Sau
-
Kẽm Oxit ZnO - Mua Kẽm Oxit ở đâu Giá TỐT, Chất Lượng? - VietChem
-
Thông Tin Chất ZnO(kẽm Oxit)
-
De Thi Hoa 8 - Tài Liệu Text - 123doc
-
Khối Lượng Mol Của Kẽm
-
(PDF) Study On The Effect Of Ag Nanoparticles Density On ZnO/Ag ...
-
Ứng Dụng Nano ZnO Làm Phân Bón Vi Lượng
-
[PDF] CHẾ TẠO VÀ NGHIÊN CỨU TÍNH CHẤT CỦA VẬT LIỆU ZnO PHA ...