Viết Phương Trình Hóa Học Thực Hiện Dãy Chuyển Hóa Lớp 9
Có thể bạn quan tâm
-
-

-
Mầm non
-
Lớp 1
-
Lớp 2
-
Lớp 3
-
Lớp 4
-
Lớp 5
-
Lớp 6
-
Lớp 7
-
Lớp 8
-
Lớp 9
-
Lớp 10
-
Lớp 11
-
Lớp 12
-
Thi vào lớp 6
-
Thi vào lớp 10
-
Thi Tốt Nghiệp THPT
-
Đánh Giá Năng Lực
-
Khóa Học Trực Tuyến
-
Hỏi bài
-
Trắc nghiệm Online
-
Tiếng Anh
-
Thư viện Học liệu
-
Bài tập Cuối tuần
-
Bài tập Hàng ngày
-
Thư viện Đề thi
-
Giáo án - Bài giảng
-
Tất cả danh mục
-
- Mầm non
- Lớp 1
- Lớp 2
- Lớp 3
- Lớp 4
- Lớp 5
- Lớp 6
- Lớp 7
- Lớp 8
- Lớp 9
- Lớp 10
- Lớp 11
- Lớp 12
- Thi Chuyển Cấp
-
- Hôm nay +3
- Ngày 2 +3
- Ngày 3 +3
- Ngày 4 +3
- Ngày 5 +3
- Ngày 6 +3
- Ngày 7 +5
Nâng cấp gói Pro để trải nghiệm website VnDoc.com KHÔNG quảng cáo, và tải file cực nhanh không chờ đợi.
Tìm hiểu thêm » Mua ngay Từ 79.000đ Hỗ trợ ZaloViết phương trình phản ứng
- Viết các phương trình hóa học biểu diễn các chuyển hóa sau đây
- Phương pháp làm dạng chuỗi phản ứng
- Câu hỏi bài tập vận dụng liên quan
Viết phương trình hóa học thực hiện dãy chuyển hóa lớp 9 được VnDoc biên soạn hướng dẫn các bạn học sinh hoàn thành tốt chuỗi phản ứng hóa học lớp 9 môn Khoa học tự nhiên.
Viết các phương trình hóa học biểu diễn các chuyển hóa sau đây
a) Fe ![]() FeCl3
FeCl3 ![]() Fe(OH)3
Fe(OH)3 ![]() Fe2(SO4)3
Fe2(SO4)3 ![]() FeCl3
FeCl3
b) Fe(NO3)3 ![]() Fe(OH)3
Fe(OH)3 ![]() Fe2O3
Fe2O3 ![]() Fe
Fe ![]() FeCl2
FeCl2 ![]() Fe(OH)2
Fe(OH)2
Phương pháp làm dạng chuỗi phản ứng
Nắm chắc tính chất hóa học của kim loại Fe
- Tác dụng với phi kim
Với oxi: 3Fe + 2O2 ![]() Fe3O4
Fe3O4
Ở nhiệt độ cao, sắt phản ứng được với nhiều phi kim, Cl2, S, O2,...
- Tác dụng với dung dịch acid
Tác dụng với với HCl, H2SO4 loãng
Fe + 2HCl → FeCl2 + H2
Tác dụng với H2SO4 đặc, nóng; HNO3 đặc:
2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2 + 6H2O
Không tác dụng với H2SO4 đặc nguội, HNO3 đặc, nguội
- Tác dụng với dung dịch muối
Đẩy được kim loại yếu hơn ra khỏi muối
Fe + CuSO4 → FeSO4 + Cu
Đáp án hướng dẫn giải chi tiết
Phương trình hóa học:
a)
(1) Fe + 3Cl2 ![]() 2FeCl3
2FeCl3
(2) FeCl3 + 3NaOH → Fe(OH)3 + 3NaCl
(3) 2Fe(OH)3 + 3H2SO4 → Fe2(SO4)3 + 6H2O
(4) Fe2(SO4)3 + 3BaCl2 → 3BaSO4 + 2FeCl3
b)
(1) Fe(NO3)3 + 3NaOH → Fe(OH)3 + 3NaNO3
(2) 2Fe(OH)3 ![]() Fe2O3 + 3H2O
Fe2O3 + 3H2O
(3) Fe2O3 + 3CO → 2Fe + 3CO2
(4) Fe + 2HCl → FeCl2 + H2
(5) FeCl2 + 2NaOH → Fe(OH)2 + 2NaCl
Câu hỏi bài tập vận dụng liên quan
Câu 1. CaCl2 → NaCl → Cl2 → CaOCl2 → CaCO3 → CaCl2 → NaCl
Hướng dẫn hoàn thành chuỗi phản ứng hóa học
1)CaCl2 + Na2CO3→ NaCl + CaCO3
2) NaCl ![]() Na + Cl2
Na + Cl2
3) 2Cl2 + 2Ca(OH)2 → Ca(OCl)2 + CaCl2 + 2H2O
4) 2CaOCl2 + H2O + CO2 → CaCl2 + CaCO3 + 2HClO
5) CaCO3 + 2HCl → CaCl2 + H2O + CO2
6) CaCl2 + Na2CO3 → CaCO3 + 2NaCl
Câu 2. Hoàn thành chuỗi phản ứng sau: S → SO2 → SO3 → H2SO4 → SO2 → H2SO3 → Na2SO3 → SO2
Hướng dẫn hoàn thành chuỗi phản ứng hóa học
(1) S + O2 ![]() SO2
SO2
(2) SO2 + O2 ![]() SO3
SO3
(3) SO3 + H2O → H2SO4
(4) H2SO4 + Na2SO3 → Na2SO4 + SO2 + H2O
(5) SO2 + H2O→ H2SO3
(6) H2SO3 + 2NaOH → Na2SO3 + 2H2O
(7) H2SO4 + Na2SO3 → Na2SO4 + SO2 + H2
Câu 3. Hoàn thành chuỗi phản ứng sau:
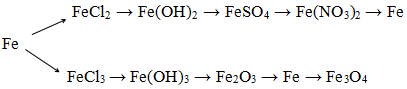
Hướng dẫn hoàn thành chuỗi phản ứng hóa học
Fe + 2HCl → FeCl2 + H2
FeCl2 + NaOH → Fe(OH)2 + NaCl
Fe(OH)2 + H2SO4 → FeSO4 + H2
FeSO4 + Ba(NO3)2 → Fe(NO3)2 + BaSO4
4Fe(NO3)2 → 2Fe2O3 + 8NO2 + O2
2 Fe + 3 Cl2 → 2 FeCl3
FeCl3 + 3 NaOH → Fe(OH)3 + 3 NaCl
2Fe(OH)3 → Fe2O3 + 3 H2O
Fe2O3 + 3CO → 2Fe + 3CO2
3Fe + 2O2 → Fe3O4
Câu 4. Hoàn thành chuỗi phản ứng sau: FeS2 → SO2 → SO3 → H2SO4 → ZnSO4 → Zn(OH)2 → ZnO → Zn
Hướng dẫn hoàn thành chuỗi phản ứng hóa học
1) 4FeS2 + 11O2 → 2Fe2O3 + 8SO2
2) 2SO2 + O2 → 2SO3
3) SO3 + H2O → H2SO4
4) H2SO4 +Zn → ZnSO4 + H2
5) ZnSO4 + 2NaOH → Zn(OH)2 + Na2SO4
6) Zn(OH)2 → ZnO + H2O
Câu 5. Hoàn thành chuỗi phản ứng sau: MnO2 → Cl2 → KClO3 → KCl → HCl → Cl2 → clorua vôi
Hướng dẫn hoàn thành chuỗi phản ứng hóa học
1) MnO2 + 4HCl ![]() MnO2 + Cl2 + H2O
MnO2 + Cl2 + H2O
2) 3Cl2 + 6KOH(đặc) ![]() 5KCl + KClO3 + 3H2O
5KCl + KClO3 + 3H2O
3) KClO3![]() KCl + 3O2
KCl + 3O2
4) KCl(rắn) + H2SO4 ![]() 2HCl + K2SO4
2HCl + K2SO4
5) 4HCl + MnO2 ![]() MnO2 + Cl2 + H2O
MnO2 + Cl2 + H2O
6) Cl2 + Ca(OH)2![]() CaOCl2 + H2O
CaOCl2 + H2O
Câu 6. Hoàn thành chuỗi phản ứng sau: Al → Al2O3 → NaAlO2 →Al(OH)3 → Al2(SO4)3 → AlCl3→ Al(NO3)3
Hướng dẫn hoàn thành chuỗi phản ứng hóa học
1) 4Al + 3O2 → 2Al2O3
2) Al2O3 + 2NaOH → 2NaAlO2 + H2O
3) NaAlO2 + 2H2O → NaOH + Al(OH)3
4) 2Al(OH)3 + 3ZnSO4 → Al2(SO4)3 + 3Zn(OH)2
5) Al2(SO4)3 + 3BaCl2 → 2AlCl3 + 3BaSO4
6) AlCl3 + 3AgNO3 → Al(NO3)3 + 3AgCl
Câu 7. Hoàn thành chuỗi phản ứng sau: FeS2 → SO2 → SO3 → H2SO4 → ZnSO4 → Zn(OH)2 → ZnO → Zn
Hướng dẫn hoàn thành chuỗi phản ứng hóa học
1) 4FeS2 + 11O2 → 2Fe2O3 + 8SO2
2) 2SO2 + O2 → 2SO3
3) SO3 + H2O → H2SO4
4) H2SO4 +Zn → ZnSO4 + H2
5) ZnSO4 + 2NaOH → Zn(OH)2 + Na2SO4
6) Zn(OH)2 → ZnO + H2
Câu 8. Hoàn thành chuỗi phản ứng sau: Na → NaOH → Na2CO3 → NaHCO3 → NaOH → NaCl → NaOH → Na → NaH → NaOH → NaCl + NaOCl
Hướng dẫn hoàn thành chuỗi phản ứng hóa học
1) 2Na + 2H2O → 2NaOH + H2
2) 2NaOH + CO2 → Na2CO3 + H2O
3) Na2CO3 + CO2 + H2O → 2NaHCO3
4) 2NaHCO3 + Ca(OH)2 → CaCO3 + 2NaOH + 2H2O
5) NaOH + HCl → NaCl + H2O
6) 2NaCl + 2H2O → 2NaOH + Cl2 + H2
7) 4NaOH → 4Na + O2 + 2H2O
8) 2Na + H2 → 2NaH
9) NaH + H2O → NaOH + H2
10) 2NaOH + Cl2 → NaCl + NaOCl + H2O
Câu 9. Hoàn thành chuỗi phản ứng sau: Al → Al2O3 → Al(NO3)3 → Al(OH)3 → Na[Al(OH)4] → Al(OH)3 → Al2O3 → Na[Al(OH)4] → Al2(SO4)3 → KAl(SO4)2.12H2O
Hướng dẫn hoàn thành chuỗi phản ứng hóa học
1) 4Al + 3O2 ![]() 2Al2O3
2Al2O3
2) Al2O3 + 6HNO3 → 2Al(NO3)3 + 3H2O
3) Al(NO3)3 + 3NH3 + 3H2O → Al(OH)3 + 3NH4NO3
4) Al(OH)3 + NaOH → Na[Al(OH)4]
5) K[Al(OH)4] + CO2 → Al(OH)3 + KHCO3
6) 2Al(OH)3 → 2Al2O3 + 3H2O
7) Al2O3 + 2NaOH + 3H2O → 2Na[Al(OH)4]
8) 2K[Al(OH)4] + 4H2SO4 → Al2(SO4)3 + K2SO4 + 4H2O
9) Al2(SO4)3 + K2SO4 + 24H2O → 2KAl(SO4)2.12H2O
Câu 10. Hoàn thành chuỗi phản ứng sau: Fe → FeCl3 → Fe(OH)3 → Fe2O3 → Fe2(SO4)3 → FeSO4 → Fe(OH)2 → Fe(NO3)3 → Fe(NO3)2 → FeO
Hướng dẫn hoàn thành chuỗi phản ứng hóa học
2Fe + 3Cl2 → 2FeCl3
FeCl3 + 3NaOH → Fe(OH)3 + 3NaCl
2Fe(OH)3 → Fe2O3 + 3H2O
Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O
Fe2(SO4)3 + Cu → 2FeSO4 + CuSO4
FeSO4 + NaOH → Fe(OH)2 + Na2SO4
Fe(OH)2 + 4HNO3 → Fe(NO3)3 + NO2 + 3H2O
2Fe(NO3)3 + Fe → 3Fe(NO3)2
2Fe(NO3)2 → 2FeO + 4NO2 + O2
Câu 11. Hoàn thành chuỗi phản ứng sau:
Mg → MgO → MgCl2 → Mg(NO3)2 → Mg(OH)2 → MgO → MgSO4 → MgCO3 → Mg(HCO3)2
Hướng dẫn hoàn thành chuỗi phản ứng hóa học(1) 2Mg + O2 → 2MgO
(2) MgO + 2HCl → MgCl2 + H2
3) MgCl2 + 2AgNO3 → Mg(NO3)2 + 2AgCl
4) Mg(NO3)2 + 2NaOH → Mg(OH)2 + 2NaNO3
5) Mg(OH)2 → MgO + H2O
6) MgO + Na2SO4 → MgSO4 + H2O
7) MgSO4 + Na2CO3 → MgCO3 + Na2SO4
8) MgCO3 + CO2+ H2O → Mg(HCO3)2
Câu 12. Hoàn thành chuỗi phản ứng sau: Na → NaOH → Na2CO3 → Na2SO4 → NaCl.
Hướng dẫn hoàn thành chuỗi phản ứng hóa học
Na + H2O → NaOH + H2↑
2NaOH + CO2 → Na2CO3 + H2O
Na2CO3 + H2SO4 → Na2SO4 + H2O + CO2↑
Na2SO4 + BaCl2 → BaSO4↓ + 2NaCl.
Câu 13. Hoàn thành chuỗi phản ứng sau: Ba → BaO → Ba(OH)2 → BaCO3 → BaO → BaCl2
Hướng dẫn hoàn thành chuỗi phản ứng hóa học
(1) 2Ba + O2→ 2BaO
(2) BaO + H2O→ Ba(OH)2
(3) Ba(OH)2 + CO2 → BaCO3↓ + H2O
(4) BaCO3→ BaO + CO2.
(5) BaO + 2HCl→ BaCl2 + H2O.
(6) BaCl2 + 2AgNO3 → Ba(NO3)2 + 2AgCl
.............................................
Đóng Chỉ thành viên VnDoc PRO/PROPLUS tải được nội dung này! Đóng 79.000 / tháng Mua ngay Đặc quyền các gói Thành viên PRO Phổ biến nhất PRO+ Tải tài liệu Cao cấp 1 Lớp 30 lượt tải tài liệu Xem nội dung bài viết Trải nghiệm Không quảng cáo Làm bài trắc nghiệm không giới hạn Tìm hiểu thêm Mua cả năm Tiết kiệm tới 48%- Chia sẻ bởi:
 Nguyễn Thị Phương Tuyết
Nguyễn Thị Phương Tuyết

Có thể bạn quan tâm
Xác thực tài khoản!Theo Nghị định 147/2024/ND-CP, bạn cần xác thực tài khoản trước khi sử dụng tính năng này. Chúng tôi sẽ gửi mã xác thực qua SMS hoặc Zalo tới số điện thoại mà bạn nhập dưới đây:
Số điện thoại chưa đúng định dạng! Xác thực ngay Số điện thoại này đã được xác thực! Bạn có thể dùng Sđt này đăng nhập tại đây! Lỗi gửi SMS, liên hệ Admin Sắp xếp theo Mặc định Mới nhất Cũ nhất-
Phân môn Vật lí
- Động năng là gì? Công thức tính động năng
- Công thức tính cường độ dòng điện
- Bài tập Khoa học tự nhiên 9 Chương 1 Năng lượng cơ học
- Bài tập Khoa học tự nhiên 9 Chương 3 Điện
-
Phân môn Hóa học
- Tổng hợp kiến thức Hóa THCS
- Bài tập Khoa học tự nhiên 9 Chương 6 Kim loại. Sự khác nhau cơ bản giữa phi kim và kim loại
- Viết phương trình hóa học thực hiện dãy chuyển hóa lớp 9
- Chuỗi phản ứng Hóa học vô cơ
- Bài tập Khoa học tự nhiên 9 Kim loại
- Cách nhận biết các chất hóa học lớp 8 và 9
- Công thức tính nồng độ đương lượng
- Độ cồn là gì? Công thức tính độ cồn
- Chuỗi phản ứng hóa học hữu cơ lớp 9 Có đáp án
- Hóa học lớp 9: Nhận biết - Phân biệt các chất
-
Câu hỏi ôn tập
- Kim loại tác dụng với H2SO4 loãng
-
Ôn thi HSG
- 20 chuyên đề bồi dưỡng học sinh giỏi môn Hóa lớp 9
- Tuyển tập 30 đề thi học sinh giỏi Hóa lớp 9
- Tổng hợp đề thi học sinh giỏi Khoa học tự nhiên lớp 9
-
 Lớp 9
Lớp 9 -
 Hóa 9 - Giải Hoá 9
Hóa 9 - Giải Hoá 9 -
 Đề thi Khảo sát lớp 9
Đề thi Khảo sát lớp 9 -
 Đề thi giữa kì 1 lớp 9
Đề thi giữa kì 1 lớp 9 -
 Đề thi học kì 1 lớp 9
Đề thi học kì 1 lớp 9 -
 Đề thi giữa kì 2 lớp 9
Đề thi giữa kì 2 lớp 9 -
 Đề thi học kì 2 lớp 9
Đề thi học kì 2 lớp 9 -
 Đề thi học kì 2 lớp 9 môn Toán
Đề thi học kì 2 lớp 9 môn Toán -
 Đề thi học kì 2 lớp 9 môn Văn
Đề thi học kì 2 lớp 9 môn Văn -
 Đề thi học kì 2 lớp 9 môn Tiếng Anh
Đề thi học kì 2 lớp 9 môn Tiếng Anh -
 Đề thi học kì 2 lớp 9 môn Vật Lý
Đề thi học kì 2 lớp 9 môn Vật Lý -
 Đề thi học kì 2 lớp 9 môn Hóa
Đề thi học kì 2 lớp 9 môn Hóa -
 Đề thi học kì 2 lớp 9 môn Sinh Học
Đề thi học kì 2 lớp 9 môn Sinh Học -
 Đề thi học kì 2 lớp 9 môn Lịch Sử
Đề thi học kì 2 lớp 9 môn Lịch Sử -
 Đề thi học kì 2 lớp 9 môn Địa
Đề thi học kì 2 lớp 9 môn Địa
Tham khảo thêm
-
Nhận biết CH4, C2H4, CO2
-
Hóa học lớp 9: Nhận biết - Phân biệt các chất
-
Bản tường trình hóa học 9 bài 33
-
Công thức tính hiệu suất phản ứng hóa học
-
Chuỗi phản ứng Hóa học vô cơ
-
Chứng minh 3 điểm thẳng hàng trong đường tròn
-
Hóa học lớp 9: Nhận biết - Phân biệt các chất
-
Viết phương trình hóa học thực hiện dãy chuyển hóa lớp 9
-
Tài liệu bồi dưỡng học sinh giỏi Hóa lớp 9 phần hữu cơ
-
Bài tập Khoa học tự nhiên 9 Kim loại

Hóa 9 - Giải Hoá 9
-
Nhận biết CH4, C2H4, CO2
-
Bài tập Khoa học tự nhiên 9 Kim loại
-
Viết phương trình hóa học thực hiện dãy chuyển hóa lớp 9
-
Bản tường trình hóa học 9 bài 33
-
Chuỗi phản ứng Hóa học vô cơ
-
Tài liệu bồi dưỡng học sinh giỏi Hóa lớp 9 phần hữu cơ

Gợi ý cho bạn
-
Bộ đề kiểm tra cuối tuần Tiếng Việt lớp 4 Kết nối tri thức Tuần 21
-
Bài tập cuối tuần Tiếng Việt lớp 4 Kết nối tri thức Tuần 21 Nâng cao
-
Cặp chất nào sau đây cùng tồn tại trong một dung dịch?
-
Bản tường trình Hóa học 9 bài 23
-
Tài liệu bồi dưỡng học sinh giỏi môn Hóa lớp 9
-
Đề thi học sinh giỏi môn Hóa học lớp 9 năm học 2014 - 2015 huyện Thiệu Hóa, Thanh Hóa
-
Bài tập câu điều kiện có đáp án
-
Bài tập tiếng Anh lớp 10 Unit 1 Family life nâng cao
-
Bộ đề thi học kì 1 Hóa 9 năm học 2023 - 2024 Có đáp án (11 đề)
Từ khóa » Cách Viết Pthh Lớp 9
-
Cách Viết Phương Trình Hóa Học Hay, Chi Tiết - Lớp 9
-
Tổng Hợp Các Phương Trình Hóa Học Lớp 9 Cần Nhớ Dành Cho Học Sinh
-
Hoá Học 9 ||Viết PTHH Hoàn Thành Dãy Chuyển Hoá - YouTube
-
Cách Viết Công Thức Hóa Học – Dành Cho Học Sinh Mất Gốc - YouTube
-
Các Phương Trình Phản Ứng Hóa Học Lớp 9, Bài Tập Viết Phương ...
-
Phương Trình Hóa Học Lớp 9 - CungHocVui
-
Bài Tập Viết Phương Trình Hóa Học Lớp 9
-
Công Thức Hóa Học Lớp 9 - Trung Tâm Gia Sư Tâm Tài Đức
-
Tổng Hợp Chuỗi Phương Trình Hóa Học Lớp 9 | Bán Máy Nước Nóng
-
PHƯƠNG TRÌNH HÓA HỌC LỚP 9 - 123doc
-
13 Cách Cân Bằng Phương Trình Hóa Học Nhanh Và Chính Xác
-
Viết Các Phương Trình Hóa Học Thực Hiện Dãy Chuyển Hóa Sau (ghi Rõ ...
-
Bài 3 Trang 41 SGK Hóa 9, Viết Phương Trình Hóa Cho Những ...
-
Cách Lập Phương Trình Hóa Học - .vn
































