30 Bài Tập Đồng Vị Hóa 10 Chương 1 Nguyên Tử Nâng Cao - HOC247
Có thể bạn quan tâm
Câu hỏi trắc nghiệm (30 câu):
-
Câu 1: Mã câu hỏi: 20387
Trong tự nhiên clo có 2 đồng vị là 35Cl và 37Cl. Nguyên tử khối trung bình của clo là 35,5. Thành phần % khối lượng của 37Cl trong KClO3 là (cho K = 39, O = 16)
- A. 7,24%
- B. 7,55%.
- C. 25,00%.
- D. 28,98%.
-
Câu 2: Mã câu hỏi: 20388
Trong tự nhiên đồng có 2 đồng vị là 63Cu và 65Cu. Nguyên tử khối trung bình của đồng là 63,54. Thành phần % khối lượng của 63Cu trong CuCl2 là (cho Cl = 35,5)
- A. 12,64%.
- B. 26,77%.
- C. 27,00%.
- D. 34,18%.
-
Câu 3: Mã câu hỏi: 20389
Trong tự nhiên đồng có 2 đồng vị là 63Cu và 65Cu. Nguyên tử khối trung bình của Cu là 63,54. Tính thành phần % khối lượng của 63Cu trong CuSO4?
- A. 28,83%.
- B. 10,97%
- C. 11,00%.
- D. 28,74%.
-
Câu 4: Mã câu hỏi: 20390
Trong tự nhiên đồng có hai đồng vị là \({}_{29}^{65}Cu\) và \({}_{29}^{63}Cu\) biết nguyên tử khối trung bình của Cu là 63,54. Phần trăm khối lượng của \({}_{29}^{63}Cu\) trong Cu2O là
- A. 73%.
- B. 64,29%.
- C. 35,71%.
- D. 27%.
-
Câu 5: Mã câu hỏi: 20391
Trong tự nhiên đồng có hai đồng vị là \({}_{29}^{65}Cu\) và \({}_{29}^{63}Cu\) trong đó đồng vị \({}_{29}^{65}Cu\) chiếm 27% về số nguyên tử. Phần trăm khối lượng của \({}_{29}^{63}Cu\) trong CuSO4.5H2O là
- A. 7,03.
- B. 73.
- C. 27.
- D. 18,43.
-
Câu 6: Mã câu hỏi: 20393
Trong tự nhiên kali gồm 3 đồng vị 39K chiếm 93,26% và đồng vị 40K chiếm 0,012% và đồng vị 41K. Brom là hỗn hợp hai đồng vị 79Br và 81Br với nguyên tử khối trung bình của Br là 79,92. Thành phần % khối lượng của 39K trong KBr là
- A. 30,56%.
- B. 29,92%.
- C. 31,03%.
- D. 30,55%.
-
Câu 7: Mã câu hỏi: 20395
Nitơ trong thiên nhiên là hỗn hợp gồm hai đồng vị là 147N (99,63%) và A7N (0,37%). Trong HNO3 14N chiếm 22,1387% khối lượng. Nguyên tử khối của đồng vị thứ hai của Nitơ là:
- A. 14.
- B. 15.
- C. 16.
- D. 13.
-
Câu 8: Mã câu hỏi: 20396
Đồng trong tự nhiên gồm hai loại đồng vị là \({}_{29}^{65}Cu\) và \({}_{29}^{63}Cu\)trong đó tỉ lệ số nguyên tử \({}_{29}^{65}Cu\) : \({}_{29}^{63}Cu\) = 81 : 219. Nếu hoàn tan một miếng đồng nặng 19,062 gam bằng dung dịch HNO3 loãng thì thể tích khí NO (đktc) thu được là: (3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O)
- A. 2,24.
- B. 3,36.
- C. 4,48.
- D. 6,72.
-
Câu 9: Mã câu hỏi: 20397
Trong tự nhiên, nguyên tố clo có hai đồng vị bền là \({}_{17}^{35}Cl\) và \({}_{17}^{37}Cl\) , trong đó đồng vị \({}_{17}^{35}Cl\) chiếm 75,77% về số nguyên tử. Phần trăm khối lượng của \({}_{17}^{37}Cl\) trong CaCl2 là
- A. 47,78%.
- B. 48,46%.
- C. 16,16%.
- D. 22,78%.
-
Câu 10: Mã câu hỏi: 20398
Đồng có 2 đồng vị 63Cu và 65Cu. Nguyên tử khối trung bình của đồng bằng 63,5. Tính số nguyên tử 65Cu có trong 16 gam CuSO4 khan.
- A. 4,515.1022 nguyên tử
- B. 1,55.1022 nguyên tử
- C. 1,505.1022 nguyên tử
- D. 4,52.1022 nguyên tử.
-
Câu 11: Mã câu hỏi: 20400
Nguyên tố X có hai đồng vị X1 và X2. Tổng số hạt không mang điện trong X1 và X2 là 90. Nếu cho 1,2 gam Ca tác dụng với một lượng X vừa đủ thì thu được 5,994 gam hợp chất CaX2. Biết tỉ lệ số nguyên tử X1 : X2 = 9 : 11. Số khối của X1, X2 lần lượt là
- A. 81 và 79.
- B. 75 và 85.
- C. 79 và 81.
- D. 85 và 75.
-
Câu 12: Mã câu hỏi: 20401
Trong tự nhiên Cu có hai đồng vị: 6329Cu; 6529Cu. Khối lượng nguyên tử trung bình của Cu là 63,54. Thành phần % về khối lượng của 6329Cu trong CuCl2 là giá trị nào dưới đây? Biết MCl = 35,5.
- A. 73,00%
- B. 27,00%
- C. 32,33%
- D. 34,18 %
-
Câu 13: Mã câu hỏi: 20402
Trong tự nhiên đồng vị 37Cl chiếm 24,23% số nguyên tử clo. Nguyên tử khối trung bình của clo bằng 35,485. Thành phần phần trăm về khối lượng của 37Cl có trong HClO4 là (với 1H, 16O)
- A. 9,82%
- B. 8,65%.
- C. 8,56%.
- D. 8,92%.
-
Câu 14: Mã câu hỏi: 20404
Trong nước tự nhiên, hiđro chủ yếu tồn tại 2 đồng vị 1H và 2H. Biết nguyên tử khối trung bình của hiđro trong nước nguyên chất bằng 1,008. Thành phần % về khối lượng của đồng vị 2H có trong 1,000 gam nước nguyên chất là (cho: O = 16)
- A. 0,178%
- B. 17,762%
- C. 0,089%
- D. 11,012%
-
Câu 15: Mã câu hỏi: 20405
Trong tự nhiên Si có ba đồng vị bền 2814Si chiếm 92,23%, 2914Si chiếm 4,67% còn lại là 3014Si.Phần trăm khối lượng của 2914Si trong Na2SiO3 là (Biết Na = 23 , O = 16):
- A. 2,2018%
- B. 1,1091%
- C. 1,8143%
- D. 2,1024%
-
Câu 16: Mã câu hỏi: 20406
Trong tự nhiên clo có hai đồng vị bền là 35Cl và 37Cl trong đó 35Cl chiếm 75,77% số nguyên tử. Phần trăm khối lượng 37Cl trong HClOn là 13,09%. Giá trị của n là
- A. 1.
- B. 2.
- C. 3.
- D. 4.
-
Câu 17: Mã câu hỏi: 20407
Nguyên tử khối trung bình của Bo bằng 10,81u. Biết Bo có 2 đồng vị 105B và 115B. Hỏi có bao nhiêu phần trăm số nguyên tử đồng vị 105B trong axít H3BO3 ?
- A. 3%
- B. 4%
- C. 5%
- D. 6%
-
Câu 18: Mã câu hỏi: 20408
Một nguyên tố R có 3 đồng vị X, Y ,Z; biết tổng số các hạt cơ bản (n, p, e) trong 3 đồng vị bằng 129, số nơtron đồng vị X hơn đồng vị Y một hạt. Đồng vị Z có số proton bằng số nơtron. Số khối của X, Y, Z lần lượt là
- A. 26, 27, 29
- B. 30, 29,28
- C. 28, 29, 30
- D. 27, 28, 26
-
Câu 19: Mã câu hỏi: 20410
Một lít khí hiđro giàu đơteri (12H) ở điều kiện tiêu chuẩn có khối lượng 0,10 gam. Cho rằng hiđro chỉ có hai đồng vị là 1H và 2H. Phần trăm khối lượng nguyên tử 1H trong loại khí hiđro trên là
- A. 12,00%
- B. 88,00%.
- C. 21,43%.
- D. 78,57%.
-
Câu 20: Mã câu hỏi: 20412
Nguyên tố O có 3 đồng vị 16O, 17O, 18O. Biết 752,875. 1020 nguyên tử oxi có khối lượng m gam. Tỷ lệ giữa các đồng vị lần lượt là 16O : 17O = 4504 : 301, 18 O : 17O = 585 : 903 . Tính giá trị của m
- A. 2,0175
- B. 2,0173
- C. 2, 0875
- D. 2,0189
-
Câu 21: Mã câu hỏi: 20416
Trong tự nhiên sắt gồm 4 đồng vị 54Fe chiếm 5,8%, 56Fe chiếm 91,72%, 57Fe chiếm 2,2% và 58Fe chiếm 0,28%. Brom là hỗn hợp hai đồng vị 79Br chiếm 50,69% và 81Br chiếm 49,31%. Thành phần % khối lượng của 56Fe trong FeBr3 là
- A. 17,36%.
- B. 18,92%.
- C. 27,03%.
- D. 27,55%.
-
Câu 22: Mã câu hỏi: 20419
Trong tự nhiên clo có hai đồng vị bền: 37Cl chiếm 24,23% tổng số nguyên tử, còn lại là 35Cl (Cl có số hiệu nguyên tử là 17). Thành phần % theo khối lượng của 37Cl trong HClO4 là (Cho: H = 1, O = 16):
- A. 8,92%
- B. 8,43%
- C. 8,56%
- D. 8,79%
-
Câu 23: Mã câu hỏi: 20421
Bo có 2 đồng vị là 10B và 11B với nguyên tử khối trung bình là 10,81. Thành phần % về khối lượng của đồng vị 11B chứa trong H3BO3 là (Cho: H = 1, O = 16)
- A. 14,00%.
- B. 14,16%.
- C. 14,42%.
- D. 15,00%.
-
Câu 24: Mã câu hỏi: 20422
Trong tự nhiên nguyên tố Bo có hai đồng vị bền là 11B và 10B. Biết nguyên tử khối trung bình của Bo là 10,81. Trung bình cứ có 1539 nguyên tử 10B thì sẽ có tương ứng bao nhiêu nguyên tử 11B ?
- A. 292
- B. 361
- C. 1247
- D. 6561
-
Câu 25: Mã câu hỏi: 20424
Trong tự nhiên Mg có 3 đồng vị bền: 24Mg (79,00%); 25Mg (10,00%) và 26Mg (11,00%). Giả sử có 158 nguyên tử đồng vị 24Mg thì tổng số nguyên tử của hai đồng vị còn lại là
- A. 20.
- B. 21.
- C. 22.
- D. 42.
-
Câu 26: Mã câu hỏi: 20425
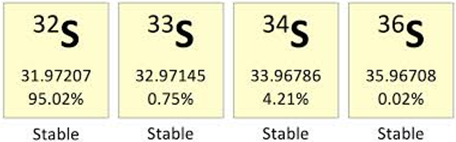
Trong tự nhiên lưu huỳnh gồm 4 đồng vị bền:
Thành phần % về khối lượng của đồng vị 32S trong H2SO4 có giá trị gần nhất với (H = 1; O = 16)
- A. 31,10%
- B. 31,05%
- C. 31,00%
- D. 30,95%
-
Câu 27: Mã câu hỏi: 20427
Số phân tử dạng A2B được tạo thành từ n đồng vị của A và m đồng vị của B là:
- A. \(\frac{{m.n(n + 1)}}{2}\)
- B. m.n(n + 1).
- C.
m.n2.
- D. m2.n.
-
Câu 28: Mã câu hỏi: 20428
Trong tự nhiên oxi có 3 đồng vị là 16O, 17O, 18O ; nitơ có 2 đồng vị là 14N, 15N còn H có 3 đồng vị bền là 1H, 2H, 3H. Khẳng định nào sau đây là không đúng
- A. có 12 phân tử dạng NO2.
- B. Có 12 phân tử dạng N2O.
- C. có 60 phân tử dạng HNO3.
- D. có 18 phân tử dạng H2O.
-
Câu 29: Mã câu hỏi: 20429
Trong tự nhiên clo có 2 đồng vị là 35Cl và 37Cl. Nguyên tử khối trung bình của clo là 35,5. Thành phần % khối lượng của 37Cl trong KClO3 là (Cho: K = 39, O = 16)
- A. 7,24%.
- B. 7,55%.
- C. 25,00%.
- D. 28,98%.
-
Câu 30: Mã câu hỏi: 20430
Nguyên tố N có 2 đồng vị là 14N và 15N ; H có 3 đồng vị là 1H, 2H và 3H. Số phân tử NH3 tối đa có thể có là (biết 3 nguyên tử H trong NH3 là tương đương về mặt cấu tạo)
- A. 6.
- B. 12.
- C. 18.
- D. 20.

Đề thi nổi bật tuần
ADSENSE TRACNGHIEM Bộ đề thi nổi bật
Bộ đề thi nổi bật  UREKA AANETWORK
UREKA AANETWORK 
XEM NHANH CHƯƠNG TRÌNH LỚP 10
Toán 10
Toán 10 Kết Nối Tri Thức
Toán 10 Chân Trời Sáng Tạo
Toán 10 Cánh Diều
Giải bài tập Toán 10 Kết Nối Tri Thức
Giải bài tập Toán 10 CTST
Giải bài tập Toán 10 Cánh Diều
Trắc nghiệm Toán 10
Ngữ văn 10
Ngữ Văn 10 Kết Nối Tri Thức
Ngữ Văn 10 Chân Trời Sáng Tạo
Ngữ Văn 10 Cánh Diều
Soạn Văn 10 Kết Nối Tri Thức
Soạn Văn 10 Chân Trời Sáng tạo
Soạn Văn 10 Cánh Diều
Văn mẫu 10
Tiếng Anh 10
Giải Tiếng Anh 10 Kết Nối Tri Thức
Giải Tiếng Anh 10 CTST
Giải Tiếng Anh 10 Cánh Diều
Trắc nghiệm Tiếng Anh 10 KNTT
Trắc nghiệm Tiếng Anh 10 CTST
Trắc nghiệm Tiếng Anh 10 CD
Giải Sách bài tập Tiếng Anh 10
Vật lý 10
Vật lý 10 Kết Nối Tri Thức
Vật lý 10 Chân Trời Sáng Tạo
Vật lý 10 Cánh Diều
Giải bài tập Lý 10 Kết Nối Tri Thức
Giải bài tập Lý 10 CTST
Giải bài tập Lý 10 Cánh Diều
Trắc nghiệm Vật Lý 10
Hoá học 10
Hóa học 10 Kết Nối Tri Thức
Hóa học 10 Chân Trời Sáng Tạo
Hóa học 10 Cánh Diều
Giải bài tập Hóa 10 Kết Nối Tri Thức
Giải bài tập Hóa 10 CTST
Giải bài tập Hóa 10 Cánh Diều
Trắc nghiệm Hóa 10
Sinh học 10
Sinh học 10 Kết Nối Tri Thức
Sinh học 10 Chân Trời Sáng Tạo
Sinh học 10 Cánh Diều
Giải bài tập Sinh 10 Kết Nối Tri Thức
Giải bài tập Sinh 10 CTST
Giải bài tập Sinh 10 Cánh Diều
Trắc nghiệm Sinh học 10
Lịch sử 10
Lịch Sử 10 Kết Nối Tri Thức
Lịch Sử 10 Chân Trời Sáng Tạo
Lịch Sử 10 Cánh Diều
Giải bài tập Lịch Sử 10 KNTT
Giải bài tập Lịch Sử 10 CTST
Giải bài tập Lịch Sử 10 Cánh Diều
Trắc nghiệm Lịch sử 10
Địa lý 10
Địa Lý 10 Kết Nối Tri Thức
Địa Lý 10 Chân Trời Sáng Tạo
Địa Lý 10 Cánh Diều
Giải bài tập Địa Lý 10 KNTT
Giải bài tập Địa Lý 10 CTST
Giải bài tập Địa Lý 10 Cánh Diều
Trắc nghiệm Địa lý 10
GDKT & PL 10
GDKT & PL 10 Kết Nối Tri Thức
GDKT & PL 10 Chân Trời Sáng Tạo
GDKT & PL 10 Cánh Diều
Giải bài tập GDKT & PL 10 KNTT
Giải bài tập GDKT & PL 10 CTST
Giải bài tập GDKT & PL 10 CD
Trắc nghiệm GDKT & PL 10
Công nghệ 10
Công nghệ 10 Kết Nối Tri Thức
Công nghệ 10 Chân Trời Sáng Tạo
Công nghệ 10 Cánh Diều
Giải bài tập Công nghệ 10 KNTT
Giải bài tập Công nghệ 10 CTST
Giải bài tập Công nghệ 10 CD
Trắc nghiệm Công nghệ 10
Tin học 10
Tin học 10 Kết Nối Tri Thức
Tin học 10 Chân Trời Sáng Tạo
Tin học 10 Cánh Diều
Giải bài tập Tin học 10 KNTT
Giải bài tập Tin học 10 CTST
Giải bài tập Tin học 10 Cánh Diều
Trắc nghiệm Tin học 10
Cộng đồng
Hỏi đáp lớp 10
Tư liệu lớp 10
Xem nhiều nhất tuần
Đề thi giữa HK2 lớp 10
Đề thi giữa HK1 lớp 10
Đề thi HK1 lớp 10
Đề thi HK2 lớp 10
Đề cương HK1 lớp 10
Video bồi dưỡng HSG môn Toán
Toán 10 Chân trời sáng tạo Bài 2: Tập hợp
Toán 10 Kết nối tri thức Bài 1: Mệnh đề
Toán 10 Cánh Diều Bài tập cuối chương 1
Soạn bài Chữ người tử tù - Nguyễn Tuân - Ngữ văn 10 KNTT
Soạn bài Thần Trụ Trời - Ngữ văn 10 CTST
Soạn bài Ra-ma buộc tội - Ngữ văn 10 Tập 1 Cánh Diều
Văn mẫu về Bình Ngô đại cáo
Văn mẫu về Chữ người tử tù
Văn mẫu về Tây Tiến
Văn mẫu về Cảm xúc mùa thu (Thu hứng)
YOMEDIA ×Thông báo
Bạn vui lòng đăng nhập trước khi sử dụng chức năng này.
Bỏ qua Đăng nhập ×Thông báo
Bạn vui lòng đăng nhập trước khi sử dụng chức năng này.
Đồng ý ATNETWORK ON QC Bỏ qua >>
QC Bỏ qua >> 
Từ khóa » Bài Tập Về đồng Vị Lớp 10 Nâng Cao
-
50 Bài Tập Về Đồng Vị Nâng Cao Siêu Hay Có Lời Giải - CungHocVui
-
Bài Tập Hóa Học 10: Đồng Vị (Có đáp án)
-
Bài Tập Về Đồng Vị Nâng Cao Siêu Hay Có Lời Giải (P1)
-
Các Dạng Bài Tập Về Đồng Vị Lớp 10
-
Các Dạng Bài Tập Về Đồng Vị Lớp 10 - ThiênBảo Edu
-
30 Câu Kèm Lời Giải Đồng Vị (đề NÂNG CAO) - 123doc
-
20 Bài Tập Vận Dụng Về đồng Vị, Nguyên Tử Khối Trung Bình Có Lời Giải
-
Giải Bài Tập SGK Hóa Học 10 Nâng Cao Bài 3: Đồng Vị. Nguyên Tử ...
-
Hóa 10 Bài 3: Đồng Vị. Nguyên Tử Khối Và Nguyên Tử Khối Trung Bình
-
Giải Bài Tập Hóa 10 Nâng Cao Sách Giáo Khoa Chương Nguyên Tử
-
Bài Tập Hóa Học Lớp 10 Nâng Cao - Chương I, II - TaiLieu.VN
-
Bài 3: Đồng Vị. Nguyên Tử Khối Và Nguyên Tử Khối Trung Bình
-
35 Bài Tập Nâng Cao Hóa 10 - Học Để Thi