Độ PH Của đất – Wikipedia Tiếng Việt
Có thể bạn quan tâm
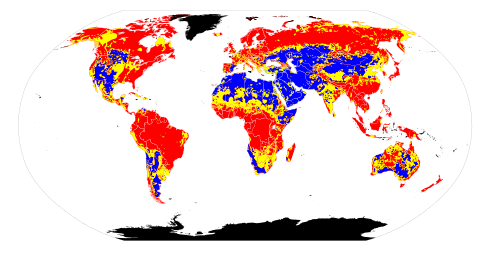
Độ pH của đất là thước đo độ axit hoặc tính base (độ kiềm) của đất. pH được định nghĩa là logarit âm (cơ sở 10) hoạt động của các ion hydronium (H+ <br /> hay chính xác hơn là H3O+aq <br /> H3O+aq <br /> H3O+aq) trong một dung dịch. Trong đất, nó được đo trong bùn đất trộn với nước (hoặc dung dịch muối, chẳng hạn như 0,01 M CaCl2 <br /> CaCl2) và thường rơi vào khoảng từ 3 đến 10, với 7 là trung tính. Đất chua có độ pH dưới 7 và đất kiềm có độ pH trên 7. Đất siêu axit (pH <3,5) và đất kiềm rất mạnh (pH> 9) là rất hiếm.[1][2]
Độ pH của đất được coi là một biến số chính trong đất vì nó ảnh hưởng đến nhiều quá trình hóa học. Nó đặc biệt ảnh hưởng đến lượng dinh dưỡng thực vật bằng cách kiểm soát các dạng hóa học của các chất dinh dưỡng khác nhau và ảnh hưởng đến các phản ứng hóa học mà chúng trải qua. Phạm vi pH tối ưu cho hầu hết các cây trồng là từ 5,5 đến 7,5;[2] tuy nhiên, nhiều loại cây trồng đã thích nghi để phát triển mạnh ở độ pH nằm ngoài phạm vi này.
Phân loại phạm vi pH đất
[sửa | sửa mã nguồn]Bộ Nông nghiệp Hoa Kỳ - Dịch vụ bảo tồn tài nguyên thiên nhiên đã phân loại phạm vi pH đất như sau:
| Tên | Phạm vi pH |
|---|---|
| Có tính axit cực cao | <3,5 |
| Có tính axit cực cao | 3,5–4,4 |
| Có tính axit rất mạnh | 4,5–5,0 |
| Có tính axit mạnh | 5,1–5,5 |
| Có tính axit vừa phải | 5,6–6,0 |
| Có tính axit nhẹ | 6,1–6,5 |
| Trung tính | 6,6–7,3 |
| Hơi kiềm | 7,4–7,8 |
| Có tính kiềm vừa phải | 7,9–8,4 |
| Có tính kiềm mạnh | 8,5–9,0 |
| Có tính kiềm rất mạnh | > 9.0 |
Xác định pH
[sửa | sửa mã nguồn]Các phương pháp xác định pH[3] bao gồm:
- Quan sát hồ sơ đất: Một số đặc điểm hồ sơ nhất định có thể là các chỉ số về điều kiện axit, mặn hoặc nước ngọt. Ví dụ là:[4]
- Sự kết hợp kém của lớp bề mặt hữu cơ với lớp khoáng bên dưới - điều này có thể chỉ ra các loại đất có tính axit mạnh;
- Trình tự chân trời podzol cổ điển, vì podzol có tính axit mạnh: trong các loại đất này, một chân trời eluvial (E) nhợt nhạt nằm dưới lớp bề mặt hữu cơ và phủ lên một chân trời B tối;
- Sự hiện diện của một lớp caliche cho thấy sự hiện diện của calci cacbonat, có trong điều kiện kiềm;
- Cấu trúc cột có thể là một chỉ số của điều kiện sodic.
- Quan sát hệ thực vật chiếm ưu thế. Các loài thực vật calcifuge (những loài thích đất chua) bao gồm Erica, Rhododendron và gần như tất cả các loài Ericaceae khác, nhiều loài bạch dương (Betula), foxglove (Digitalis), gorse (Ulex spp.) Và Scots Pine (Pinus sylvestris). Cây calcicole (vôi yêu) bao gồm cây tro (Fraxinus spp.), Cây kim ngân (Lonicera), Buddleja, dogwoods (Cornus spp.), Lilac (Syringa) và loài Clematis.
- Sử dụng bộ dụng cụ kiểm tra pH rẻ tiền, trong đó trong một mẫu đất nhỏ được trộn với dung dịch chỉ thị làm thay đổi màu theo độ axit.
- Sử dụng giấy quỳ. Một mẫu đất nhỏ được trộn với nước cất, trong đó một dải giấy quỳ được chèn vào. Nếu đất có tính axit, giấy sẽ chuyển sang màu đỏ, nếu cơ bản, màu xanh.[5]
- Sử dụng máy đo pH điện tử có bán trên thị trường, trong đó điện cực ở trạng thái rắn hoặc thủy tinh được đưa vào đất ẩm hoặc hỗn hợp (huyền phù) đất và nước; độ pH thường được đọc trên màn hình hiển thị kỹ thuật số.
- Gần đây, các phương pháp đo quang phổ đã được phát triển để đo pH đất liên quan đến việc bổ sung thuốc nhuộm chỉ thị vào chiết xuất đất.[6] Chúng so sánh tốt với các phép đo điện cực thủy tinh nhưng cung cấp các lợi thế đáng kể như thiếu trôi, mối nối lỏng và hiệu ứng treo.
Các lần đo chính xác, lặp lại của pH đất là cần thiết cho nghiên cứu khoa học và giám sát. Điều này thường đòi hỏi phân tích phòng thí nghiệm bằng cách sử dụng một giao thức chuẩn; một ví dụ về giao thức như vậy là trong Hướng dẫn phương pháp thí nghiệm đất và phòng thí nghiệm của USDA.[7] Trong tài liệu này, giao thức ba trang để đo pH đất bao gồm các phần sau: Ứng dụng; Tóm tắt phương pháp; Các cuộc họp; An toàn; Trang thiết bị; Thuốc thử; và Thủ tục:
Tóm tắt phương pháp; Sự giao thoa; Sự an toàn; Trang thiết bị; Thuốc thử; và Thủ tục.
Tóm tắt phương phápĐộ pH được đo trong dung dịch đất-nước (1: 1) và đất-muối (1: 2 ). Để thuận tiện, ban đầu đo pH trong nước và sau đó đo trong . Với việc bổ sung một thể tích bằng nhau của 0,02 M vào huyền phù đất đã được chuẩn bị cho pH của nước, tỷ lệ đất-dung dịch cuối cùng là 1: 2 0,01 M . 20 g mẫu đất được trộn với 20 mL nước thẩm thấu ngược (RO) (1: 1 w: v) và thỉnh thoảng khuấy. Để yên mẫu trong 1 h và thỉnh thoảng khuấy. Mẫu được khuấy trong 30 s, và đo pH nước 1: 1. Thêm 0,02 M (20 mL) vào huyền phù đất, khuấy mẫu và đo pH 1: 2 0,01 M (4C1a2a2).
— Tóm tắt về phương pháp USDA NRCS để xác định độ pH của đất [7]
Các yếu tố ảnh hưởng đến pH đất
[sửa | sửa mã nguồn]Độ pH của đất tự nhiên phụ thuộc vào thành phần khoáng chất của vật liệu gốc của đất và các phản ứng phong hóa trải qua vật liệu gốc đó. Trong môi trường ấm áp, ẩm ướt, quá trình axit hóa đất xảy ra theo thời gian do các sản phẩm của thời tiết bị rò rỉ bởi nước di chuyển ngang hoặc xuống dưới đất. Tuy nhiên, ở vùng khí hậu khô, thời tiết đất và nước rỉ rác ít dữ dội hơn và độ pH của đất thường trung tính hoặc kiềm.[8][9]
Nguồn axit
[sửa | sửa mã nguồn]Nhiều quá trình góp phần axit hóa đất. Chúng bao gồm:[10][11]
- Lượng mưa: Đất axit thường được tìm thấy ở những nơi có lượng mưa cao. Nước mưa có độ pH hơi axit (thường khoảng 5,7) do phản ứng với CO2 <br /> CO2 trong khí quyển tạo thành axit cacbonic. Khi nước này chảy qua đất, nó dẫn đến sự rò rỉ các cation cơ bản từ đất dưới dạng bicacbonat; điều này làm tăng tỷ lệ phần trăm của Al3+ <br /> và H+ <br /> liên quan đến các cation khác.
- Hô hấp rễ và phân hủy chất hữu cơ do vi sinh vật giải phóng CO2 <br /> CO2 làm tăng axit cacbonic (H2CO3 <br /> H2CO3 <br /> H2CO3) tập trung và lọc nước tiếp theo.
- Sinh trưởng của cây: Cây chiếm chất dinh dưỡng dưới dạng các ion (ví dụ NO−3 <br /> NO−3, NH+4 <br /> NH+4, Ca2+ <br />, H2PO−4 <br /> H2PO−4 <br /> H2PO−4), và chúng thường chiếm nhiều cation hơn anion. Tuy nhiên, thực vật phải duy trì một điện tích trung tính trong rễ của chúng. Để bù cho khoản phí tích cực thêm, họ sẽ giải phóng H+ <br /> các ion từ gốc. Một số thực vật cũng thải axit hữu cơ vào đất để axit hóa vùng xung quanh rễ của chúng để giúp hòa tan các chất dinh dưỡng kim loại không hòa tan ở pH trung tính, chẳng hạn như sắt (Fe).
- Sử dụng phân bón: Amoni (NH+4 <br /> NH+4) phân bón phản ứng trong đất bằng quá trình nitrat hóa để tạo thành nitrat (NO−3 <br /> NO−3) và trong quá trình phát hành H+ <br /> các ion.
- Mưa axit: Việc đốt nhiên liệu hóa thạch giải phóng oxit lưu huỳnh và nitơ vào khí quyển. Chúng phản ứng với nước trong khí quyển để tạo thành axit sunfuric và axit nitric trong mưa.
- Phong hóa oxy hóa: Oxy hóa một số khoáng chất chính, đặc biệt là sulfide và những chất có chứa Fe2+ <br />, tạo ra tính axit. Quá trình này thường được tăng tốc bởi hoạt động của con người:
- Chất thải mỏ: Điều kiện axit nghiêm trọng có thể hình thành trong đất gần một số chiến lợi phẩm của mỏ do quá trình oxy hóa pyrite.
- Đất phèn hình thành tự nhiên trong môi trường ven biển ngập nước và cửa sông có thể có tính axit cao khi thoát nước hoặc đào.
Nguồn kiềm
[sửa | sửa mã nguồn]Tổng độ kiềm của đất tăng khi:[12][13]
- Phong hóa khoáng silicat, aluminosilicate và cacbonat chứa Na+ <br />, Ca2+ <br />, Mg2+ <br /> và K+ <br />;
- Bổ sung khoáng silicat, aluminosilicate và cacbonat vào đất; điều này có thể xảy ra bằng cách lắng đọng vật liệu bị xói mòn ở nơi khác bởi gió hoặc nước, hoặc bằng cách trộn đất với vật liệu ít bị phong hóa (như bổ sung đá vôi vào đất axit);
- Bổ sung nước có chứa bicacbonat hòa tan (như xảy ra khi tưới với nước có hàm lượng bicarbonate cao).
Sự tích tụ độ kiềm trong đất (như cacbonat và bicacbonat của Na, K, Ca và Mg) xảy ra khi không đủ nước chảy qua đất để lọc muối hòa tan. Điều này có thể là do điều kiện khô cằn hoặc thoát nước bên trong kém; trong những tình huống này, phần lớn nước xâm nhập vào đất bị thoát ra (được thực vật hấp thụ) hoặc bốc hơi thay vì chảy qua đất.[12]
Độ pH của đất thường tăng khi tổng độ kiềm tăng, nhưng sự cân bằng của các cation được thêm vào cũng có ảnh hưởng rõ rệt đến độ pH của đất. Ví dụ, tăng lượng natri trong đất kiềm có xu hướng gây ra sự hòa tan calci cacbonat, làm tăng độ pH. Các loại đất chăm sóc có thể thay đổi độ pH từ 7,0 đến 9,5, tùy thuộc vào mức độ Ca2+ <br /> hoặc Na+ <br /> thống trị các cation hòa tan.[12]
Ảnh hưởng của pH đất đến sinh trưởng của cây
[sửa | sửa mã nguồn]Đất phèn
[sửa | sửa mã nguồn]Cây trồng trong đất axit có thể gặp nhiều loại stress bao gồm nhôm (Al), hydro (H) và/hoặc mangan (Mn) độc tính, cũng như sự thiếu hụt chất dinh dưỡng của calci (Ca) và magiê (Mg).[14]
Độc tính nhôm là vấn đề phổ biến nhất trong đất axit. Nhôm có mặt trong tất cả các loại đất, nhưng Al 3+ hòa tan gây độc cho cây; Al 3+ dễ hòa tan nhất ở pH thấp; trên pH 5.0, có ít Al ở dạng hòa tan trong hầu hết các loại đất.[15][16] Nhôm không phải là một chất dinh dưỡng thực vật, và như vậy, không được thực vật hấp thụ mà xâm nhập vào rễ cây một cách thụ động thông qua thẩm thấu. Nhôm ức chế sự phát triển của rễ; rễ bên và đầu rễ trở nên dày và rễ thiếu phân nhánh tốt; lời khuyên gốc có thể chuyển sang màu nâu. Trong gốc, tác dụng ban đầu của Al 3+ là ức chế sự mở rộng của các tế bào của rhizodermis, dẫn đến vỡ của chúng; Sau đó, nó được biết là can thiệp vào nhiều quá trình sinh lý bao gồm sự hấp thu và vận chuyển calci và các chất dinh dưỡng cần thiết khác, phân chia tế bào, hình thành tế bào và hoạt động của enzyme.[15][17]
Căng thẳng proton (ion H +) cũng có thể hạn chế sự phát triển của thực vật. Bơm proton, H + -ATPase, của plasmalemma của tế bào gốc hoạt động để duy trì độ pH gần như trung tính của tế bào chất của chúng. Một hoạt động proton cao (pH trong phạm vi 3.0-4.0 đối với hầu hết các loài thực vật) trong môi trường tăng trưởng bên ngoài vượt qua khả năng của tế bào để duy trì pH tế bào chất và sự tăng trưởng ngừng lại.[18]
Trong đất có hàm lượng khoáng chất chứa mangan cao, độc tính Mn có thể trở thành vấn đề ở pH 5,6 và thấp hơn. Mangan, giống như nhôm, ngày càng hòa tan khi pH giảm và các triệu chứng nhiễm độc Mn có thể được nhìn thấy ở mức độ pH dưới 5,6. Mangan là một chất dinh dưỡng thực vật thiết yếu, vì vậy thực vật vận chuyển Mn vào lá. Triệu chứng kinh điển của độc tính Mn là nhăn nheo hoặc uốn lá.
Lượng dinh dưỡng sẵn có liên quan đến pH đất
[sửa | sửa mã nguồn]
PH đất ảnh hưởng đến sự sẵn có của một số chất dinh dưỡng thực vật:
Như đã thảo luận ở trên, độc tính nhôm có ảnh hưởng trực tiếp đến sự tăng trưởng của thực vật; tuy nhiên, bằng cách hạn chế sự phát triển của rễ, nó cũng làm giảm sự sẵn có của các chất dinh dưỡng thực vật. Do rễ bị hư hại, sự hấp thu chất dinh dưỡng bị giảm và sự thiếu hụt các chất dinh dưỡng đa lượng (nitơ, phosphor, kali, calci và magnesi) thường gặp trong đất có tính axit rất mạnh đối với đất siêu axit (pH <5,0).[20]
Molypden có sẵn được tăng ở pH cao hơn; điều này là do ion molybdate bị hấp thụ mạnh hơn bởi các hạt đất sét ở pH thấp hơn.[21]
Kẽm, sắt, đồng và mangan cho thấy giảm khả dụng ở pH cao hơn (tăng độ hấp thụ ở pH cao hơn).[21]
Ảnh hưởng của pH đến lượng phosphor thay đổi đáng kể, tùy thuộc vào điều kiện đất đai và vụ mùa. Quan điểm phổ biến trong những năm 1940 và 1950 là tính khả dụng của P được tối đa hóa gần mức trung tính (pH đất 6,5.57,5), và giảm ở pH cao hơn và thấp hơn.[22][23] Tuy nhiên, tương tác của phosphor với pH trong phạm vi vừa phải đến hơi axit (pH 5,5 xăng6,5), tuy nhiên, phức tạp hơn nhiều so với đề xuất của quan điểm này. Các thử nghiệm trong phòng thí nghiệm, thử nghiệm nhà kính và thử nghiệm thực địa đã chỉ ra rằng việc tăng pH trong phạm vi này có thể tăng, giảm hoặc không ảnh hưởng đến tính khả dụng của P đối với cây trồng.[23][24]
Nguồn nước liên quan đến pH đất
[sửa | sửa mã nguồn]Các loại đất có tính kiềm mạnh là sodic và phân tán, với độ thấm chậm, độ dẫn thủy lực thấp và khả năng chứa nước kém.[25] Tăng trưởng thực vật bị hạn chế nghiêm trọng vì sục khí kém khi đất ẩm ướt; trong điều kiện khô ráo, nước có sẵn từ thực vật bị cạn kiệt nhanh chóng và đất trở nên cứng và vón cục (độ bền của đất cao).[26]
Mặt khác, nhiều loại đất có tính axit mạnh, có sự kết tụ mạnh mẽ, thoát nước bên trong tốt và đặc tính giữ nước tốt. Tuy nhiên, đối với nhiều loài thực vật, độc tính nhôm hạn chế nghiêm trọng sự phát triển của rễ và căng thẳng độ ẩm có thể xảy ra ngay cả khi đất tương đối ẩm.[15]
Lựa chọn pH thực vật
[sửa | sửa mã nguồn]Nói chung, các loài thực vật khác nhau thích nghi với các loại đất có độ pH khác nhau. Đối với nhiều loài, phạm vi pH đất thích hợp là khá đặc thù. Cơ sở dữ liệu trực tuyến về các đặc điểm của thực vật, như CÂY USDA [27] và Cây cho tương lai [28] có thể được sử dụng để tìm kiếm phạm vi pH đất thích hợp của nhiều loại cây. Các tài liệu như giá trị chỉ thị của Ellenberg cho các cây trồng của Anh[29] cũng có thể được tham khảo.
(Tuy nhiên, một loại cây có thể không dung nạp được độ pH cụ thể trong một số loại đất do một cơ chế cụ thể và cơ chế đó có thể không được áp dụng trong các loại đất khác. Ví dụ, đất có hàm lượng molypden thấp có thể không phù hợp với cây đậu tương ở pH 5,5, nhưng đất có đủ molypden cho phép tăng trưởng tối ưu ở độ pH đó.[20] Tương tự, một số calcifuges (thực vật không dung nạp đất có độ pH cao) có thể chịu được đất đá vôi nếu cung cấp đủ phosphor.[30] Một yếu tố gây nhiễu khác là các giống khác nhau của cùng một loài thường có phạm vi pH đất thích hợp khác nhau. Các nhà nhân giống thực vật có thể sử dụng điều này để nhân giống các giống có thể chịu được các điều kiện được coi là không phù hợp với loài đó - ví dụ là các dự án nhân giống các loại cây ngũ cốc chịu được nhôm và mangan để sản xuất thức ăn trong đất chua mạnh.[31]
Bảng dưới đây cung cấp phạm vi pH đất thích hợp cho một số cây được trồng rộng rãi như được tìm thấy trong Cơ sở dữ liệu của USDA PLANTS.[27] Một số loài (như Pinus radiata và Opuntia ficus-indica) chỉ chịu được một phạm vi hẹp trong pH đất, trong khi những loài khác (như Vetiveria zizanioides) chịu được phạm vi pH rất rộng.
| Tên khoa học | Tên gọi chung | pH (tối thiểu) | pH (tối đa) |
|---|---|---|---|
| Cỏ Vetiveria zizanioides | cỏ vetivergrass | 3.0 | 8,0 |
| Pinus Rigida | Sân bóng | 3,5 | 5.1 |
| Rubus chamaemorus | cây mâm xôi | 4.0 | 5,2 |
| Anana hôn mê | Trái dứa | 4.0 | 6.0 |
| Cà phê Ả Rập | Cà phê Ả Rập | 4.0 | 7,5 |
| Đỗ quyên arborescens | đỗ quyên mịn | 4.2 | 5,7 |
| Pinus radiata | Cây thông | 4,5 | 5,2 |
| Carya illinoinensis | hồ đào | 4,5 | 7,5 |
| Tam Thất | quả me | 4,5 | 8,0 |
| Vaccinium corymbosum | quả việt quất | 4,7 | 7,5 |
| Manihot esculenta | sắn | 5.0 | 5,5 |
| Morus alba | dâu trắng | 5.0 | 7,0 |
| Malus | táo | 5.0 | 7,5 |
| Pinus sylvestris | Scots thông | 5.0 | 7,5 |
| Đu đủ | đu đủ | 5.0 | 8,0 |
| Cajanus cajan | bồ câu | 5.0 | 8.3 |
| Cộng đồng Pyrus | lê thông thường | 5,2 | 6,7 |
| Solanum lycopersicum | vườn cà chua | 5,5 | 7,0 |
| Psidium guajava | trái ổi | 5,5 | 7,0 |
| Cây trúc đào | cây trúc đào | 5,5 | 7,8 |
| Granica granatum | trái thạch lựu | 6.0 | 6,9 |
| Viola | màu xanh tím phổ biến | 6.0 | 7,8 |
| Caragana arborescens | Đậu Hà Lan | 6.0 | 9.0 |
| Cotoneaster integerrimus | cotoneaster | 6,8 | 8,7 |
| Opuntia ficus-indica | Barbary fig (pricklypear) | 7,0 | 8,5 |
Thay đổi độ pH của đất
[sửa | sửa mã nguồn]Tăng độ pH của đất chua
[sửa | sửa mã nguồn]Vôi nông nghiệp nghiền mịn thường được áp dụng cho đất chua để tăng độ pH của đất (bón vôi). Lượng đá vôi hoặc phấn cần thiết để thay đổi pH được xác định bởi kích thước mắt lưới của vôi (độ mịn của mặt đất) và khả năng đệm của đất. Kích thước mắt lưới cao (60 lưới = 0,25 mm; 100 lưới = 0,149 mm) chỉ ra một loại vôi nghiền mịn sẽ phản ứng nhanh với độ chua của đất. Khả năng đệm của đất phụ thuộc vào hàm lượng sét trong đất, loại đất sét và lượng chất hữu cơ có mặt, và có thể liên quan đến khả năng trao đổi cation của đất. Đất có hàm lượng sét cao sẽ có khả năng đệm cao hơn đất có ít đất sét và đất có chất hữu cơ cao sẽ có khả năng đệm cao hơn so với đất có chất hữu cơ thấp. Các loại đất có khả năng đệm cao hơn đòi hỏi một lượng vôi lớn hơn để đạt được sự thay đổi tương đương về độ pH.[32]
Những sửa đổi khác ngoài vôi nông nghiệp có thể được sử dụng để tăng độ pH của đất bao gồm tro gỗ, oxit calci công nghiệp (vôi cháy), oxit magiê, xỉ cơ bản (calci silicat) và vỏ hàu. Những sản phẩm này làm tăng độ pH của đất thông qua các phản ứng axit-base khác nhau. Calci silicat trung hòa độ axit hoạt động trong đất bằng cách phản ứng với H + các ion tạo thành axit monosilicic (H 4 SiO 4), một chất tan trung tính.[33]
Giảm độ pH của đất kiềm
[sửa | sửa mã nguồn]Độ pH của đất kiềm có thể được giảm bằng cách thêm các tác nhân axit hóa hoặc vật liệu hữu cơ có tính axit. Lưu huỳnh nguyên tố (90 Tắt99% S) đã được sử dụng với tỷ lệ ứng dụng là 300 FPV500 kg / ha - nó từ từ oxy hóa trong đất để tạo thành axit sulfuric. Phân bón axit hóa, chẳng hạn như ammonium sulfate, ammonium nitrate và urê, có thể giúp giảm độ pH của đất vì amoni oxy hóa để tạo thành axit nitric. Vật liệu hữu cơ axit hóa bao gồm than bùn hoặc rêu than bùn.[34]
Tuy nhiên, trong đất có độ pH cao có hàm lượng calci cacbonat cao (hơn 2%), sẽ rất tốn kém và/hoặc không hiệu quả khi cố gắng giảm độ pH bằng axit. Trong những trường hợp như vậy, thường sẽ hiệu quả hơn khi thêm phosphor, sắt, mangan, đồng và/hoặc kẽm, vì sự thiếu hụt các chất dinh dưỡng này là lý do phổ biến nhất cho sự phát triển của cây trồng kém trong đất đá vôi.[35][36]
Tham khảo
[sửa | sửa mã nguồn]- ^ Slessarev, E. W.; Lin, Y.; Bingham, N. L.; Johnson, J. E.; Dai, Y.; Schimel, J. P.; Chadwick, O. A. (ngày 21 tháng 11 năm 2016). "Water balance creates a threshold in soil pH at the global scale". Nature. Quyển 540 số 7634. tr. 567–569. doi:10.1038/nature20139.
- ^ a b Queensland Department of Environment and Heritage Protection. "Soil pH". www.qld.gov.au (bằng tiếng Anh). Truy cập ngày 15 tháng 5 năm 2017.
- ^ "Solutions to Soil Problems: High pH – eXtension" (bằng tiếng Anh). Truy cập ngày 26 tháng 2 năm 2017.
- ^ Buol, SW, RJ Southard, RC Graham và PA McDaniel.
- ^ Thomas, G. W. (1996), "Soil pH measurement and Changing soil pH", Methods of Soil Analysis, SSSA Book Series (bằng tiếng Anh), John Wiley & Sons, Ltd, tr. 475–490, doi:10.2136/sssabookser5.3.c16, ISBN 978-0-89118-866-7, S2CID 93493509, truy cập ngày 15 tháng 2 năm 2021
- ^ Bargrizan S, Smernik R, Mosley LM (2017).
- ^ a b Soil Survey Staff (2014). R. Burt and Soil Survey Staff (biên tập). Kellogg Soil Survey Laboratory Methods Manual. Soil Survey Investigations Report No. 42, Version 5.0 (PDF). U.S. Department of Agriculture, Natural Resources Conservation Service. tr. 276–279. Bản gốc (PDF) lưu trữ ngày 6 tháng 5 năm 2017. Truy cập ngày 26 tháng 6 năm 2017.
- ^ USDA-NRCS. "Soil pH" (PDF). Guides for Educators: Soil Quality Kit. www.nrcs.usda.gov. Bản gốc (PDF) lưu trữ ngày 1 tháng 5 năm 2017. Truy cập ngày 15 tháng 5 năm 2017.
- ^ van Breemen, N.; Mulder, J.; Driscoll, C. T. (tháng 10 năm 1983). "Acidification and alkalinization of soils". Plant and Soil. Quyển 75 số 3. tr. 283–308. doi:10.1007/BF02369968.
- ^ Van Breemen, N.; Driscoll, C. T.; Mulder, J. (ngày 16 tháng 2 năm 1984). "Acidic deposition and internal proton sources in acidification of soils and waters". Nature. Quyển 307 số 5952. tr. 599–604. doi:10.1038/307599a0.
- ^ Tia lửa, Donald; Hóa học đất môi trường. 2003, Nhà xuất bản Học thuật, Luân Đôn, Vương quốc Anh
- ^ a b c Bloom, Paul R.; Skyllberg, Ulf (2012). "Soil pH and pH buffering". Trong Huang, Pan Ming; Li, Yuncong; Sumner, Malcolm E. (biên tập). Handbook of soil sciences: properties and processes (ấn bản thứ 2). Boca Raton, FL: CRC Press. tr. 19-1 to 19-14. ISBN 9781439803059.
- ^ Oosterbaan, R.J. "Soil Alkalinity (Alkaline-sodic soils)" (PDF). www.waterlog.info. Truy cập ngày 16 tháng 5 năm 2017.
- ^ Brady, N. và Weil, R. Bản chất và tính chất của đất. Tái bản lần thứ 13 2002
- ^ a b c Kopittke, Peter M.; Menzies, Neal W.; Wang, Peng; Blamey, F. Pax C. (tháng 8 năm 2016). "Kinetics and nature of aluminium rhizotoxic effects: a review". Journal of Experimental Botany. Quyển 67 số 15. tr. 4451–4467. doi:10.1093/jxb/erw233.
- ^ Hansson et al (2011) Sự khác biệt về tính chất đất trong các cây liền kề của cây thông Scots, cây vân sam Na Uy và bạch dương ở SW Thụy Điển.
- ^ Rout, GR; Samantaray, S; Das, P (2001). "Aluminium toxicity in plants: a review" (PDF). Agronomie. Quyển 21 số 1. tr. 4–5. doi:10.1051/agro:2001105. Truy cập ngày 11 tháng 6 năm 2014.
- ^ Shavrukov, Yuri; Hirai, Yoshihiko (tháng 1 năm 2016). "Good and bad protons: genetic aspects of acidity stress responses in plants". Journal of Experimental Botany. Quyển 67 số 1. tr. 15–30. doi:10.1093/jxb/erv437.
- ^ Finck, Arnold (1976). Pflanzenernährung in Stichworten. Kiel: Hirt. tr. 80. ISBN 3-554-80197-6.
- ^ a b Sumner, Malcolm E.; Yamada, Tsuioshi (tháng 11 năm 2002). "Farming with acidity". Communications in Soil Science and Plant Analysis. Quyển 33 số 15–18. tr. 2467–2496. doi:10.1081/CSS-120014461.
- ^ a b Bolan, N; Brennan, R. (2011). "Bioavailability of N, P, K, Ca, Mg, S, Si, and Micronutrients". Trong Huang, Pan Ming; Li, Yuncong; Sumner, Malcolm E. (biên tập). Handbook of soil sciences: resource management and environmental impacts (ấn bản thứ 2). Boca Raton, FL: CRC Press. tr. 11-1 to 11-80. ISBN 9781439803073.
- ^ Truog, Emil (1946). "The Liming of Soils". Science in farming, USDA Yearbook, 1941–1947. tr. 566–576.
- ^ a b Sumner, M.E.; Farina, M.P.W. (1986). "Phosphorus interactions with other nutrients and lime in field cropping systems". Trong Stewart, B.A. (biên tập). Advances in Soil Science. New York, NY: Springer New York. tr. 201–236. ISBN 978-1-4613-8660-5.
- ^ Haynes, R. J. (tháng 10 năm 1982). "Effects of liming on phosphate availability in acid soils". Plant and Soil. Quyển 68 số 3. tr. 289–308. doi:10.1007/BF02197935.
- ^ Ellis, Boyd; Foth, Henry (ngày 9 tháng 3 năm 2017). "Soil Fertility, Second Edition". Google Books. tr. 73–74. Truy cập ngày 19 tháng 5 năm 2017.
- ^ "Sodic soils". plantsinaction.science.uq.edu.au (bằng tiếng Anh). Bản gốc lưu trữ ngày 19 tháng 4 năm 2018. Truy cập ngày 19 tháng 5 năm 2017.
- ^ a b USDA PLANTS Database (2017). "PLANTS Database Advanced Search using minimum and maximum pH". plants.usda.gov. USDA NCRS. Truy cập ngày 2 tháng 6 năm 2017.
- ^ Plants for a Future. "Plant Database Search". www.pfaf.org. Truy cập ngày 22 tháng 5 năm 2017.
- ^ Hill, M.O.; Mountford, J.O.; Roy, D.B.; Bunce, R.G.H. (1999). Ellenberg's indicator values for British plants. ECOFACT Volume 2. Technical Annex (PDF). Institute of Terrestrial Ecology. ISBN 1870393481. Truy cập ngày 29 tháng 5 năm 2017.
- ^ Lee, J.A. (1998). "The calcicole-calcifuge problem revisited". Advances in Botanical Research. Quyển 29. tr. 13. Truy cập ngày 5 tháng 6 năm 2017.
- ^ Scott, B.J.; Fisher, J.A. (1989). "Selection of genotypes tolerant of aluminium and manganese". Trong Robson, A.D. (biên tập). Soil acidity and plant growth. Sydney: Academic Press. tr. 167–203. ISBN 0125906552. Truy cập ngày 5 tháng 6 năm 2017.
- ^ Aitken, R.L.; Moody, P.W.; Mckinley, P.G. (1990). "Lime requirement of acidic Queensland soils. I. Relationships between soil properties and pH buffer capacity". Australian Journal of Soil Research. Quyển 28 số 5. tr. 695–701. doi:10.1071/SR9900695. Truy cập ngày 5 tháng 6 năm 2017.
- ^ Von Uexkull, H.R. (1986). "Lime and liming". Efficient Fertilizer Use in Acid Upland Soils of the Humid Tropics (bằng tiếng Anh). Food & Agriculture Org. tr. 16–22. ISBN 9789251023877. Truy cập ngày 5 tháng 6 năm 2017.
- ^ Cox, Loralie. "SOLUTIONS TO SOIL PROBLEMS" (PDF).
- ^ "Soil Quality Indicators: pH" (PDF). NCRS.USDA. Bản gốc (PDF) lưu trữ ngày 16 tháng 2 năm 2020.
- ^ "Solutions to Soil Problems: High pH – eXtension" (bằng tiếng Anh). Bản gốc lưu trữ ngày 16 tháng 11 năm 2018. Truy cập ngày 26 tháng 2 năm 2017.
Từ khóa » độ Ph Của đất Bao Nhiêu Là Tốt
-
PH đất Là Gì ? Cách Xem Tính Chất Của đất Trồng Thông Qua Chỉ Số PH
-
PH đất Bao Nhiêu Thì Thích Hợp Cho Cây Trồng Phát Triển?
-
PH đất Là Gì? Độ PH Nào Thích Hợp Cho Cây Trồng? - Sfarm
-
TẦM QUAN TRỌNG CỦA PH TRONG ĐẤT TRỒNG
-
Hướng Dẫn Chi Tiết Cách đo độ PH Của đất
-
Tìm Hiểu Chi Tiết Các Cách đo độ PH Của đất Phổ Biến Nhất Hiện Nay
-
Độ PH Của đất - Thế Giới Giá Thể, đất Trồng Cây
-
Độ PH Của đất Trồng Và Cách Tăng Giảm độ PH - AZ Farming
-
Độ PH Là Gì? PH Trong Cơ Thể ở Mức Bao Nhiêu?
-
Độ PH Của đất Là Gì? Độ PH đất ảnh Hưởng đến Cây Trồng Như Thế ...
-
Độ PH âm đạo Bao Nhiêu Là Bình Thường? | Vinmec
-
Độ PH Của Da Là Gì Và Bao Nhiêu Là Bình Thường? | Vinmec
-
PH đất Là Gì? Cách Cải Tạo đất Chua, đất Kiềm, Bảng Tra Cứu PH đất
-
Chỉ Số PH Đất Phù Hợp Với Các Loại Cây Trồng Tại Việt Nam
![{\displaystyle {\mathrm {CaCl} {\vphantom {A}}_{\smash[{t}]{2}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a4a568dd23b6accc3e836cd448bebe96b18fb275)