Hoá Học 9 Bài 7: Tính Chất Hóa Học Của Bazơ - Hoc247
Có thể bạn quan tâm
Nội dung bài học chủ yếu đề cập đến tính chất hoá học chung của bazơ (tác dụng với chất chỉ thị màu, và với axit); tính chất hoá học riêng của bazơ tan (kiềm) (tác dụng với oxit axit và với dung dịch muối); tính chất riêng của bazơ không tan trong nước (bị nhiệt phân huỷ).
ATNETWORK YOMEDIA1. Tóm tắt lý thuyết
1.1. Tác dụng với chất chỉ thị
1.2. Tác dụng với oxit axit (tạo muối và nước)
1.3. Tác dụng với axit (tạo muối và nước)
1.4. Bazơ không tan bị nhiệt phân huỷ
1.5. Tổng kết
2. Bài tập minh hoạ
3. Luyện tập Bài 7 Hóa học 9
3.1. Trắc nghiệm
3.2. Bài tập SGK và Nâng cao
4. Hỏi đáp về Bài 7 chương 1 Hóa học 9

Tóm tắt lý thuyết
1.1. Tác dụng với chất chỉ thị
- Quỳ tím hóa xanh .
- Phenolphtalin không màu thành đỏ.
- Các em chú ý quan sát hiện tượng xảy ra trên miếng quỳ trong thí nghiệm sau:
Video 1: Sự đổi màu của quỳ tím trong các môi trường axit, bazơ và nước
1.2. Tác dụng với oxit axit (tạo muối và nước)
- Oxit axit tác dụng với dung dịch bazơ tạo thành muối và nước.
- Thí nghiệm: Khí CO2 tác dụng với dung dịch Ca(OH)2
Video 2: Khí CO2 làm vẩn đục dung dịch nước vôi trong
- Hiện tượng: Khi sục khí CO2 vào dung dịch nước vôi trong thấy kết tủa trắng.
- Giải thích: Do phản ứng CO2 + Ca(OH)2 → CaCO3 (kết tủa trắng) + H2O
Ví dụ khác:
Ca(OH)2+ SO2 → CaSO3 + H2O
6KOH+ P2O5→2K3PO4+ 3H2O
1.3. Tác dụng với axit (tạo muối và nước)
- Các em chú ý quan sát thao tác thí nghiệm và hiện tượng phản ứng diễn ra:
Video 2: Phản ứng giữa dung dịch Cu(OH)2 và H2SO4
- Hiện tượng: Cu(OH)2 tan dần và tạo dung dịch màu xanh
- Giải thích: Do xảy ra phản ứng H2SO4l+Cu(OH)2 → CuSO4 + 2H2O
Ví dụ khác:
Fe(OH)3 + 3HCl → FeCl3 + 3H2O
Ba(OH)2+ 2HNO3→ Ba(NO3)2 + 2H2O
1.4. Bazơ không tan bị nhiệt phân huỷ (tạo oxit và nước)
- Các em chú ý quan sát thao tác thí nghiệm và hiện tượng phản ứng diễn ra:
Video 3: Phản ứng Nhiệt phân Đồng (II) hidroxit
- Hiện tượng: Cu(OH)2 chất rắn màu xanh chuyển dần thành bột màu đen
- Giải thích: Do xảy ra phản ứng
Cu(OH)2 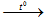
Màu xanh Màu đen
1.5. Tổng kết
Hình 1: Sơ đồ tư duy bài tính chất hóa học của bazơ
Bài tập minh họa
Bài 1:
Có những bazơ sau: NaOH, Cu(OH)2, Ba(OH)2. Hãy cho biết những bazơ nào: (viết PTHH minh họa nếu có)
a) Tác dụng được với dd HCl?
b) Bị nhiệt phân hủy?
c) Tác dụng được với CO2?
d) Đổi màu quì tím thành xanh?
Hướng dẫn:
a) Tác dụng được với dd HCl: NaOH, Cu(OH)2, Ba(OH)2
2NaOH (dd) + 2HCl (dd) → 2NaCl (dd) + H2O (l)
Cu(OH)2 (dd) + 2HCl (dd) → CuCl2 (dd) + 2H2O (l)
Ba(OH)2 (dd) + 2HCl (dd) → FeCl2 (dd) + 2H2O (l)
b) Bị nhiệt phân hủy: Cu(OH)2
Cu(OH)2 (r) .PNG)
c) Tác dụng được với CO2: NaOH, Ba(OH)2
2NaOH (dd) + CO2 (k) → Na2CO3 (dd) + H2O (l)
Ba(OH)2 (dd) + CO2 (k) → BaCO3 (dd) + H2O (l)
d) Đổi màu quì tím thành xanh: NaOH, Ba(OH)2
Bài 2:
Cần bao nhiêu ml dung dịch NaOH 0,75M để trung hoà 400ml hỗn hợp dung dịch axit gồm H2SO4 0,5M và HCl 1M.
Hướng dẫn:
Đổi 400ml thành 0,4 lít
Số mol mỗi axit là:
\(\begin{array}{l} {n_{{H_2}S{O_4}}} = {C_M}.V = 0,4 \times 0,5 = 0,2(mol)\\ {n_{HCl}} = {C_M}.V = 0,4 \times 1 = 0,4(mol) \end{array}\)
Phương trình phản ứng:
H2SO4 + 2NaOH → Na2SO4 + 2H2O
0,2 → 0,4 (mol)
HCl + NaOH → NaCl + H2O
0,4 → 0,4 (mol)
Số ml dung dịch NaOH 0,75M cần để trung hòa lượng axit trên là:
\({C_M} = \frac{n}{V} \Rightarrow V = \frac{n}{{{C_M}}} = \frac{{0,4 + 0,4}}{{0,75}} = 1,07(lit)\)
3. Luyện tập Bài 7 Hóa học 9
Sau bài học cần nắm:
- Tính chất hoá học chung của bazơ (tác dụng với chất chỉ thị màu, và với axit)
- Tính chất hoá học riêng của bazơ tan (kiềm) (tác dụng với oxit axit và với dung dịch muối); tính chất riêng của bazơ không tan trong nước (bị nhiệt phân huỷ).
3.1. Trắc nghiệm
Bài kiểm tra Trắc nghiệm Hóa học 9 Bài 7 có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
-
Câu 1:
Dung dịch làm phenolphtalein không màu thành màu hồng là:
- A. H2SO4
- B. NaCl
- C. Ca(OH)2
- D. K2SO4
-
Câu 2:
Chỉ dùng nước có thể nhận biết chất rắn nào trong 4 chất rắn sau đây :
- A. Zn(OH)2
- B. Fe(OH)2
- C. NaOH
- D. Al(OH)3
-
Câu 3:
Chất khí sẽ không bị giữ lại khi cho qua dung dịch Ca(OH)2 là:
- A. CO2
- B. O2
- C. SO2
- D. Cả A , B và C
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
3.2. Bài tập SGK và Nâng cao
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 9 Bài 7.
Bài tập 1 trang 25 SGK Hóa học 9
Bài tập 2 trang 25 SGK Hóa học 9
Bài tập 3 trang 25 SGK Hóa học 9
Bài tập 4 trang 25 SGK Hóa học 9
Bài tập 5 trang 25 SGK Hóa học 9
Bài tập 7.1 trang 9 SBT Hóa học 9
Bài tập 7.2 trang 9 SBT Hóa học 9
Bài tập 7.3 trang 9 SBT Hóa học 9
Bài tập 7.4 trang 9 SBT Hóa học 9
Bài tập 7.5 trang 9 SBT Hóa học 9
4. Hỏi đáp về Bài 7 chương 1 Hóa học 9
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa HOC247 thảo luận và trả lời nhé.
 NONE
NONE Bài học cùng chương
 Hoá học 9 Bài 1: Tính chất hóa học của oxit và Khái quát về sự phân loại oxit
Hoá học 9 Bài 1: Tính chất hóa học của oxit và Khái quát về sự phân loại oxit  Hoá học 9 Bài 2: Một số oxit quan trọng
Hoá học 9 Bài 2: Một số oxit quan trọng  Hoá học 9 Bài 3: Tính chất hóa học của axit
Hoá học 9 Bài 3: Tính chất hóa học của axit  Hoá học 9 Bài 4: Một số axit quan trọng
Hoá học 9 Bài 4: Một số axit quan trọng  Hoá học 9 Bài 5: Luyện tập Tính chất hóa học của oxit và axit
Hoá học 9 Bài 5: Luyện tập Tính chất hóa học của oxit và axit  Hoá học 9 Bài 6: Thực hành Tính chất hóa học của oxit và axit ADSENSE TRACNGHIEM
Hoá học 9 Bài 6: Thực hành Tính chất hóa học của oxit và axit ADSENSE TRACNGHIEM  Bộ đề thi nổi bật
Bộ đề thi nổi bật  UREKA AANETWORK
UREKA AANETWORK 
XEM NHANH CHƯƠNG TRÌNH LỚP 9
Toán 9
Lý thuyết Toán 9
Giải bài tập SGK Toán 9
Trắc nghiệm Toán 9
Đại số 9 Chương 4
Hình học 9 Chương 3
Ngữ văn 9
Lý thuyết Ngữ Văn 9
Soạn văn 9
Soạn văn 9 (ngắn gọn)
Văn mẫu 9
Soạn bài Viếng lăng bác
Tiếng Anh 9
Giải bài Tiếng Anh 9
Giải bài tập Tiếng Anh 9 (Mới)
Trắc nghiệm Tiếng Anh 9
Unit 6 Lớp 9 The environment
Tiếng Anh 9 mới Unit 9
Vật lý 9
Lý thuyết Vật lý 9
Giải bài tập SGK Vật Lý 9
Trắc nghiệm Vật lý 9
Vật Lý 9 Chương 3
Hoá học 9
Lý thuyết Hóa 9
Giải bài tập SGK Hóa học 9
Trắc nghiệm Hóa 9
Hóa học 9 Chương 4
Sinh học 9
Lý thuyết Sinh 9
Giải bài tập SGK Sinh 9
Trắc nghiệm Sinh 9
Ôn tập Sinh 9 Chương 1- SV&MT
Lịch sử 9
Lý thuyết Lịch sử 9
Giải bài tập SGK Lịch sử 9
Trắc nghiệm Lịch sử 9
Lịch Sử 9 Chương 4 Lịch Sử VN
Địa lý 9
Lý thuyết Địa lý 9
Giải bài tập SGK Địa lý 9
Trắc nghiệm Địa lý 9
Địa Lý 9 Sự Phân Hóa Lãnh Thổ
GDCD 9
Lý thuyết GDCD 9
Giải bài tập SGK GDCD 9
Trắc nghiệm GDCD 9
GDCD 9 Học kì 2
Công nghệ 9
Lý thuyết Công nghệ 9
Giải bài tập SGK Công nghệ 9
Trắc nghiệm Công nghệ 9
Công nghệ 9 Quyển 4
Tin học 9
Lý thuyết Tin học 9
Giải bài tập SGK Tin học 9
Trắc nghiệm Tin học 9
Tin học 9 Chương 3
Cộng đồng
Hỏi đáp lớp 9
Tư liệu lớp 9
Xem nhiều nhất tuần
Đề thi giữa HK1 lớp 9
Đề thi HK2 lớp 9
Đề thi giữa HK2 lớp 9
Đề thi HK1 lớp 9
8 bài văn mẫu Chuyện người con gái Nam Xương
5 bài văn mẫu về tác phẩm Nói với con
Văn mẫu Nghị luận về một vấn đề tư tưởng, đạo lí
5 bài văn mẫu bài thơ Sang thu
6 bài văn mẫu về tác phẩm Lặng lẽ Sa Pa
5 bài văn mẫu hay về bài thơ Con cò
Sang thu
Tiếng Anh Lớp 9 Unit 7
Mùa xuân nho nhỏ
Tiếng Anh Lớp 9 Unit 8
Video Toán NC lớp 9- Luyện thi vào lớp 10 Chuyên Toán
YOMEDIA YOMEDIA ×Thông báo
Bạn vui lòng đăng nhập trước khi sử dụng chức năng này.
Bỏ qua Đăng nhập ×Thông báo
Bạn vui lòng đăng nhập trước khi sử dụng chức năng này.
Đồng ý ATNETWORK ON QC Bỏ qua >>
QC Bỏ qua >> 
Từ khóa » Giải Bài Tập Hóa 9 Bài 7 Trang
-
Giải Hóa 9 Bài 7: Tính Chất Hóa Học Của Bazơ
-
Giải Bài 7 Trang 19 SGK Hóa 9
-
Giải Hóa 9 Bài 7: Tính Chất Hóa Học Của Bazơ
-
Bài 7. Tính Chất Hóa Học Của Bazơ
-
Bài 7 Trang 19 SGK Hóa Học 9
-
Giải Vở Bài Tập Hóa Học 9 Bài 7: Tính Chất Hóa Học Của Bazơ
-
Hóa 9 Bài 7: Tính Chất Hóa Học Của Bazơ - Haylamdo
-
Tính Chất Hóa Học Của Bazơ - Giải Hoá 9 Trang 25
-
Giải Bài 7 Hóa Học 9: Tính Chất Hóa Học Của Bazơ - Tech12h
-
Giải Bài Tập Hóa 9 Bài 7: Tính Chất Hóa Học Của Bazơ
-
Bài 1,2,3,4,5 Trang 25 SGK Hóa Lớp 9: Tính Chất Hóa Học Của Bazơ
-
Giải Bài 7.1, 7.2, 7.3, 7.4, 7.5 Trang 9 Sách Bài Tập Hóa Học 9
-
Giải Bài Tập Hóa 9 Bài 7 - Thu Trang
-
Hóa 9 Bài 7
.PNG)