K2cr2o7 Là Gì? Ứng Dụng Của K2cr2o7 Và Nơi Mua Hóa Chất
Có thể bạn quan tâm
K2CR2O7 là gì? Kali Dicromat là gì? Cấu tạo phân tử của K2CR2O7 như thế nào? Tính chất lý hóa của K2CR2O7 – Kali Dicromat ra sao? Làm thế nào để có thể điều chế được K2CR2O7? Những ứng dụng vượt bật của hóa chất này là gì? Những lưu ý nào khi sử dụng – bảo quản K2CR2O7? Và nơi nào tại TP Hồ Chí Minh cung cấp hóa K2CR2O7 này?
Cũng giống như nhiều hóa chất khác K2CR2O7 có những công dụng và tính chất đặc trưng riêng cho chính mình. Để có thể hiểu được về K2CR2O7 thì hôm nay Công Ty Trung Sơn sẽ giới thiệu đến bạn một bài viết xoay quanh chủ đề về hóa chất K2CR2O7 – Dicromat là gì?
Nào chúng ta hãy cùng theo dõi bài viết dưới đây!
K2CR2O7 LÀ GÌ? CẤU TẠO PHÂN TỬ CỦA KALI DICROMAT
K2CR2O7 là gì?

K2CR2O7 là công thức hóa học của một hợp chất vô cơ mang tính chất oxy hóa với tên gọi phổ biến là Kali dicromat. K2CR2O7 có màu đỏ cam rất đặc trưng ở dạng tinh thể. Đây là hóa chất rất độc hại đối với cơ thể con người.
K2CR2O7 là hợp chất muối với nhiều tên gọi khác nhau như Potassium dichromate, potassium bichromate, dichromic acid, dipotassium salt, chromic acid, dipotassium salt.
Công thức hóa học của kali cromat là K2CR2O7
K2CR2O7 là hóa chất được ứng dụng khá phổ biến trong công nghiệp hiện nay như ứng dụng trong các ngành thuộc da, xi mạ, bảo quản gỗ, bảo quản kim loại, chống ăn mòn, ….
Cấu tạo phân tử K2CR2O7 là gì?
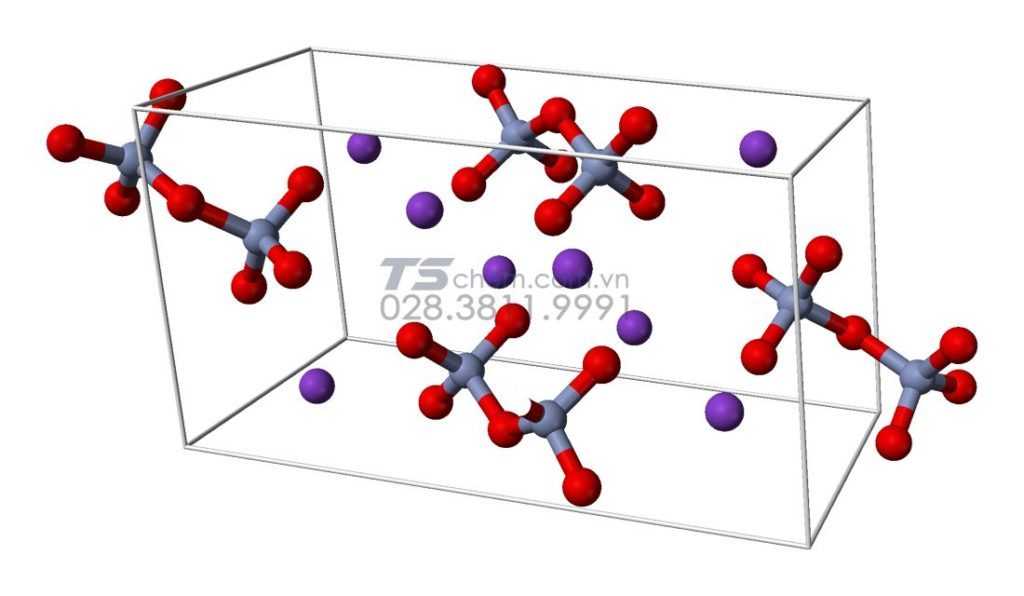
 +
+Ống chuẩn K2Cr2O7 0,1N – 1099280001 – Merck
Tư vấn ngay- Thương hiệu: Merck – Đức
- Mã sản phẩm: 1099280001
- Khối lượng riêng: 1.06 g/cm3 (20 °C)
- Giá trị pH: 4.1 (H₂O, 25 °C)
- Nhiệt độ bảo quản: +15°C to +25°C.
- Sản phẩm là dung dịch chuẩn sử dụng trong chuẩn độ
TÍNH CHẤT LÝ HÓA CỦA KALI DICROMAT – K2CR2O7
Tính chất vật lý của K2CR2O7 là gì?
- K2CR2O7 – Kali Dicromat có dạng tinh thể rắn, không mùi, vị đắng, tan được trong nước nhưng không hòa tan được trong alcohol, acetone và nó không tồn tại dưới dạng ngậm nước.
- Màu sắc của K2Cr2O7 dạng tinh thể là cam đỏ. Khi đun sôi dung dịch có màu đỏ thẫm đậm.
- Khối lượng mol của K2Cr2O7 là 294.185 g/mol.
- Khối lượng riêng của K2Cr2O7 là 2.676 g/cm3, rắn.
- Điểm nóng chảy của K2Cr2O7 là 398 °C (671 K; 748 °F).
- Điểm sôi của K2Cr2O7 là 500 °C (773 K; 932 °F).
- Độ hòa tan trong nước của K2Cr2O7 là 4.9 g/100 mL (0 °C), 13 g/100 mL (20 °C) và 102 g/100 mL (100 °C).
Tính chất hóa học của K2CR2O7 là gì?
Dung dịch của K2Cr2O7 sẽ làm quỳ tím hóa đỏ.
Kali Dicromat là chất oxy hóa mạnh.
Trong môi trường axit muối Cr(VI) bị khử thành muối Cr(III).
- K2Cr2O7 + 6FeSO4 + 7H2SO4→3Fe2(SO4)3 +Cr2(SO4)3 + K2SO4 +7H2O
Kali Dicromat có thể tác dụng với dung dịch bazơ và sinh ra muối có màu vàng đó là K2CrO4.
- K2CrO7 + KOH => K2CrO4 + H2O
Kali Dicromat ở nhiệt độ 500 độ C bị phân hủy thành muối cromat.
- 4 K2Cr2O7 → 4 K2CrO4 + 2 Cr2O3 + H2O
Kali Dicromat tác dụng được với các axit như HCL hoặc H2SO4 như sau:
- K2Cr2O7 + H2SO4 → 2 K2Cr3O10+ K2SO4+ H2O
K2Cr2O7 + 14 HCl → 2 CrCl3+ 2 KCl + 3 Cl2+ 7 H2O
- Cách thực hiện phản ứng
- cho dung dịch axit hCl tác dụng với K2Cr2O7
- Hiện tượng nhận biết
- Xuất hiện khí màu vàng lục Clo (Cl2) làm sủi bọt khí.
ĐIỀU CHẾ KALI DICROMAT – K2CRO7 NHƯ THẾ NÀO?
K2Cr2O7 có thể được điều chế từ quặng cromit ( Fe(CrO2)2 ) qua 3 giai đoạn chính đó là:
Giai đoạn thứ nhất: Dùng không khí oxi hóa hỗn hợp đã nghiền mịn của cromit, sođa và đá vôi sau đó đem nung nóng trong lò với nhiệt độ giao động từ 1000°C – 1300°C.
- 4 Fe(CrO2)2+ 8 Na2CO3+ 7 O2 → 8 Na2CrO4+ 2 Fe2O3+ 8 CO2
Giai đoạn thứ hai: Hòa tan hỗn hợp sản phẩm Na2CrO4 rồi cho tác dụng với Axit Sulfuric để chuyển cromat thành dicromat.
- 2 Na2CrO4 + 2 H2SO4 → Na2Cr2O7+ 2 NaHSO4+ H2O
Giai đoạn cuối cùng: Ta tiến hành chuyển Na2Cr2O7 thành K2Cr2O7 bằng phản ứng trao đổi.
- Na2Cr2O7+ 2 KCl → K2Cr2O7+ 2 NaCl
Tham khảo thêm bài viết: Axit hipoclorơ là gì? Những điều cần biết về hoá chất này
 +
+Potassium dichromate (K2Cr2O7) – 7778-50-9 – Xilong
Tư vấn ngay- Thương hiệu: Xilong – Trung Quốc
- Số Cas: 7778-50-9
- Khối lượng phân tử: 294,19 g / mol
- Giá trị pH: 3,6 (100 g / l, H₂O)
- Điểm sôi: > 500 ° C (1013 hPa)
- Tỉ trọng: 2,7 g / cm3 (20 ° C)
ỨNG DỤNG CỦA KALI DICROMAT -K2CR2O7

Kali Dichromate K2Cr2O7 ứng dụng trong phòng thí nghiệm
- Kali Dichromate K2CrO7 được dùng với vai trò là thuốc thử trong hóa phân tích nhờ vào sự thay đổi màu sắc của hợp chất này trong nước cũng như trong một số hợp chất hữu cơ để xác định hàm lượng của một số hợp chất.
Kali Dichromate K2Cr2O7 ứng dụng trong công nghiệp sản xuất
- Kali Dichromate K2Cr2O7 là nguồn nguyên liệu để tổng hợp nên axit cromic sử dụng trong công nghiệp thủy tinh : làm sạch và điêu khắc trong các sản phẩm thủy tinh.
- Sản phẩm được sử dụng trong sản xuất, xử lý gỗ và đó cũng chính là một thành phần được sử dụng trong sản xuất xi măng để tăng độ kết dính.
- Kali Dichromate K2Cr2O7 còn được ứng dụng trong công nghệ nhiếp ảnh và in ấn. Sản xuất thuốc nhuôm
- Kali Dichromate K2Cr2O7 là hóa chất được sử dụng trong các lĩnh vực in, nhiếp ảnh, sản xuất thuốc nhuộm, sử dụng trong lĩnh vực da,….
- Kali Dichromate K2Cr2O7 là nguyên liệu để sản xuất phèn crom, oxit crom xanh, chất màu vàng crôm hoặc với tính chất như một chất oxy hóa, nó được dùng để sản xuất kalium crom và để sản xuất thuốc thử hóa học.
NHỮNG LƯU Ý KHI SỬ DỤNG VÀ BẢO QUẢN K2CR2O7

Cảnh báo nguy hiểm đối với con người:
- K2Cr2O7 gây kích ứng da và có thể gây bỏng da. Nguy hiểm hơn có thể gây lỡ loét.
- Kali Dichromate K2Cr2O7 gây tổn thương cho nghiêm trọng cho thị lực như giác mạc phồng lên, loạn thị không thường xuyên và gây mê.
- Kali Dichromate K2Cr2O7 khi hít phải kích ứng đường hô hấp dù chỉ một lượng nhỏ.
- Kali Dichromate K2Cr2O7 nếu nuốt phải với số lượng nhỏ, nó có thể gây bỏng thực quản, phế quản và thủng dạ dày. Các triệu chứng có thể bao gồm đau thực quản, buồn nôn, nôn, tiêu chảy, đường tiêu hóa gây kích ứng và chảy máu, suy hô hấp, tím tái, hôn mê, và chết.
- Kali Dichromate K2Cr2O7 cũng có thể ảnh hưởng đến hệ tim mạch, gan và hệ thống thần kinh.
Những lưu ý khi sử dụng và bảo quản K2Cr2O7
- Chúng ta cần phải thận trọng trước những hóa chất không tương thích với K2Cr2O7 như : phản ứng với chất khử, vật liệu dễ cháy, vật liệu hữu cơ, kim loại, axít, kiềm.
- Không được bảo quản, lưu trữ K2Cr2O7 trong thủy tinh vì nó mang tính ăn mòn.
- K2Cr2O7 rất dễ dàng oxy hóa vật liệu như gỗ, giấy, nhôm, lưu huỳnh, sắt, vonfram, acid sulfuric + aceton nên cần thận trọng.
- Khi tiếp xúc với hóa chất cần trang bị bảo hộ lao động cá nhân như kính bảo hộ, áo khoác phòng thí nghiệm, khẩu trang thích hợp, găng tay.
- Khi tồn trữ K2CrO7 luôn phải giữ bình hóa chất khô, tránh xa nguồn nóng, nguồn phát lửa, không được nuốt, không được hít bụi và lưu trữ ở 1 ngăn cách biệt và an toàn.
Tìm hiểu thêm: Axít Gluconic là gì? Cấu tạo phân tử, tính chất, điều chế & ứng dụng
SẢN PHẨM CÙNG DANH MỤC
 +
+Ống chuẩn K2Cr2O7 0,1N – 1099280001 – Merck
 +
+Hóa chất Potassium Dichromate, Certified AR for Analysis – Fisher
 +
+Hóa chất Potassium dichromate K2Cr2O7 – Scharlau
 +
+Potassium dichromate (K2Cr2O7) – 7778-50-9 – Xilong
Tư vấn ngayNƠI MUA HÓA CHẤT KALI DICROMAT – K2CR2O7

Công ty Công Nghệ Trung Sơn là nhà cung cấp và phân phối hóa chất Kali Dichromate K2Cr2O7 tại TPHCM. Với những ưu điểm vượt bật như sản phẩm hóa chất luôn đảm bảo hàng hóa chất lượng và nguồn hàng ổn định, giá cả rất cạnh tranh, phù hợp và chính sách giao hàng rất nhanh, …
Công ty Trung Sơn có rất nhiều năm kinh doanh cũng như kinh nghiệm trong việc cung cấp hóa chất vì vậy chúng tôi tin chắc rằng sẽ khiến bạn hài lòng về những dịch vụ bên chúng tôi đem đến.
Ngoài hóa chất Kali Dichromate K2Cr2O7, Công ty Trung Sơn còn cung cấp cho khách hàng của mình những loại hóa chất công nghiệp, thiết bị, dụng cụ phòng thí nghiệm tốt nhất, với giá thành hợp lý trên thị trường.
Nếu bạn có nhu cầu tìm mua những sản phẩm trên thì không nên bỏ qua công ty Trung Sơn của chúng tôi.
Những điều xoay quanh về hóa chất Kali Dichromate K2Cr2O7 như K2CR2O7 là gì? Kali Dicromat là gì? Cấu tạo phân tử của K2CR2O7 như thế nào? Tính chất lý hóa của K2CR2O7 – Kali Dicromat ra sao? Làm thế nào để có thể điều chế được K2CR2O7? Những ứng dụng vượt bật của hóa chất này là gì? Những lưu ý nào khi sử dụng – bảo quản K2CR2O7? Mà công ty Trung Sơn đem đến, chắc chắn đã cung cấp cho bạn kha khá thông tin rồi đúng không nè?
Cảm ơn bạn đã theo dõi bài viết và nếu có bất kỳ thắc mắc nào thì đừng quên để lại bình luận ngay bên dưới để được nhân viên chúng tôi hỗ trợ.
YÊU CẦU CỦA KHÁCH HÀNG
Từ khóa » định Tính Paracetamol Bằng K2cr2o7
-
TH Hóa Dược 2 Bài 3 - 123doc
-
Thực Hành Hóa Dược B3 - PDFCOFFEE.COM
-
TH C Hành Hóa Dư C B3 | PDF - Scribd
-
[PDF] MÔ TĂ NGẮN GỌN HIỆN TƯỢNG CỦA CÁC PHÉP ĐỊNH TÍNH SAU
-
Thực Hành Kiểm Nghiệm ÔN THI TKIỂM NGHIỆM THỰC HÀcx
-
TopList #Tag: Định Tính Paracetamol Bằng K2Cr2O7
-
[PDF] THỰC HÀNH HÓA DƯỢC - Cao Đẳng Y Tế Ninh Bình
-
BÀI BÁO CÁO HÓA DƯỢC - ACID ASCORBIC - NATRI CLORID ...
-
THUỐC GIẢM ĐAU- HẠ SỐT- KHÁNG VIÊM Flashcards | Quizlet
-
Kiểm Nghiệm Paracetamol Flashcards | Quizlet
-
định Lượng đồng Thời Paracetamol, Phenylephrine Hydrocloride Và ...
-
Paracetamol (acetaminophen 500mg): Thuốc Giảm đau, Hạ Sốt
-
Định Lượng Vitamin B12 Bằng Phương Pháp Uv-Vis / TOP #10 Xem ...