Lượng Axit Nucleic- Phần 1
Có thể bạn quan tâm
Trong sinh học phân tử, việc định lượng các axit nucleic thường được thực hiện để xác định nồng độ trung bình DNA hoặc RNA trong hỗn hợp, cũng như độ tinh khiết của chúng. Các phản ứng sử dụng axit nucleic thường đòi hỏi một lượng và độ tinh khiết đặc biệt để có hiệu suất tối ưu. Cho đến nay, có hai cách tiếp cận chính được sử dụng bởi các nhà khoa học để định lượng, hoặc thiết lập nồng độ của axit nucleic (như DNA hoặc RNA) trong dung dịch. Đây là các phép đo lượng tử quang phổ và sự gắn kết huỳnh quang tia cực tím với sự hiện diện của một chất nhuộm DNA
 Phân tích quang phổ Một trong những thực tiễn được sử dụng phổ biến để định lượng DNA hoặc RNA là sử dụng phân tích quang phổ sử dụng một quang phổ kế . Máy quang phổ có thể xác định nồng độ trung bình của DNA axit nucleic hoặc RNA trong hỗn hợp, cũng như độ tinh khiết của chúng.
Phân tích quang phổ Một trong những thực tiễn được sử dụng phổ biến để định lượng DNA hoặc RNA là sử dụng phân tích quang phổ sử dụng một quang phổ kế . Máy quang phổ có thể xác định nồng độ trung bình của DNA axit nucleic hoặc RNA trong hỗn hợp, cũng như độ tinh khiết của chúng.
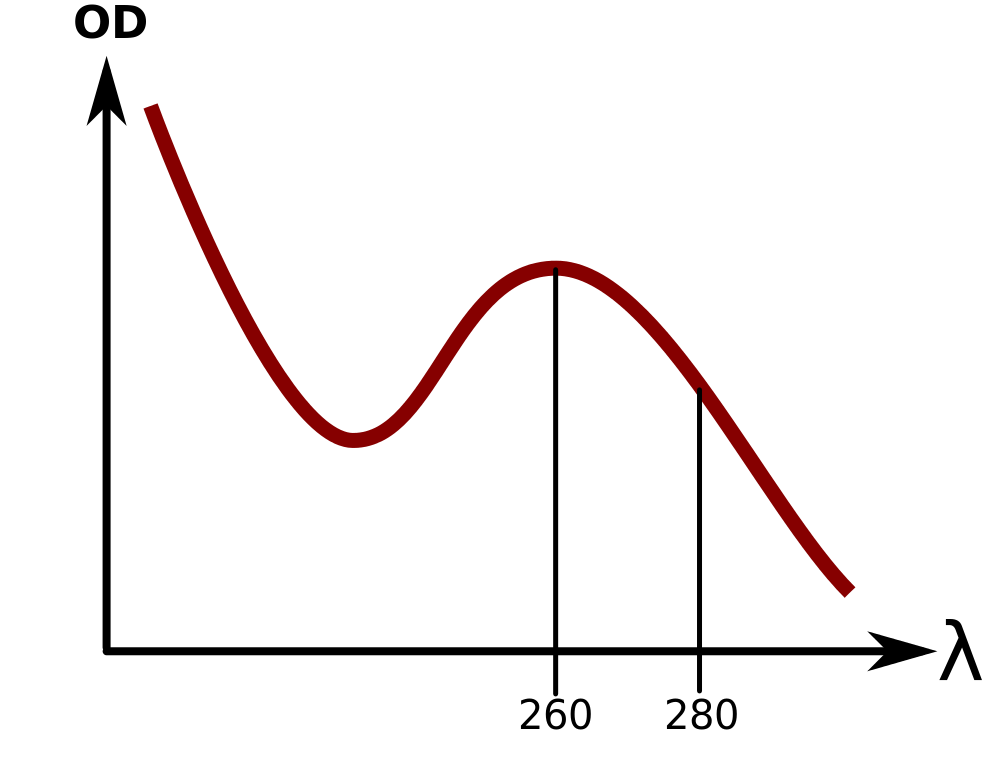
Phân tích quang phổ dựa trên các nguyên tắc mà axit nucleic hấp thụ ánh sáng cực tím theo một mẫu cụ thể. Trong trường hợp DNA và RNA, một mẫu được tiếp xúc với ánh sáng cực tím ở bước sóng 260 nanô mét (nm) và một máy dò ảnh đo ánh sáng đi qua mẫu. Một số ánh sáng cực tím sẽ đi qua và một số sẽ được hấp thụ bởi DNA / RNA. Ánh sáng càng hấp thụ bởi mẫu, nồng độ axit nucleic càng cao trong mẫu. Hiệu ứng kết quả là ít ánh sáng hơn sẽ tấn công photodetector và điều này sẽ tạo ra mật độ quang học cao hơn (OD)
Sử dụng Luật Beer-Lambert có thể liên quan đến lượng ánh sáng hấp thụ đến nồng độ của phân tử hấp thụ. Ở bước sóng 260 nm, hệ số tuyệt chủng trung bình của DNA sợi đôi là 0,020 (μg / ml) -1 cm-1, đối với DNA đơn sợi, 0,027 (μg / ml) -1 cm-1, đối với đơn RNA có vân là 0,025 (μg / ml) -1 cm-1 và đối với oligonucleotides sợi đơn đơn ngắn phụ thuộc vào độ dài và thành phần cơ bản. Do đó, Absorbance (A) là 1 tương ứng với nồng độ 50 μg / ml đối với DNA kép. Phương pháp tính này có giá trị cho đến A ít nhất là 2.Cần có một hệ số tuyệt chủng chính xác hơn cho các oligonucleotide; những điều này có thể được dự đoán bằng cách sử dụng mô hình hàng xóm gần nhất.
Tính toán Mật độ quang phổ được tạo ra từ phương trình:
Mật độ quang học = Log (cường độ ánh sáng / cường độ ánh sáng Ánh sáng truyền qua) Về mặt thực tế, một mẫu không chứa DNA hoặc RNA không nên hấp thụ bất kỳ ánh sáng cực tím nào và do đó tạo ra OD = 0
Mật độ quang học = Nhật ký (100/100) = 0
Khi sử dụng phân tích quang phổ để xác định nồng độ DNA hoặc RNA, luật Beer-Lambert được sử dụng để xác định nồng độ không biết mà không cần các đường cong tiêu chuẩn. Về cơ bản, Luật Beer Lambert làm cho nó có thể liên quan đến lượng ánh sáng hấp thụ vào nồng độ của phân tử hấp thụ. Các đơn vị hấp thụ sau cho các yếu tố chuyển đổi nồng độ axit nucleic được sử dụng để chuyển đổi OD thành nồng độ của các mẫu axit nucleic chưa biết:
A260 dsDNA = 50 μg / ml A260 ssDNA = 33 μg / ml A260 ssRNA = 40 μg / ml Các nhân tố chuyển đổi Khi sử dụng chiều dài đường dẫn 10 mm, chỉ cần nhân OD bằng hệ số chuyển đổi để xác định nồng độ. Ví dụ, mẫu dsDNA OD ODD 2.0 tương ứng với mẫu có nồng độ 100 ug / ml.
Khi sử dụng chiều dài đường dẫn ngắn hơn 10mm, OD kết quả sẽ được giảm bởi một yếu tố 10 / chiều dài đường dẫn. Sử dụng ví dụ trên với chiều dài đường dẫn 3 mm, OD đối với mẫu 100 ug / ml sẽ giảm xuống còn 0,6. Để bình thường hóa nồng độ tương đương 10mm, sau đây được thực hiện:
0,6 OD X (10/3) * 50 ug / ml = 100 ug / ml
Hầu hết các chất quang phổ cho phép lựa chọn loại axit nucleic và chiều dài đường dẫn để nồng độ kết quả được bình thường hóa với chiều dài đường dẫn 10 mm dựa trên các nguyên tắc của luật Bia.
Từ khóa » Tính Nồng độ Dna
-
Tinh Nong Do D NA Bang Ky Thuat Quang Pho Hap Thu
-
DNA - Duybiotech's Blog
-
TÍNH TOÁN SỐ LƯỢNG PHÂN TỬ TRONG MỘT LƯỢNG DNA ĐÃ ...
-
Phương Pháp Xác định Nồng độ ADN Trong Dung Dịch - LawNet
-
Phương Pháp Ly Trích Và Kiểm Tra Chất Lượng DNA
-
Pha Dung Dịch | Diễn đàn Sinh Học Việt Nam
-
DNA Là Gì Và ý Nghĩa Của Xét Nghiệm DNA | Vinmec
-
Các Loại Xét Nghiệm Sinh Học Phân Tử Thường Dùng | Vinmec
-
Xét Nghiệm Phân Mảnh DNA Tinh Trùng Trong Chẩn đoán Vô Sinh Nam
-
Máy Quang Phổ Xác định ADN, Protein, ARN
-
Máy đo Nồng độ DNA/RNA - Colibri
-
Máy đo Nồng độ đo Nồng độ DNA/ RNA/ Protein Colibri Berthold - Đức
-
Nguyên Lý Hoạt động Của Bộ Kit Tách Chiết ADN Trong Phòng Thí Nghiệm