Lý Thuyết Phản ứng Trao đổi Ion Trong Dung Dịch Các Chất điện Li (mới ...
Có thể bạn quan tâm
Lý thuyết Hóa 11 Bài 4: Phản ứng trao đổi ion trong dung dịch các chất điện li
Bài giảng Hóa 11 Bài 4: Phản ứng trao đổi ion trong dung dịch các chất điện li
1. Điều kiện xảy ra phản ứng trao đổi ion trong dung dịch các chất điện li
Xét phản ứng:
Dung dịch A + dung dịch B → Sản phẩm.
- Phản ứng xảy ra trong dung dịch các chất điện li là phản ứng giữa các ion.
- Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi các ion kết hợp được với nhau tạo thành ít nhất 1 trong số các chất sau:
+ Chất kết tủa.
+ Chất điện li yếu.
+ Chất khí.
Thí dụ:
+ Phản ứng tạo thành chất kết tủa:
Na2SO4 + BaCl2 → 2NaCl + BaSO4↓

Kết tủa BaSO4
+ Phản ứng tạo thành chất điện li yếu:
HCl + NaOH → NaCl + H2O
+ Phản ứng tạo thành chất khí:
Fe + H2SO4 loãng → FeSO4 + H2↑
2. Phương trình ion rút gọn
- Phương trình ion rút gọn cho biết bản chất của phản ứng trong dung dịch các chất điện li.
- Cách chuyển từ phương trình dưới dạng phân tử thành phương trình ion rút gọn như sau:
Bước 1:
+ Chuyển các chất vừa dễ tan, vừa điện li mạnh thành ion.
+ Các chất khí, chất kết tủa, chất điện li yếu để nguyên ở dạng phân tử.
⇒ Khi này, phương trình thu được gọi là phương trình ion đầy đủ.
Thí dụ: Xét phản ứng:
Na2SO4 + BaCl2 → 2NaCl + BaSO4↓
Phương trình ion đầy đủ là:
2Na+ +SO42-+ Ba2+ + 2Cl- → BaSO4↓ + 2Na+ + 2Cl-
Bước 2: Lược bỏ những ion không tham gia phản ứng, ta được phương trình ion rút gọn.
Ba2+ +SO42-→ BaSO4↓
Từ phương trình này ta thấy rằng, muốn điều chế kết tủa BaSO4 chỉ cần trộn 2 dung dịch, một dung dịch chứa Ba2+, dung dịch kia chứa ion SO42-.
Trắc nghiệm Hóa 11 Bài 4: Phản ứng trao đổi ion trong dung dịch các chất điện li
Câu 1:Dãy ionkhôngthể tồn tại đồng thời trong dung dịch là
A. Na+,OH−, Mg2+,NO3−
B. K+, H+,Cl−,SO42−
C.HSO3−, Mg+, Ca2+,NO3−
D.OH−, Na+, Ba2+, Cl−
Hiển thị đáp ánĐáp án: A
Giải thích:
![]()
Câu 2:Phương trình phản ứng: Ba(OH)2+ 2HCl → BaCl2+ 2H2O có phương trình ion rút gọn là:
A.H++ OH–→ H2O
B.Ba2++ 2OH–+ 2H++ 2Cl–→ BaCl2+ 2H2O
C.Ba2++ 2Cl–→ BaCl2
D.Cl–+ H+→ HCl
Hiển thị đáp ánĐáp án: A
Giải thích:
Phương trình phân tử:
Ba(OH)2 + 2HCl → BaCl2 + 2H2O
Phương trình ion đầy đủ:
Ba2+ + 2OH– + 2H+ + 2 → Ba2+ + 2 + 2H2O
Phương trình ion rút gọn:
H+ + OH– → H2O
Câu 3:Cho phản ứng: Mg(OH)2 + 2HCl → MgCl2 + H2O.
Phương trình ion thu gọn của phản ứng trên là
A.HCl + OH – → H2O +Cl−.
B.2H+ + Mg(OH)2 → Mg2+ + 2H2O.
C.H+ + OH – → H2O.
D.2HCl + Mg(OH)2 → Mg2+ + 2Cl− + 2H2O.
Hiển thị đáp ánĐáp án: B
Giải thích:
Ta có phản ứng: Mg(OH)2 + 2HCl → MgCl2 + 2H2O.
Phương trình ion đầy đủ là:
Mg(OH)2 + 2H+ + 2Cl− → Mg2+ + 2Cl− + 2H2O.
→ Phương trình ion thu gọn là: Mg(OH)2 + 2H+ → Mg2+ + 2H2O.
Câu 4:Phương trình ion rút gọn Ba2+ +SO42− → BaSO4 tương ứng với phương trình phân tử nào sau đây?
A.Ba(OH)2 + CuSO4 → BaSO4 + Cu(OH)2.
B.H2SO4 + BaCO3 → BaSO4 + CO2 + H2O.
C.Na2SO4 + Ba(NO3)2 → BaSO4 + 2NaNO3.
D.H2SO4 + Ba(OH)2 → BaSO4 + 2H2O.
Hiển thị đáp ánĐáp án: C
Giải thích: 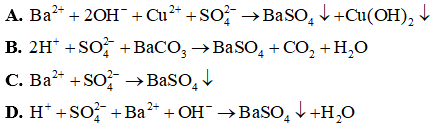
Câu 5:Phản ứng nào sau đây là phản ứng trao đổi ion trong dung dịch các chất điện li?
A.2Al + 3H2SO4→ Al2(SO4)3+ 3H2
B.2HCl + FeS → FeCl2+ H2S
C.NaOH + HCl → NaCl + H2O
D.Cu + 2AgNO3→ Cu(NO3)2+ 2Ag
Hiển thị đáp ánĐáp án: C
Giải thích: Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi các ion kết hợp được với nhau tạo thành ít nhất một trong các chất sau: chất kết tủa, chất điện li yếu, chất khí.
Câu 6:Trong dung dịch, ion OH- khôngtác dụng được với ion
A.K+.
B.H+.
C.HCO3−
D.Fe3+.
Hiển thị đáp ánĐáp án: A
Giải thích:
A. K+ không phản ứng được với
B. H++OH−→H2O
C. H++HCO3−→CO2+H2O
D. Fe3++3OH−→Fe(OH)3↓
Câu7:Cho dung dịch X chứa các ion: H+, Ba2+, NO3− vào dung dịch Y chứa các ion: Na+, SO32−, SO42−, S2−. Số phản ứng xảy ra làA.1.
B.2.
C.3.
D.4.
Hiển thị đáp ánĐáp án: D
Câu8:Cho các phản ứng hóa học sau:
(1) NaHS + NaOH →
(2) Ba(HS)2+ KOH →
(3) Na2S + HCl →
(4) CuSO4+ Na2S →
(5) FeS + HCl →
(6) NH4HS + NaOH →
Các phản ứng đều có cùng một phương trình ion rút gọn là:
A.(3), (4), (5).
B.(1), (2).
C.(1), (2), (6).
D.(1), (6).
Hiển thị đáp ánĐáp án: B
Giải thích:
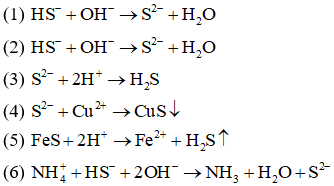
Câu9:Phương trình ion thu gọn:Ca2++CO32−→CaCO3↓là của phản ứng xảy ra giữa cặp chất nào sau đây?
(1) CaCl2+ Na2CO3
(2) Ca(OH)2+ CO2
(3) Ca(HCO3)2+ NaOH
(4) Ca(NO3)2+ (NH4)2CO3
A.(1) và (2).
B.(2) và (3).
C.(1) và (4).
D.(2) và (4).
Hiển thị đáp ánĐáp án: C
Giải thích:
(1), (4) có cùng phương trình ion thu gọn là Ca2++CO32−→CaCO3↓
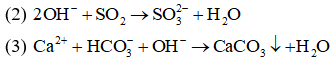
Câu10:Phản ứng nào dưới đây là phản ứng trao đổi ion trong dung dịch?
A.Zn + H2SO4 ZnSO4+ H2
B.Fe(NO3)3+ 3NaOH Fe(OH)3+ 3NaNO3
C.2Fe(NO3)3+ 2KI 2Fe(NO3)2+ I2+ 2KNO3
D.Zn + 2Fe(NO3)3 Zn(NO3)2+ 2Fe(NO3)2
Hiển thị đáp ánĐáp án: B
Giải thích:
A, C, D là phản ứng oxi hóa khử
B là phản ứng trao đổi ion trong dung dịch:
Fe3++3OH−→Fe(OH)3↓
Xem thêm các bài tổng hợp lý thuyết Hóa học lớp 11 đầy đủ, chi tiết khác:
Lý thuyết Bài 5: Luyện tập: Axit, bazơ và muối. Phản ứng trao đổi ion trong dung dịch các chất điện li
Lý thuyết Bài 7: Nito
Lý thuyết Bài 8: Amoniac và muối amoni
Lý thuyết Bài 9: Axit nitric và muối nitrat
Lý thuyết Bài 10: Photpho
Từ khóa » Hóa Học 11 Bài 4 Lý Thuyết
-
Bài 4. Phản ứng Trao đổi Ion Trong Dung Dịch Các Chất điện Li
-
Hoá Học 11 Bài 4: Phản ứng Trao đổi Ion Trong Dung ...
-
Hóa 11 Bài 4: Phản ứng Trao đổi Ion Trong Dung Dịch Các Chất điện Li
-
Bài 4: Phản ứng Trao đổi Ion Trong Dung Dịch Các Chất điện Li
-
Hoá Học 11 Bài 4: Phản ứng Trao đổi Ion Trong Dung Dịch ...
-
Phản ứng Trao đổi Ion Trong Dung Dịch Các Chất điện Li - TaiLieu.VN
-
Bài 4: Phản ứng Trao đổi Trong Dung Dịch Các Chất điện Li - Hoc24
-
Hóa Học 11 - Bài 4 - Phản ứng Trao đổi Ion Trong Dung Dịch Chất điện ...
-
Giải Hóa Bài 4: Phản ứng Trao đổi Ion Trong Dung Dịch Các Chất điện Li
-
Hóa Học 11 Bài 4
-
Bài 4. Phản ứng Trao đổi Ion Trong Dung Dịch Các Chất điện Li
-
Giáo án Hóa Học 11 - Bài 4: Phản ứng Trao đổi Ion Trong Dung Dịch ...
-
Hóa Lớp 11 Bài 4: Phản ứng Trao đổi Ion Trong Dung Dịch Các Chất ...
-
Hóa Học 11 – Bài 4 – Phản ứng Trao đổi Ion Trong Dung Dịch Chất ...