Nhúng 1 Lá Al Vào Dung Dịch CuSO4 . Sau Phản ứng Lấy Al ... - Hoc24
Có thể bạn quan tâm
HOC24
Lớp học Học bài Hỏi bài Giải bài tập Đề thi ĐGNL Khóa học Tin tức Cuộc thi vui Khen thưởng- Tìm kiếm câu trả lời Tìm kiếm câu trả lời cho câu hỏi của bạn
Lớp học
- Lớp 12
- Lớp 11
- Lớp 10
- Lớp 9
- Lớp 8
- Lớp 7
- Lớp 6
- Lớp 5
- Lớp 4
- Lớp 3
- Lớp 2
- Lớp 1
Môn học
- Toán
- Vật lý
- Hóa học
- Sinh học
- Ngữ văn
- Tiếng anh
- Lịch sử
- Địa lý
- Tin học
- Công nghệ
- Giáo dục công dân
- Tiếng anh thí điểm
- Đạo đức
- Tự nhiên và xã hội
- Khoa học
- Lịch sử và Địa lý
- Tiếng việt
- Khoa học tự nhiên
- Hoạt động trải nghiệm, hướng nghiệp
- Hoạt động trải nghiệm sáng tạo
Chủ đề / Chương
Bài học
HOC24
 Khách vãng lai Đăng nhập Đăng ký Khám phá Hỏi đáp Khóa học Đề thi Tin tức Cuộc thi vui Khen thưởng
Khách vãng lai Đăng nhập Đăng ký Khám phá Hỏi đáp Khóa học Đề thi Tin tức Cuộc thi vui Khen thưởng - Tất cả
- Toán
- Vật lý
- Hóa học
- Sinh học
- Ngữ văn
- Tiếng anh
- Lịch sử
- Địa lý
- Tin học
- Công nghệ
- Giáo dục công dân
- Tiếng anh thí điểm
Câu hỏi
Hủy Xác nhận phù hợp Chọn lớp Tất cả Lớp 12 Lớp 11 Lớp 10 Lớp 9 Lớp 8 Lớp 7 Lớp 6 Lớp 5 Lớp 4 Lớp 3 Lớp 2 Lớp 1 Môn học Toán Vật lý Hóa học Sinh học Ngữ văn Tiếng anh Lịch sử Địa lý Tin học Công nghệ Giáo dục công dân Tiếng anh thí điểm Đạo đức Tự nhiên và xã hội Khoa học Lịch sử và Địa lý Tiếng việt Khoa học tự nhiên Hoạt động trải nghiệm, hướng nghiệp Hoạt động trải nghiệm sáng tạo Mới nhất Mới nhất Chưa trả lời Câu hỏi hay
- Võ Khánh Lê
nhúng 1 lá Al vào dung dịch CuSO4 . Sau phản ứng lấy Al ra thấy khối lượng nhẹ đi 1,38g. Tính khối lượng Al đã phản ứng
Xem chi tiết Lớp 0 Hóa học 2 0
 Gửi Hủy
Gửi Hủy 
- Dangtheanh
bie
Đúng 0 Bình luận (0)
- Nguyễn Thị Minh Nguyệt
2Al + 3CuSO4 \(\rightarrow\) Al2(SO4)3 + 3Cu
m dd giảm= 3 . 64 - 2 . 27 = 138 (g)
Cứ 2 mol Al pư thì khối lượng dd giảm 138 g
Vậy 0,02 mol <---------------------------- 1,38 g
mAl pư= 0,02 . 27 = 0,54 (g)
Đúng 2 Bình luận (1)
- Nguyễn Hoàng Nam
Nhúng một lá nhôm vào dung dịch CuSO 4 . Sau một thời gian, lấy lá nhôm ra khỏi dung dịch thì thấy khối lượng dung dịch giảm 1,38 gám. Khối lượng của Al đã tham gia phản ứng là
A. 0,27 gam ; B. 0,81 gam ; C. 0,54 gam ; D. 1,08 gam.
Xem chi tiết Lớp 9 Hóa học 1 0 Gửi Hủy
Gửi Hủy 
- Ngô Quang Sinh
-
Đáp án C.
Gọi khối lượng miếng Al là a gam, lượng nhôm đã phản ứng là x gam :
2Al + 3 CuSO 4 → Al 2 SO 4 3 + 3 Cu
Gọi x là khối lượng Al phản ứng.
![]()
So với khối lượng miếng Al ban đầu thì khối lượng miếng Al sau phản ứng tăng 1,38 gam.
Đúng 0 Bình luận (0)
- Nguyễn Thị Thúy Hiền
Nhúng 1 lá Al vào dung dịch CuSO4 . Sau phản ứng lấy lá Al ra thấy khối lượng dung dịch nhẹ đi 1,38g. Tính khối lượng Al đã phản ứng
HELP ME!!!![]()
![]()
 Gửi Hủy
Gửi Hủy 
- Hoàng Tuấn Đăng
Lời giải:
PTHH: 2Al + 3CuSO4 ==> Al2(SO4)3 + 3Cu
Đặt số mol Al phản ứng là a (mol)
Theo PTHH, nCu = 1,5a (mol)
=> mCu = 96a (gam)
Ta có: mdung dịch giảm = mCu - mAl = \(96a-27a=1,38\)
Giải phương trình, ta được \(a=0,02\left(mol\right)\)
=> Khối lượng nhôm phản ứng: mAl = \(0,02\cdot27=0,54\left(gam\right)\)
Đúng 0 Bình luận (0)
- Nguyễn Minh Tiệp
Hòa tan 11,2g Fe vào 200ml dung dịch CuSO4. Sau một thời gian lấy lá sắt ra, rửa nhẹ, lau khô và đem cân thấy khối lượng kim loại tăng 0,8g. Tính khối lượng Fe đã tham gia phản ứng và khối lượng Cu sinh ra sau phản ứng?
Xem chi tiết Lớp 8 Hóa học 1 0 Gửi Hủy
Gửi Hủy 
- 𝓓𝓾𝔂 𝓐𝓷𝓱
-
PTHH: \(Fe+CuSO_4\rightarrow FeSO_4+Cu\)
Đặt \(n_{Fe\left(phản.ứng\right)}=x\left(mol\right)=n_{Cu\left(tạo.ra\right)}\)
\(\Rightarrow64x-56x=0,8\) \(\Rightarrow x=0,1\) \(\Rightarrow\left\{{}\begin{matrix}m_{Fe\left(phản.ứng\right)}=0,1\cdot56=5,6\left(g\right)\\m_{Cu\left(tạo.ra\right)}=0,1\cdot64=6,4\left(g\right)\end{matrix}\right.\)
Đúng 1 Bình luận (0)
- Muối Hóa Học
Đề bài: Nhúng thanh nhôm Al vào dung dịch CuSO4, sau một thời gian lấy thanh Al ra cân nặng thấy khối lượng giảm 2,07g.
a) Viết PTHH
b) Tính mAl phản ứng
c) Tính mmuối tạo thành
Cảm ơn nhé !!!
Xem chi tiết Lớp 8 Hóa học 2 1 Gửi Hủy
Gửi Hủy 
- hnamyuh
-
a)
$2Al + 3CuSO_4 \to Al_2(SO_4)_3 + 3Cu$
b)
Gọi $n_{Al\ pư} = a(mol)$
Theo PTHH : $n_{Cu} = \dfrac{3}{2}n_{Al\ pư} = 1,5a(mol)$
Ta có :
$64.1,5a - 27a = 2,07 \Rightarrow a = 0,03(mol)$$m_{Al} = 0,03.27 = 0,81(gam)$
c)
$n_{CuSO_4} = n_{Cu} = 1,5a = 0,045(mol)$$m_{CuSO_4} = 0,045.160 = 7,2(gam)$
Đúng 0 Bình luận (1)
- Thảo Phương CTVVIP
-
\(2Al+3CuSO_4\rightarrow Al_2\left(SO_4\right)_3+3Cu\)
Gọi x là số mol Al phản ứng, ta có :
\(m_{KLgiam}=m_{Cu}-m_{Al}=64.\dfrac{3}{2}x-27x=2,07\)
=>x=0,03 (mol)
=> \(m_{Al}=0,03.27=0,81\left(g\right)\)
\(n_{muối}=\dfrac{1}{2}n_{Al}=0,015\left(mol\right)\)
=> \(m_{muối}=0,015.342=5,13\left(g\right)\)
Đúng 2 Bình luận (0)
- Milk___
Cho 333g hh: \(MgSO_4;CuSO_4;BaSO_4\) vào nước thu được dung dịch D và 1 phần không tan C có khối lượng 233g. Nhúng thanh Al vào dung dịch D sau phản ứng nhấc thanh Al ra khỏi dung dịch, làm sạch, sấy khô, thấy khối lượng thanh Al tăng 11,5g
a) Viết pt
b) Tính khối lượng mỗi muối trong hỗn hợp ban đầu
Xem chi tiết Lớp 9 Hóa học 1 0 Gửi Hủy
Gửi Hủy 
- Như Quỳnh
-
\(MgSO_4;CuSO_4;BaSO_4+H_2O\)
\(\Rightarrow\) Dung dịch D gồm \(MgSO_4;CuSO_4\)
\(\Rightarrow\) Phần không tan là \(BaSO_4\)\(\Leftrightarrow m_{BaSO_4}=233\left(g\right)\)
Vậy \(m_{MgSO_4;CuSO_4}=m_{hh}-m_{BaSO_4}=333-233=100\left(g\right)\)
\(3CuSO_4+2Al\rightarrow Al_2\left(SO_4\right)_3+3Cu\)
TĐB: 1,5x x 1,5x (mol)
Gọi x là số mol của Al
\(m\) khối lượng tăng= \(m_{Cu}-m_{Al}\)
\(\Leftrightarrow11,5=1,5x.64-27x\)
\(\Leftrightarrow11,5=96x-27x\)
\(\Leftrightarrow11,5=69x\)
\(\Leftrightarrow x=\dfrac{1}{6}\left(mol\right)\)
\(m_{CuSO_4}=n.M=1,5x.160=1,5.\dfrac{1}{6}.160=40\left(g\right)\)
\(m_{MgSO_4}=m_{MgSO_4;CuSO_4}-m_{CuSO_4}=100-40=60\left(g\right)\)
Đúng 2 Bình luận (0)
- Khanh Linh
 Gửi Hủy
Gửi Hủy 
- Minh Nguyệt
\(V_{H_2}\)= \(\dfrac{V}{22,4}=\dfrac{6,72}{22,4}=0,3mol\)PTHH: 2Al+6HCL→2AlCl3+3H2a)Theo pt: \(n_{Al_{ }}=\dfrac{2}{3}n_{H_2}=\dfrac{2}{3}.0,3=0,2mol\)⇒ mAl=n.M=0,2.27=5,4gb)Theo pt:\(n_{HCl}=\dfrac{6}{2}n_{H_2}=\dfrac{6}{2}.0,3=0,9mol\)⇒mHCl=n.M=0,9.36.5=32,85g
Đúng 1 Bình luận (0)
- Nguyễn Duy
Nhúng 1 lá nhôm vào dd 200ml CuSO4 . Sau một thời gian lấy lá nhôm ra khỏi dd làm khô rồi cân thì thấy khối lượng lá nhôm tăng 1,38g
a) Tính khối lượng đồng tạo thành
b) Tính nồng độ mol CuSO4 đã phản ứng
Xem chi tiết Lớp 9 Hóa học 2 0 Gửi Hủy
Gửi Hủy 
- Nguyễn Hoàng Minh
-
\(a,\) Đặt \(n_{CuSO_4}=x(mol)\)
\(PTHH:2Al+3CuSO_4\to Al_2(SO_4)_3+3Cu\\ \dfrac{2}{3}x.....x......\dfrac{1}{3}x.....x(mol)\\ \Rightarrow \Delta m_{Al\uparrow}=m_{Cu}-m_{Al}=64x-\dfrac{2}{3}.27x=1,38\\ \Rightarrow x=0,03\\ \Rightarrow m_{Cu}=0,03.64=1,92(g)\\ b,n_{CuSO_4}=0,03(mol)\\ \Rightarrow C_{M_{CuSO_4}}=\dfrac{0,03}{0,2}=0,15M\)
Đúng 0 Bình luận (0)
- Lê Thị Mộng Du
Gọi khối lượng Al ban đầu là a gam khối lượng Al pư là x gamPTHH: 2Al+3CuSO4→Al2(SO4)3+3Cua, vì khối lượng của nhôm sau pư tăng 1,38g, nên ta có PT:(a-x) + 192x/54 = a + 1,38⇒ x= 0,54 ⇒ a= 0,54 + 1,38 = 1,92gb, nAl=0,54/27 = 0,02 mol theo PTHH có nCuSO4=2/3 .nAl = 0,03 mol⇒CMCuSO4=0,03/0,2=0,15MChúc bạn học tốt nha!
Đúng 0 Bình luận (0)

- Nguyễn Hoàng Nam
Cho 86 gam hỗn hợp X gồm x mol Fe3O4, (1,05 – 4x) mol FeO, Fe(NO3)2 và Mg tan hết trong 1540 ml dung dịch H2SO4 1M. Sau phản ứng thu được dung dịch Y (chỉ chứa các muối trung hòa) và 0,04 mol N2. Cho KOH dư vào dung dịch Y rồi đun nóng nhẹ thấy số mol KOH phản ứng tối đa là 3,15 mol và có m gam kết tủa xuất hiện. Mặt khác, nhúng thanh Al vào Y sau khi các phản ứng xảy ra hoàn toàn nhấc thanh Al ra cân lại thấy khối lượng tăng 28 gam (kim loại Fe sinh ra bám hết vào thanh Al). Phần trăm khối lượng của Mg trong X gần nhất với?
A. 6,2%
B. 5,2%
C. 4,2%
D. 7,2%
Xem chi tiết Lớp 12 Hóa học 1 0 Gửi Hủy
Gửi Hủy 
- Ngô Quang Sinh
-
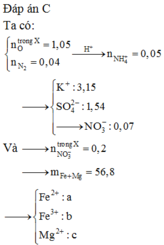
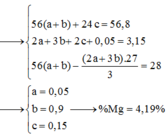

- Dieu Anh
nhúng một lá nhôm vào dung dịch CuSO4 . sau một thời gian lấy lá nhôm ra khỏi dd thấy khối lượng nhôm tăng 1,38g a) tính khối lượng nhôm pứ b) khối lượng đồng sunfat tham gia pứ
Xem chi tiết Lớp 9 Hóa học 1 0 Gửi Hủy
Gửi Hủy 
- Buddy
-
Phương trình phản ứng:
2Al + 3CuSO4 --> Al2(SO4)3 + 3Cu
Cứ 2 mol Al thì dung dịch giảm 3.64 - 2.27 = 138 gam
x mol Al thì dung dịch giảm 1,38 gam
Số mol Al tham gia phản ứng là: (1,38 . 2)/138 = 0,02 (gam)
Khối lượng Al là: m = 0,02 . 27 = 0,54 gam
Đúng 0 Bình luận (0)Từ khóa » Cho Al Vào Dung Dịch Cuso4
-
Hiện Tượng Khi Cho Al + CuSO4 Là Gì? - Tuấn Huy
-
Hiện Tượng Xảy Ra Khi Cho Al Vào ống Nghiệm Chứa Dung Dịch CuSO4
-
Tiến Hành Các Thí Nghiệm Sau Cho Lá Al Vào Dung Dịch Gồm CuSO4
-
Cho Lá Al Vào Dung Dịch HCl, Có Khí Thoát Ra. Thêm Vài Giọt Dung ...
-
Cho Một Lượng Bột Al Vào Dung Dịch CuSO4 Sau Một Thời Gian Thấy ...
-
Tôi Yêu Hóa Học - Nêu Hiện Tưởng Khi Cho Thanh Al Vào Dung...
-
[LỜI GIẢI] Cho Một Lượng Bột Al Vào Dung Dịch CuSO4 Dư Lấy Rắn ...
-
Nhúng 1 Lá Al Vào Dung Dịch CuSO4 . Sau Phản ứng Lấy Lá ... - Hoc24
-
Thả Một Mảnh Nhôm Vào ống Nghiệm Chứa Dung Dịch CuSO4 . Xảy ...
-
2Al + 3CuSO4 → Al2(SO4)3 + 3Cu | Phương Trình Phản Ứng Hóa ...
-
Nhúng Một Thanh Nhôm Kim Loại Vào Dung Dịch CuSO4 Thì Hiện ...
-
(a) Cho Al Vào Dung Dịch HNO3 Loãng Nguội (b ... - Bài Giảng 365
-
Kim Loại Al Có Tác Dụng được Với Dung Dịch CuSO4 Không ? Vì Sao ...
-
(a) Cho Al Vào Dung Dịch FeCl3 Dư. (b) Cho Kim Loại Na ...





