PH Wert Von NH4Cl Berechnen? - Gutefrage
Hallo, ich will denkt- Wert berechnen .. muss ich einfach -log(0,2) rechnen oder ist es komplizierter ? 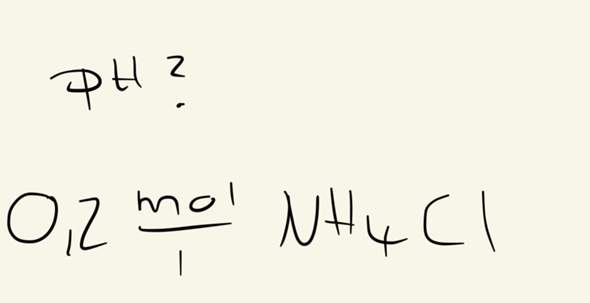
Danke für die Hilfe !
...kompletten Beitrag anzeigen 22.02.2020, 14:47 
Ich habe es mal anders probiert, wäre es so richtig ?
Antworten3 Antworten
MeisterRuelps, UserMod Light Experte Von gutefrage auf Grund seines Wissens auf einem Fachgebiet ausgezeichneter Nutzer Chemie 22.02.2020, 14:35Tipp: Das Ammonium-Kation wird ein Proton abgeben. Daher also den pKs-Wert von diesem zur Hilfe nehmen.
Woher ich das weiß:Studium / Ausbildung – MSc in Biochemie 2 Kommentare 2 Kommentar schreiben… chillzone Beitragsersteller 22.02.2020, 14:48Danke, ich habe es mal anders probiert, kannst du mal kontrollieren ( siehe oben )
MeisterRuelps, UserMod Light 22.02.2020, 14:52 @chillzoneDer pKs-Wert vom Ammoniumkation ist 9,25. Ich habe 4,97 raus ;)
Weitere Kommentare zur Antwort anzeigen Spikeman197 Experte Von gutefrage auf Grund seines Wissens auf einem Fachgebiet ausgezeichneter Nutzer Chemie 22.02.2020, 14:36komplizierter!
Es ist ja keine starke Säure, sondern ein saures Salz!
Man braucht den pKs des Kations und eine andere Formel!
verreisterNutzer 22.02.2020, 14:35Hier kannst nicht einfach die Definition des pH Werts der starken Säure nehmen sondern die Henderson Hasselbalch Gleichung
pH = 1/2 (pKs - lg c0)
Weil die Lösung als schwache Säure reagiert
Hcl=starke Säure
Ammoniak ist eine Schwache Base
8 Kommentare 8 Kommentar schreiben… Spikeman197 22.02.2020, 14:38Richtiger Weg, aber als HH Gleichung bezeichnet man die Puffergleichung!
verreisterNutzer 22.02.2020, 14:40 @Spikeman197Dachte das beide Gleichungen so heißen weil sie voneinander abgeleitet sind
Hat den diese Gleichung auch einen Namen?
Spikeman197 22.02.2020, 14:46 @verreisterNutzerAlso ich kenne keinen! Für mich ist das einfach die Gleichung für saure Salzlösungen.
Abstammen tun die alle vom MWG und der Autoprotolyse von Wasser.
Nicht jede Gleichung wird da gleich nach ihrem Entdeckter beannnt.
chillzone Beitragsersteller 22.02.2020, 14:48Ich habs mal mit der Gleichnung probiert, kannst du mal gucken ob ich’s richtig gemacht habe ? ( siehe oben )
verreisterNutzer 22.02.2020, 14:52 @chillzoneWenn du den pks Wert richtig ausgerechnet hast ist dein pH Wert auch richtig
Spikeman197 22.02.2020, 14:54 @chillzoneEmm, nein...Die Umrechnjng von Kb auf pKb ist falsch!
Der ist für pKs(NH4+/NH3) = 9,24!
verreisterNutzer 22.02.2020, 15:11 @Spikeman197Das stimmt natürlich auch wollte aber sagen das die Gleichung richtig verwendet worden ist
verreisterNutzer 22.02.2020, 15:18 @verreisterNutzerAber das richtige Ergebnis ist sowieso 4.97448500217 für den pH Aber der Fragesteller kommt wegen dem falschen pKs Wert nicht darauf
Weitere Kommentare zur Antwort anzeigen Weitere Antworten zeigenÄhnliche Beiträge
Wie berechnet man sich den pH-Wert einer NH4Cl Lösung?
Ich muss den pH-Wert berechnen und habe gegeben:
die Massenkonzentration der Lösung: 3,74g/L
molare Masse von NH4Cl: 53
Ks der Essigsäure: 1,6*10^-5
pKb-Wert von NH3: 4,796.
Welche Formel verwende ich für die Berechnung des pH-Wertes?
...zum BeitragPKs Wert berechnen (Säuren und Basen_Chemie?
Hallo, wie berechne ich den pKs Wert aus? Angegeben ist der pH-Wert einer schwachen Säure pH= 3 und c0= 0,2 [mol/l]
Danke im Voraus :)))
...zum BeitragpH Wert einer Mischung berechnen?
Hallo, ich weiß, dass es so eine ähnliche Frage schonmal gab, aber ich konnte mit den Antworten leider nicht viel anfangen. Daher hoffe ich, dass mir jemand helfen kann.
Ich soll den pH wert einer Mischung von 50ml einer 1 molaren Ammoniaklösung und 50ml einer 1,2 molaren Ammoniumchlorid(NH4Cl) berechnen. der pKb von NH3=4,76.
...zum BeitragpH Wert, PKs und PKb?
Hallo die folgende Aufgabe bereitet mir sehr schwere Kopfschmerzen! Bitte dringend um Hilfe.
Berechnen Sie den pH-Wert folgender Lösungen mit den Stoffmengenkonzentrationen c = 0,1M
Starke Säuren Ph= -log (HA)
1. Salzsäure (pKs= -6)
2. Schwefelsäure (pKs= -3)
Schwache säure PH= ½ (PKs-log {HA})
3. Essigsäure (pKs= 4,75)
Starke Basen Poh= -log{BA}
4. Natronlauge NaOH
(pKb= 0)
5. Ammomiak (pKb= 4,75)
...zum BeitragpH-Wert berechnen?
Berechnen Sie die pH-Werte folgender Salzlösungen: NH4Cl (𝑐 = 0,3 mol/L) und CH3COONa (𝑐 = 0,1 mol/L); für NH + 4 gilt p𝐾S = 9,26, für CH3COOH gilt p𝐾S = 4,74.
...zum BeitragWie berechne ich den pH-Wert einer Mischung aus schwache Säure und starke Base?
Hallo!
Ich habe ein Problem bei einer Aufgabe zur Berechnung des pH-Wertes eines Säure/Base Gemisches.
100 ml 0,1 mol/l Ameisensäure werden in 30 ml 0,2 mol/l NaOH gegeben. Nun soll ich den pH wert berechnen und sagen ob es sich um ein Puffersystem handelt. Es gibt keine weiteren Angaben danke für eure Hilfe.
...zum BeitragpH-Wert von NH4Cl und NaOH?
Hey ich soll bei der mischlösung von 50 ml NH4Cl mit 50 ml NaOh den ph-Wert bereich, also alkalisch, neutral oder sauer , sagen. Ich dachte jetzt das die lösung im alkalischen Bereich liegt da OH- ja eine starke Base ist. Oder lieg ich da falsch
...zum BeitragPH Wert Puffersystem Aufgabe?
Welcher PH Wert ergibt sich bei 0,2 mol je HPO4-2 (Hydrogenphosphat) und H2PO4- (Dihydrogenphosphat), wenn dies in 1,4 l Wasser gelöst wird.
Ich habe bisher:
V = 1,4 l
n = 0,2 mol je
Pufferoptimum pKs Wert = 7,21
c = n/V also 0,2 mol/ 1,4 l = 0,143 mol/l
Das in die Henderson Hasselbalch Gleichung einsetzen
pH = 7,21 + log(1) = 7,21
Das kann ja irgendwie nicht sein, was habe ich falsch gemacht
...zum BeitragWie berechnet man hier den pH-Wert?
Wenn z.B Salzsäure eine Konzentration von 10 mol/L hat, wie findet man den pH-Wert heraus? Weil normalerweise macht man ja -log(c), aber das wäre ja hier -1, was nicht als pH-Wert sein kann. Wie kann man das berechnen?
...zum BeitragpH und pOH Unterschied?
Servus, was ist hier der Unterschied?
Mir ist bewusst, dass ph + POH = 14 ist. Den PH Wert berechne ich mit der Konzentration von mol/L. -log(10^-2) wenn Konzentration 0,01 mol/L
...zum BeitragpH-Werte bei schwachen Basen berechnen?
Hey hoo👋🏾 Ich hoffe ihr habt heute schon "gebrückt". Bei mir ging der Brückentag leider für's Lernen auf die Praktikumsklausur drauf - wobei eine Aufgabe mir jetzt gerade besonders viel Zeit raubt
"Bestimmen SIe die pH-Werte folgender wässriger Lsöungen. Begründen SI eihre Vorgehensweise!".
- 1,6 molare NH4CL-Lösung. (pKB (NH3) = 4,74)
Lösung: 14 - 4,74 = 9,26
=> pH = 1/2 (9,26 - log (1,6)) = 4,53
- 0,8 M NH3 (pKB (NH3) = 4,74)
Lösung: pOH = 1/2 (pKB - lg c (OH-)= 1/2 (4,74 - lg 0,8 mol/L)= 2,42
=> pH = 14 - 2,42= 11,58
-------------------------------------------------------------------Das triggert mich gerade so hart.
Bei der ersten Aufgabe wird einfach als Formel genommen:
pH = 1/2 (pKs - log co) = 1/2 (9,26 - log (1,6)) = 4,53
Also es wird einfach der pKB-Wert von 14 substrahiert, und dann mit dem pKS = 9,26 weitergerechnet.
Bei der zweiten Aufgabe wird direkt mit dem pKB-Wert gerechnet.
pH 1/2 (pKB - lg c(OH-) = 1/2 (4,74 - log (0,8 mol/L) = 2,42Und das dann von 14 substrahiert.
Aber wir haben es doch bei beiden Aufgaben mit der schwachen Base NH3 zu tun.
Wenn ich die Formel aus der ersten Aufgabe für die zweite annehme, wäre es:
pH = 1/2 (pKs - log co) = 1/2 (9,26 - log (0,8)) = 4,67... Aber das ist anscheinden falsch.
Hat es damit zu tun, daß bei der ersten Aufgabe an NH3 noch die starke Säure HCl dranklebt und man deswegen die Formel für starke Säuren nehmen muß?
Ich hatte mir jetzt folgende Formel zurechtglegt....
starke Säure: pH = - log cschwache SÄure: pH = 1/2 (pKS - log co)schwache Base: pOH = 1/2 (pKB - log co) und dann 14 - poHstarke Base: poH = - log (c) und dann 14 - poH
und für die Konzentrationen:starke Säure: 10 ^-pHschwache Säure: 10^(pKS/2pH)schwache Base 10^(pKB/2poH)starke Base: 10^-pOH
Aber irgendwie stolper ich immer wieder über so Ausnahmefälle...
in einer anderen Aufgabe soll der PH-Wert von 2 M CH3COOK bestimmt werden (mit PKS Essigsäure = 4,75).Ich hätte jetzt gedacht, CH3COOK ist eine schwache Base , also pKB = 14 - 4,75 = 9,25. Dann pOH = 1/2 (pKB - log co) und dann 14 - poH=> pOH = 1/2 (9,25 - log 2) = 4,48 und dann 14 - 4,48 = 9,52
Aber die Musterlösung rechnet munter mit dem PKS-Wert und substrahiert den von 14, alsopH = 14 - 1/2 (4,75 - log (2 mol/L)= 11,78
Und das belastet mich...Wie berechnet man also den PH-Wert bei schwachen Basen? Warum wird für 1,6 M NH4Cl und 0,8 M NH3 und 2 M CH3COOK jeweils unterschiedliche Formeln verwendet und warum gilt meine Formel "schwache Base: pOH = 1/2 (pKB - log co) und dann 14 - poH" hier nicht.
LG und ein schönes verlängertes Restwochenende!.
...zum BeitragMolarität,Normalität und pH-Wert?
Also nachdem ich nun lange rumprobiert habe versuche ich es mal hier.
Meine Aufgabe ist: Welchen pH-Wert besitzt eine
a) 0.01 N HCl
b) 0.1 N CH3COOH (Ks=10^-5)
c) 0.01 N H2SO4
d) 0.1 N NH4Cl (Kb= 10^-5)
also, ich habe herausgefunden, dass bei einer 0.1 N HCl die Molarität ebenfalls 0.1 ist, da diese nur ein Proton abgeben kann. Bei einer CH3COOH soll dies ebenfalls so sein. bei einer H2SO4 ist 0.01 N = 0.02 M? Und bei einer NH4Cl habe ich leider nichts dazu herausgefunden.
Ich habe wie folgt gerechnet:
a) 0.01 N HCl = 0.01 M HCl
pH = - lg([H3O+]) = - lg(0.01) = 2
b) 0.1 N CH3COOH = 0.1 M CH3COOH
pH=1/2 (pKs - lg ([H3O+]) = 1/2 (10^-5 - lg(0.1) = 3
c) ?? Also diese Aufgabe habe ich für 0.01 M berechnet. Wie läuft das als 0.01 N ? Ich frage, weil diese Säure ja doppelt Dissoziiert und damit ist die Formel :
pH = -lg ([ks1 + ks2]) , wenn es jetzt eine 0.01 N H2SO4 ist, verändern sich dann die beiden ks-Werte?
d) ?? Hier weiß ich leider auch gar nicht weiter. also die Formel wäre ja
pKb = - log (Kb) = - lg (10^-5) = 5 -> pKs= 14 - pKb = 9
pH = 1/2 (pKs - lg ([NH4Cl])
Es wäre wirklich nett, wenn sich jemand dieser Frage annehmen könnte und mir genau erklären würde, was ich tun muss um den pH-Wert zu berechnen.
Danke schon mal!
...zum BeitragpH-Wert berechnen einer Pufferlösung?
Berechnen Sie den pH-Wert einer Pufferlösung aus 2 Litern einer 0,1 molaren Essigsäure, in die Sie 2 Gramm Natriumhydroxid gegeben haben!
Jetzt habe ich M(NaOH)= 39,0 g/mol ; n(NaOH)=0,051mol
n(CH3COOH)=0,2
pH= 4,75- lg( 0,2 / 0,051) = 4,16
Ist das so richtig?
...zum BeitragWieso benutzt man minus log (ph wert)?
Wieso benutzt man den negativen Logarithmus wenn man den ph wert berechnen möchte?
...zum Beitrag Was möchtest Du wissen? Deine Frage stellen
Was möchtest Du wissen? Deine Frage stellen Từ khóa » Nh4cl Ph Wert
-
Ammoniumchlorid
-
Ammoniumchlorid – BS-Wiki: Wissen Teilen
-
Ammoniumchlorid - Seilnacht
-
Ammoniumchlorid - Wikipedia
-
Berechnen Sie Den PH-Wert Einer 1M Ammoniumchlorid-Lösung ...
-
Mischverhältnis PH-Wert Ammoniak/Ammoniumchlorid
-
NH 4 Cl-Lösung Mit Ammoniak-Zugabe - Aqion
-
Ammoniumpuffer
-
Ammoniak-Pufferlösung, Ammoniumchlorid/Ammoniak, PH-Wert 10 ...
-
Berechnung Der PH-Werte Von Lösungen Schwacher Säure/Base ...
-
Effekte Einer Natriumchlorid- Oder Ammoniumchlorid
-
[PDF] Säure-Base-Reaktionen
-
[PDF] Laboratorium (WS 2010/11), Stichpunkte Zur Lösung 15.01.