Ozon – Wikipedia Tiếng Việt
Có thể bạn quan tâm
Nội dung
chuyển sang thanh bên ẩn- Đầu
- Bài viết
- Thảo luận
- Đọc
- Sửa đổi
- Sửa mã nguồn
- Xem lịch sử
- Đọc
- Sửa đổi
- Sửa mã nguồn
- Xem lịch sử
- Các liên kết đến đây
- Thay đổi liên quan
- Liên kết thường trực
- Thông tin trang
- Trích dẫn trang này
- Tạo URL rút gọn
- Tải mã QR
- Tạo một quyển sách
- Tải dưới dạng PDF
- Bản để in ra
- Wikimedia Commons
- Khoản mục Wikidata
| Bài viết này cần thêm chú thích nguồn gốc để kiểm chứng thông tin. Mời bạn giúp hoàn thiện bài viết này bằng cách bổ sung chú thích tới các nguồn đáng tin cậy. Các nội dung không có nguồn có thể bị nghi ngờ và xóa bỏ. (Tìm hiểu cách thức và thời điểm xóa thông báo này) |
| Ozone | |||
|---|---|---|---|
| |||
 | |||
| Danh pháp IUPAC | Ozone | ||
| Tên hệ thống | Trioxygen | ||
| Tên khác | 2λ4-trioxidiene; catena-trioxygen | ||
| Nhận dạng | |||
| Số CAS | 10028-15-6 | ||
| PubChem | 24823 | ||
| Số EINECS | 233–069–2 | ||
| MeSH | Ozone | ||
| ChEBI | 25812 | ||
| Số RTECS | RS8225000 | ||
| Ảnh Jmol-3D | ảnh | ||
| SMILES | đầy đủ
| ||
| InChI | đầy đủ
| ||
| Tham chiếu Gmelin | 1101 | ||
| UNII | 66H7ZZK23N | ||
| Thuộc tính | |||
| Công thức phân tử | O3 | ||
| Bề ngoài | Từ không màu đến xanh nhạt[1] | ||
| Mùi | Hăng[1] | ||
| Khối lượng riêng | 2.144 mg cm−3 (at 0 °C) | ||
| Điểm nóng chảy | −192,2 °C; 81,0 K; −313,9 °F | ||
| Điểm sôi | −112 °C; 161 K; −170 °F | ||
| Độ hòa tan trong nước | 1.05 g L−1 (at 0 °C) | ||
| Độ hòa tan trong dung môi khác | Tan nhiều trong CCl4, H2SO4 | ||
| Áp suất hơi | 55.7 atm[2] (Lỗi Lua trong Mô_đun:Convert tại dòng 328: attempt to compare number with nil.)[a] | ||
| MagSus | +6.7·10−6 cm³/mol | ||
| Chiết suất (nD) | 1.2226 (lỏng), 1.00052 (khí, STP, 546 nm—độ phân tán cao)[3] | ||
| Cấu trúc | |||
| Nhóm không gian | C2v | ||
| Tọa độ | Digonal | ||
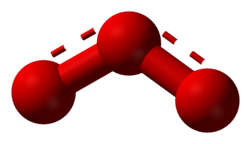
| Hình dạng phân tử | Lưỡng diện | ||
| Lai hóa quỹ đạo | sp2 for O1 | ||
| Mômen lưỡng cực | 0.53 D | ||
| Nhiệt hóa học | |||
| Enthalpyhình thành ΔfHo298 | 142.67 kJ mol−1 | ||
| Entropy mol tiêu chuẩn So298 | 238.92 J K−1 mol−1 | ||
| Các nguy hiểm | |||
| NFPA 704 |
| ||
| PEL | TWA 0.1 ppm (0.2 mg/m³)[1] | ||
| REL | C 0.1 ppm (0.2 mg/m³)[1] | ||
| IDLH | 5 ppm[1] | ||
| Ký hiệu GHS |      | ||
| Báo hiệu GHS | Nguy hiểm | ||
| Chỉ dẫn nguy hiểm GHS | H270, H314 | ||
| Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |||
Ozon (O3) là một phân tử chất vô cơ với công thức hóa học O3. Nó là một chất khí màu xanh lam nhạt, có mùi hăng đặc trưng. Nó là một dạng thù hình của oxy kém bền hơn nhiều so với dạng nguyên tử O2, bị phá vỡ trong bầu khí quyển thấp hơn thành O2 (đioxy). Ozon được hình thành từ đioxy do tác động của tia cực tím (UV) và phóng điện trong bầu khí quyển Trái Đất. Nó hiện diện với nồng độ rất thấp trong suốt tầng sau, với nồng độ cao nhất ở tầng ozon của tầng bình lưu, nơi hấp thụ hầu hết bức xạ cực tím (UV) của Mặt Trời.
Mùi của ozon gợi nhớ đến clo và nhiều người có thể phát hiện được ozon ở nồng độ nhỏ nhất là 0,1 ppm trong không khí. Cấu trúc O3 của ozon được xác định vào năm 1865. Phân tử này sau đó đã được chứng minh là có cấu trúc uốn cong và thuận từ yếu. Ở điều kiện tiêu chuẩn, ozon là một chất khí màu xanh lam nhạt, ngưng tụ ở nhiệt độ lạnh thành chất lỏng màu xanh lam đậm và cuối cùng là chất rắn màu tím đen. Tính không ổn định của ozon đối với đioxy phổ biến hơn là cả khí đặc và ozon lỏng có thể bị phân hủy bùng nổ ở nhiệt độ cao hoặc nóng lên nhanh đến điểm sôi.[4] Do đó nó chỉ được sử dụng cho mục đích thương mại với nồng độ thấp.
Ozon là một chất oxy hóa mạnh (hơn nhiều so với oxy) và có nhiều ứng dụng trong công nghiệp và tiêu dùng liên quan đến quá trình oxy hóa. Tuy nhiên, cùng một tiềm năng oxy hóa cao này lại gây ra ozon phá hủy các mô niêm mạc và hô hấp ở động vật và cả các mô ở thực vật, trên nồng độ khoảng 0,1 ppm. Trong khi điều này làm cho ozon trở thành một chất gây ô nhiễm và nguy hiểm hô hấp mạnh gần mặt đất, nồng độ cao hơn trong tầng ozon (từ 2 đến 8 ppm) là có lợi, ngăn chặn tia cực tím có hại đến bề mặt Trái đất.
Một số thiết bị điện có thể sản sinh ra ozon mà con người có thể ngửi thấy dễ dàng. Điều này đặc biệt đúng với các thiết bị sử dụng điện cao áp, như ti vi và máy photocopy. Các động cơ điện sử dụng chổi quét cũng có thể sản sinh ozon do sự đánh lửa lặp lại bên trong khối. Các động cơ lớn, ví dụ những chiếc được sử dụng cho máy nâng hay máy bơm thủy lực, sản sinh nhiều ozon hơn các động cơ nhỏ.
Mật độ tập trung cao nhất của ozon trong khí quyển nằm ở tầng bình lưu, khoảng từ giữa 10 và 17 km đến 50 km tính từ mặt đất,[5] trong khu vực được biết đến như là tầng ozon. Tại đây, nó lọc phần lớn các tia cực tím từ Mặt Trời, là tia có thể gây hại cho phần lớn các loại hình sinh vật trên Trái Đất. Phương pháp tiêu chuẩn để đo lượng ozon trong khí quyển là sử dụng đơn vị Dobson (DU). ozon sử dụng trong công nghiệp được đo bằng ppm (ví dụ các giới hạn phơi nắng của OSHA), và phần trăm theo khối lượng hay trọng lượng.
Danh pháp
[sửa | sửa mã nguồn]Tên gọi bình thường ozone là tên IUPAC được sử dụng phổ biến và ưa thích nhất. Các tên có hệ thống 2λ 4-trioxidiene và catena-baxygen, tên IUPAC hợp lệ, được xây dựng theo danh pháp nhóm thế và phụ gia tương ứng. Tên ozone bắt nguồn từ ozein (ὄζειν), động từ tiếng Hy Lạp chỉ mùi, dùng để chỉ mùi đặc biệt của ozon.
Trong các bối cảnh thích hợp, ozon có thể được xem như trioxidan với hai nguyên tử hydro bị loại bỏ, và như vậy, trioxidanylidene có thể được sử dụng như một tên có hệ thống, theo danh pháp thay thế. Theo mặc định, những cái tên này không liên quan đến tính xuyên tâm của phân tử ozon. Trong một ngữ cảnh cụ thể hơn, điều này cũng có thể đặt tên cho trạng thái cơ bản đơn không cực đoan, trong khi trạng thái lưỡng cực được đặt tên là trioxidanediyl.
Trioxidanediyl (hoặc ozonide) được sử dụng một cách không hệ thống để chỉ nhóm thế (-OOO-). Cần cẩn thận để tránh nhầm lẫn tên của nhóm với tên theo ngữ cảnh cụ thể của ozon đã nêu ở trên.
Lịch sử
[sửa | sửa mã nguồn]

Vào năm 1785, nhà hóa học người Hà Lan Martinus van Marum đang tiến hành các thí nghiệm liên quan đến tia lửa điện trên mặt nước thì ông nhận thấy một mùi bất thường, mà ông cho là do phản ứng điện, không nhận ra rằng ông thực sự đã tạo ra ozon.[6]
Nửa thế kỷ sau, Christian Friedrich Schönbein nhận thấy mùi hăng tương tự và nhận ra đó là mùi thường xuất hiện sau một tia chớp. Năm 1839, ông đã thành công trong việc cô lập hóa chất dạng khí và đặt tên nó là "ozôn", từ tiếng Hy Lạp ozein (ὄζειν) nghĩa là "ngửi".[7][8] Vì lý do này, Schönbein thường được ghi nhận là người đã phát hiện ra ozon.[6][9][10][11] Công thức của ozon, O3, không được xác định cho đến năm 1865 bởi Jacques-Louis Soret [12] và được Schönbein xác nhận vào năm 1867.[7][13]
Trong phần lớn nửa sau của thế kỷ 19 và đến cả thế kỷ 20, ozon được các nhà tự nhiên học và những người tìm kiếm sức khỏe coi là một thành phần lành mạnh của môi trường. Beaumont, California lấy khẩu hiệu chính thức của mình là "Beaumont: Zone of Ozone", được minh chứng trên bưu thiếp và giấy tiêu đề của Phòng Thương mại.[14] Các nhà tự nhiên học làm việc ngoài trời thường coi độ cao cao hơn có lợi vì hàm lượng ozon của chúng. Nhà tự nhiên học Henry Henshaw, làm việc tại Hawaii, viết: "Có một bầu khí quyển khá khác biệt [ở độ cao hơn] với lượng ozon đủ để duy trì năng lượng cần thiết [để hoạt động].[15] Không khí ven biển được coi là tốt cho sức khỏe vì hàm lượng ozon được cho là của nó; nhưng mùi gây ra niềm tin này thực chất là mùi của các chất chuyển hóa từ rong biển được halogen hóa.[16]
Phần lớn sự hấp dẫn của ozon dường như đến từ mùi "tươi" của nó, gợi lên các mối liên hệ với đặc tính làm sạch. Tuy nhiên, các nhà khoa học đã ghi nhận tác hại của nó. Năm 1873 James Dewar và John Grey McKendrick đã ghi lại rằng ếch trở nên chậm chạp, chim thở hổn hển và máu của thỏ cho thấy lượng oxy giảm sau khi tiếp xúc với "không khí bị ozon hóa".[9][17] Bản thân Schönbein đã báo cáo rằng những cơn đau tức ngực, kích ứng màng nhầy và khó thở xảy ra do hít phải khí ozon và các động vật có vú nhỏ bị chết.[18] Năm 1911, Leonard Hill và Martin Flack đã tuyên bố trong Kỷ yếu của Hiệp hội Hoàng gia B rằng tác dụng có lợi cho sức khỏe của ozon, " mà chỉ bằng cách lặp đi lặp lại, đã trở thành một phần của niềm tin của công chúng; và cho đến nay bằng chứng sinh lý chính xác ủng hộ tác dụng tốt của nó vẫn còn gần như hoàn toàn chỉ là tưởng tượng. Kiến thức duy nhất được xác minh rõ ràng về tác dụng sinh lý của ozon, cho đến nay, là nó gây kích ứng và phù phổi, và tử vong nếu hít phải ở nồng độ tương đối mạnh bất cứ lúc nào. " [9][19] Trong Chiến tranh thế giới thứ nhất, ozon đã được thử nghiệm tại Bệnh viện Quân đội Queen Alexandra ở London như một chất khử trùng có thể dùng cho vết thương. Khí ozon được sử dụng trực tiếp lên vết thương trong 15 phút. Điều này dẫn đến thiệt hại cho cả tế bào vi khuẩn và mô người. Các kỹ thuật vệ sinh khác, chẳng hạn như tưới ozon cùng với thuốc sát trùng, được cho là thích hợp hơn.[9][20]
Ozon tầng bình lưu
[sửa | sửa mã nguồn]Ozon được biết đến do khả năng hấp thụ bức xạ UV-B. Ozon được tạo thành một cách tự nhiên trong tầng ozon. Sự suy giảm ozon và lỗ thủng ozon diễn ra bởi chlorofluorocarbon (CFC) và các chất gây ô nhiễm khác trong bầu khí quyển.
Ozon trong bầu khí quyển Trái Đất nói chung được tạo thành bởi tia cực tím, nó phá vỡ các phân tử O2, tạo thành oxy nguyên tử. Oxy nguyên tử sau đó kết hợp với phân tử oxy chưa bị phá vỡ để tạo thành O3. Trong một số trường hợp oxy nguyên tử kết hợp với N2 để tạo thành các oxide nitơ; sau đó nó lại bị phá vỡ bởi ánh sáng nhìn thấy để tái tạo ozon.
Khi tia cực tím chiếu vào ozon, nó chia ozon thành phân tử O2 và nguyên tử của oxy nguyên tử, quá trình liên tục này được gọi là chu trình ozon-oxy. Chu trình này có thể bị phá vỡ bởi sự có mặt của các nguyên tử clo, flo hay brom trong khí quyển; các nguyên tố này tìm thấy trong những hợp chất bền vững, đặc biệt là cloroflorocacbon (CFC) là chất có thể thấy ở tầng bình lưu và được giải phóng dưới tác động của tia cực tím.
Chu trình nitơ oxide để tạo thành ozon cũng có thể bị phá vỡ do sự có mặt của hơi nước trong khí quyển vì nó làm biến đổi các oxide nitơ thành các dạng bền vững hơn.
Sử dụng trong công nghiệp
[sửa | sửa mã nguồn]Ozon được sử dụng để tẩy trắng đồ vật và tiêu diệt vi khuẩn. Rất nhiều hệ thống nước sinh hoạt công cộng sử dụng ozon để khử vi khuẩn thay vì sử dụng clo. Ozon không tạo thành các hợp chất hữu cơ chứa clo, nhưng chúng cũng không tồn tại trong nước sau khi xử lý, vì thế một số hệ thống cho thêm một chút ozon vào để ngăn cản sự phát triển của vi khuẩn trong đường ống.
Trong công nghiệp ozon được sử dụng để:
- Khử trùng nước uống trước khi đóng chai,
- Khử các chất gây ô nhiễm có trong nước bằng phương pháp hóa học (sắt, asen, hydro sulfide, nitrit, và các chất hữu cơ phức tạp liên kết với nhau tạo ra "màu" của nước,
- Hỗ trợ trong quá trình kết tụ (là quá trình kết tụ của các phân tử, được sử dụng trong quá trình lọc để loại bỏ sắt và asen),
- Làm sạch và tẩy trắng vải (việc sử dụng để tẩy trắng được cấp bằng sáng chế),
- Hỗ trợ trong gia công chất dẻo (plastic) để cho phép mực kết dính,
- Đánh giá tuổi thọ của mẫu cao su để xác định chu kỳ tuổi thọ của cả lô cao su.
Sử dụng trong y tế
[sửa | sửa mã nguồn]Ozon, cùng với các ion hypoclorit, được sản xuất tự nhiên bởi các tế bào máu trắng (bạch cầu) cũng như rễ của cây cúc vạn thọ như là phương pháp để tiêu diệt các vật thể lạ. Khi ozon phân rã nó tạo thành các gốc tự do của oxy, là những chất có hoạt tính cao và gây nguy hiểm hay tiêu diệt phần lớn các phân tử hữu cơ.
Ozon được sử dụng trong một số trường hợp trong y tế. Nó có thể được sử dụng để ảnh hưởng tới cân bằng chống oxy hóa-hỗ trợ oxy hóa của cơ thể, khi đó thông thường cơ thể sẽ phản ứng với sự hiện diện của nó bằng cách sản sinh ra các enzym chống oxy hóa.
Liệu pháp ozon được sử dụng trong y học thử nghiệm, việc này đang gây ra nhiều nghi vấn do nó chưa được nghiên cứu và kiểm nghiệm một cách khoa học và cẩn thận. Liệu pháp này là nguy hiểm bởi vì ozon là một chất ăn mòn rất mạnh.
Tại Mỹ, liệu pháp ozon là bất hợp pháp, vì FDA vẫn chưa cho phép thử nghiệm nó trên người. Ít nhất đã có một người chết vì sử dụng nó tại Mỹ. Các máy "làm sạch không khí" để sản xuất "oxy hoạt hóa", tức ozon, vẫn được bày bán trên thị trường Mỹ.
Ozon được tìm thấy để chuyển đổi cholesteron trong máu thành cục (làm cứng và hẹp các động mạch). Sản phẩm cholesteron này cũng gây ra bệnh Alzheimer.
Ozon được nghiên cứu rất nhiều và nó bị coi là chất gây ung thư cho một số động vật (số khác thì không), cũng như là tác nhân gây đột biến ở một số vi khuẩn.
Ghi chú
[sửa | sửa mã nguồn]- ^ This vapor pressure is for the critical temperature, which is below room temperature.
Chú thích
[sửa | sửa mã nguồn]- ^ a b c d e "NIOSH Pocket Guide to Chemical Hazards #0476". Viện An toàn và Sức khỏe Nghề nghiệp Quốc gia Hoa Kỳ (NIOSH).
- ^ Gas Encyclopedia; Ozone
- ^ Cuthbertson, Clive; Cuthbertson, Maude (1914). "On the Refraction and Dispersion of the Halogens, Halogen Acids, Ozone, Steam Oxides of Nitrogen, and Ammonia". Philosophical Transactions of the Royal Society A. 213 (497–508): 1–26. Bibcode:1914RSPTA.213....1C. doi:10.1098/rsta.1914.0001. Truy cập ngày 4 tháng 2 năm 2016.
- ^ Streng, A. G. (1961). "Tables of Ozone Properties". Journal of Chemical & Engineering Data. Quyển 6 số 3. tr. 431–436. doi:10.1021/je00103a031.
- ^ "Ozone Basics". NOAA. ngày 20 tháng 3 năm 2008.
- ^ a b Toth, Gary; Hillger, Don. "Precursor Era Contributors to Meteorology". colostate.edu.
- ^ a b Rubin, Mordecai B. (2001). "The History of Ozone: The Schönbein Period, 1839–1868" (PDF). Bull. Hist. Chem. Quyển 26 số 1. tr. 40–56. Bản gốc (PDF) lưu trữ ngày 11 tháng 4 năm 2008. Truy cập ngày 28 tháng 2 năm 2008.
- ^ "Scientists born on October 18th". Today in Science History.
- ^ a b c d Jacewicz, Natalie (2017). "A Killer of a Cure". Distillations. Quyển 3 số 1. tr. 34–37. Truy cập ngày 13 tháng 4 năm 2018.
- ^ Le Prestre, Philippe G., biên tập (1998). Protecting the ozone layer: lessons, models, and prospects; [product of the Tenth Anniversary Colloquium of the Montreal Protocol, held on ngày 13 tháng 9 năm 1997; part of a series of events held in Montreal to mark the tenth anniversary of the signing of the Montreal Protocol on Substances that Deplete the Ozone Layer, ngày 16 tháng 9 năm 1987]. Boston: Kluwer. tr. 2. ISBN 9780792382454.
- ^ Schönbein, Christian Friedrich (1840). "Research on the nature of the odour in certain chemical reactions". Letter to the Académie des Sciences in Paris.
- ^ Jacques-Louis Soret (1865). "Recherches sur la densité de l'ozone". Comptes rendus de l'Académie des sciences. Quyển 61. tr. 941.
- ^ "Ozone FAQ". Global Change Master Directory. Bản gốc lưu trữ ngày 1 tháng 6 năm 2006. Truy cập ngày 10 tháng 5 năm 2006.
- ^ Redlands Chamber of Commerce Collection, City Archives, A.K. Smiley Public Library, Redlands, CA
- ^ Henry Henshaw to William Brewster, ngày 2 tháng 7 năm 1902, Harvard Museum of Comparative Zoology Archives.
- ^ O'Connell, Sanjida (ngày 18 tháng 8 năm 2009). "The science behind that fresh seaside smell". The Telegraph.
- ^ Anstie, Francis (1874). "Clinic of the Month: Dr. McKendrick on Ozone". The Practitioner: A Journal of Therapeutics and Public Health. Quyển 12 số January–June. tr. 123.
- ^ Rubin, Mordecai B. (2001). "THE HISTORY OF OZONE. THE SCHÖNBEIN PERIOD, 1839–1868" (PDF). Bulletin for the History of Chemistry. Quyển 26 số 1. tr. 48. Truy cập ngày 13 tháng 4 năm 2018.
- ^ Hill, L.; Flack, M. (ngày 28 tháng 12 năm 1911). "The Physiological Influence of Ozone". Proceedings of the Royal Society B: Biological Sciences. Quyển 84 số 573. tr. 404–415. Bibcode:1911RSPSB..84..404H. doi:10.1098/rspb.1911.0086.
- ^ Stoker, George (1916). "The Surgical Uses of Ozone". Lancet. Quyển 188 số 4860. tr. 712. doi:10.1016/S0140-6736(01)31717-8.
Xem thêm
[sửa | sửa mã nguồn]- Suy giảm ozon, còn được gọi là "lỗ thủng ozon"
- Tiềm năng suy giảm tầng ozon
- Lớp ozon
- Ozon tầng đối lưu
Liên kết ngoài
[sửa | sửa mã nguồn]- NASA's Earth Observatory article on Ozone Lưu trữ ngày 2 tháng 10 năm 2008 tại Wayback Machine
- Chất tẩy
- Chất oxy hóa
- Suy giảm tầng ozon
- Chất khí
- Khí nhà kính
- Hóa môi trường
- Oxy
- Trang có lỗi kịch bản
- Trang thiếu chú thích trong bài
- Bản mẫu webarchive dùng liên kết wayback
- Bài viết có văn bản tiếng Hy Lạp
Từ khóa » Công Thức Electron Của Ozon
-
Bài 29. Oxi - Ozon - Củng Cố Kiến Thức
-
Oxi Và Ozon - Thầy Phạm Ngọc Dũng Dạy HÓA
-
Bài 29: Oxi-Ozon - Hoc24
-
Phân Tử Ozon Gồm Ba Nguyên Tử Oxi.Công Thức Của Ozon Là Gì?
-
[PDF] BÀI 29: OXI-OZON A. OXI I. VỊ TRÍ VÀ CẤU TẠO Số Hiệu Nguyên Tử 8 ...
-
Bài 29: Oxi - Ozon
-
Ozone Là Gì?
-
Công Thức Electron Của Oxi Là Gì? . Khối Lương Nguyên Tử Của ôzon ...
-
Oxi Ozon - SlideShare
-
Tính Chất Hóa Học Của Oxi (O), Ozon Và Bài Tập Về Oxi - Hóa 10 Bài 29
-
Bài Giảng Hóa Học 10 - Bài 29: Oxi - Ozon - Giáo Án Lớp 10
-
Top 12 Công Thức Hóa Học Của Ozon - Thư Viện Hỏi Đáp