Lưu Huỳnh – Wikipedia Tiếng Việt
Có thể bạn quan tâm
| Lưu huỳnh, 16S | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tính chất chung | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tên, ký hiệu | Lưu huỳnh, S | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Phiên âm | /ˈsʌlfər/ SUL-fər | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hình dạng | Màu vàng chanh | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lưu huỳnh trong bảng tuần hoàn | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Số nguyên tử (Z) | 16 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Khối lượng nguyên tử chuẩn (±) (Ar) | 32,065(5) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Phân loại | phi kim | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhóm, phân lớp | 16, p | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chu kỳ | Chu kỳ 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cấu hình electron | [Ne] 3s2 3p4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| mỗi lớp | 2, 8, 6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tính chất vật lý | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Màu sắc | Vàng chanh | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Trạng thái vật chất | Chất rắn | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhiệt độ nóng chảy | 388,36 K (115,21 °C, 239,38 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhiệt độ sôi | 717,8 K (444,6 °C, 832,3 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mật độ | (alpha) 2,07 g·cm−3 (ở 0 °C, 101.325 kPa) (beta) 1,96 g·cm−3 (gamma) 1,92 g·cm−3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mật độ ở thể lỏng | ở nhiệt độ nóng chảy: 1,819 g·cm−3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Điểm tới hạn | 1314 K, 20,7 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhiệt lượng nóng chảy | (mono) 1,727 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhiệt bay hơi | (mono) 45 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhiệt dung | 22,75 J·mol−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Áp suất hơi
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tính chất nguyên tử | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Trạng thái oxy hóa | 6, 5, 4, 3, 2, 1, -1, -2 Acid mạnh | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Độ âm điện | 2,58 (Thang Pauling) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Năng lượng ion hóa | Thứ nhất: 999,6 kJ·mol−1Thứ hai: 2252 kJ·mol−1Thứ ba: 3357 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bán kính liên kết cộng hóa trị | 105±3 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bán kính van der Waals | 180 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Thông tin khác | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cấu trúc tinh thể | Trực thoi | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Độ dẫn nhiệt | (Vô định hình)0.205 W·m−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Điện trở suất | ở 20 °C: (Vô định hình)2×1015 Ω·m | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tính chất từ | Nghịch từ[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mô đun khối | 7,7 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Độ cứng theo thang Mohs | 2,0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Số đăng ký CAS | 7704-34-9 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Đồng vị ổn định nhất | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bài chính: Đồng vị của Lưu huỳnh | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Lưu huỳnh (tên khác: Sulfur (đọc như "Xun-phu"), lưu hoàng hay diêm sinh) là nguyên tố hóa học trong bảng tuần hoàn có ký hiệu S và số nguyên tử 16. Nó là một phi kim phổ biến, không mùi, không vị, nhiều hóa trị. Lưu huỳnh, trong dạng gốc của nó là chất rắn kết tinh màu vàng chanh. Trong tự nhiên, nó có thể tìm thấy ở dạng đơn chất hay trong các khoáng chất sulfide và sulfat. Nó là một nguyên tố thiết yếu cho sự sống và được tìm thấy trong hai amino acid. Lưu huỳnh được ứng dụng chủ yếu để tạo ra axit sunfuric-nguyên liệu sản xuất phân lân (P) nhưng cũng được dùng rộng rãi trong việc chế tạo thuốc súng, diêm, thuốc trừ sâu và thuốc diệt nấm.
Các đặc trưng nổi bật
[sửa | sửa mã nguồn]
Ở nhiệt độ phòng, lưu huỳnh là một chất rắn xốp màu vàng nhạt. Mặc dù lưu huỳnh không được ưa thích do mùi của nó - thường xuyên bị so sánh với mùi trứng ung - mùi này thực ra là đặc trưng của hydro sulfide (H2S); còn lưu huỳnh đơn chất không có mùi. Nó cháy với ngọn lửa màu xanh lam và tỏa ra lưu huỳnh dioxide, với mùi ngột ngạt dị thường. Lưu huỳnh không hòa tan trong nước nhưng hòa tan trong carbon disulfide và các dung môi không phân cực khác. Các trạng thái oxy hóa phổ biến của nó là -2, -1 (pirit sắt...), +2, +4 và +6. Lưu huỳnh tạo thành các hợp chất ổn định với gần như mọi nguyên tố, ngoại trừ các khí trơ.
Lưu huỳnh trong trạng thái rắn thông thường tồn tại như là các phân tử vòng dạng vòng hoa S8. Lưu huỳnh có nhiều thù hình bên cạnh S8. Loại một nguyên tử từ vòng sẽ là S7, đây là nguyên nhân cho màu vàng đặc trưng của lưu huỳnh. Nhiều vòng khác cũng được điều chế ra, bao gồm S12 và S18. Trái lại, nguyên tố oxy cùng phân nhóm nhưng nhẹ hơn về cơ bản chỉ tồn tại trong hai dạng cơ bản có ý nghĩa hóa học là: O2 và O3. Seleni, nguyên tố nặng hơn cùng phân nhóm với lưu huỳnh có thể tạo ra các vòng nhưng thông thường nó nằm trong chuỗi polymer.
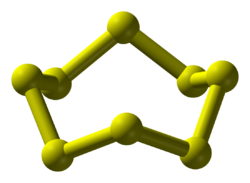
Tinh thể lưu huỳnh rất phức tạp. Phụ thuộc vào các điều kiện cụ thể, các thù hình của lưu huỳnh tạo thành vài cấu trúc tinh thể khác nhau, với các dạng tà phương và đơn tà S8 là các dạng được nghiên cứu kỹ nhất.
Một tính chất đáng chú ý là độ nhớt của lưu huỳnh nóng chảy, không giống như phần lớn các chất lỏng khác, tăng lên theo nhiệt độ do sự hình thành các chuỗi polymer. Tuy nhiên, sau khi đã đạt được một khoảng nhiệt độ nhất định thì độ nhớt lại bị giảm do đã đủ năng lượng để phá vỡ chuỗi polyme.
Lưu huỳnh vô định hình hay "dẻo" có thể được tạo ra khi làm nguội nhanh lưu huỳnh nóng chảy. Các nghiên cứu tinh thể bằng tia X chỉ ra rằng dạng vô định hình có thể có cấu trúc xoắn ốc với 8 nguyên tử trên một vòng. Dạng này là ổn định động ở nhiệt độ phòng và dần dần chuyển ngược thành dạng kết tinh. Tiến trình này diễn ra trong vòng vài giờ hay vài ngày nhưng có thể tăng tốc nhờ xúc tác.
Ứng dụng
[sửa | sửa mã nguồn]
Lưu huỳnh có nhiều ứng dụng công nghiệp. Thông qua dẫn xuất chính của nó là acid sulfuric (H2SO4), lưu huỳnh được đánh giá là một trong các nguyên tố quan trọng nhất khi được sử dụng như là nguyên liệu công nghiệp. Nó có vai trò quan trọng bậc nhất đối với mọi lĩnh vực của nền kinh tế thế giới.
Sản xuất acid sulfuric là ứng dụng chủ yếu của lưu huỳnh, và việc tiêu thụ acid sulfuric được coi như một trong các chỉ số tốt nhất về sự phát triển công nghiệp của một quốc gia. Acid sulfuric được sản xuất hàng năm ở Hoa Kỳ nhiều hơn bất kỳ hóa chất công nghiệp nào khác.
Lưu huỳnh cũng được sử dụng trong ắc quy, bột giặt, lưu hóa cao su, thuốc diệt nấm và trong sản xuất phân bón phosphat. Các sulfit được sử dụng để làm trắng giấy và làm chất bảo quản trong rượu vang và làm khô hoa quả. Do bản chất dễ cháy của nó, lưu huỳnh cũng được dùng trong các loại diêm, thuốc súng và pháo hoa. Các thiosulfat natri và amôni được sử dụng như là các tác nhân cố định trong nhiếp ảnh. Magnesi sulfat, được biết dưới tên gọi muối Epsom có thể dùng như thuốc nhuận tràng, chất bổ sung cho các bình ngâm (xử lý hóa học), tác nhân làm tróc vỏ cây, hay để bổ sung magnesi cho cây trồng. Lưu huỳnh tác dụng được với thủy ngân ngay ở điều kiện thường nên được dùng để thu hồi thủy ngân rơi vãi.[2]
Cuối thế kỷ XVIII, các nhà sản xuất đồ gỗ sử dụng lưu huỳnh nóng chảy để tạo ra các lớp khảm trang trí trong các sản phẩm của họ. Do dioxide lưu huỳnh được tạo ra trong quá trình nung chảy lưu huỳnh nên các đồ gỗ với lớp khảm lưu huỳnh đã bị loại bỏ rất nhanh.
Từ xa xưa, người ta đã biết dùng lưu huỳnh để làm đẹp da và trị mụn trứng cá. Tuy nhiên đến nay vẫn chưa có nghiên cứu nào tìm ra cách hoạt động của lưu huỳnh trong việc điều trị mụn. Bằng thực nghiệm, người ta đã kết luận lưu huỳnh có khả năng kháng viêm và kháng khuẩn cao, từ đó làm xẹp nốt mụn một cách nhanh chóng. Để đạt hiệu quả cao, lưu huỳnh có thể được kết hợp với acid salicylic (BHA) hay resorcinol trong thành phần dược liệu.[cần dẫn nguồn]
Điều chế
[sửa | sửa mã nguồn]Lưu huỳnh có thể được tìm thấy riêng lẻ và trong lịch sử thường thu được ở dạng này; pyrit cũng là nguồn cung cấp lưu huỳnh Ở các vùng núi lửa ở Sicily, vào thời cổ đại, nó được tìm thấy trên bề mặt Trái đất và "quy trình Sicilia" đã được sử dụng: các mỏ lưu huỳnh được chất đống và xếp chồng lên nhau trong các lò gạch xây trên sườn đồi dốc, có khoảng không giữa chúng. Sau đó, một ít lưu huỳnh được nghiền thành bột, rải lên quặng đã xếp chồng lên nhau và bốc cháy, khiến lưu huỳnh tự do tan chảy xuống các ngọn đồi. Cuối cùng, các lớp trầm tích trên bề mặt đã cạn kiệt và các thợ mỏ đã khai quật các mạch mà cuối cùng rải rác khắp cảnh quan Sicilia với các mỏ mê cung. Việc khai thác không được cơ giới hóa và sử dụng nhiều lao động, với những người nhặt quặng lấy quặng ra khỏi đá, và những người thợ mỏ hoặc carusi mang những giỏ quặng lên bề mặt, thường xuyên qua những đường hầm dài một dặm trở lên. Khi quặng đã nổi lên bề mặt, nó sẽ được khử và chiết xuất trong lò nấu chảy. Điều kiện ở các mỏ lưu huỳnh ở Sicilia thật khủng khiếp, khiến Booker T. Washington viết "Ngay bây giờ tôi chưa sẵn sàng để nói rằng tôi tin vào địa ngục vật chất ở thế giới tiếp theo ở mức độ nào, nhưng mỏ lưu huỳnh ở Sicily là điều gần nhất." đến địa ngục mà tôi mong được thấy trong cuộc đời này."Lưu huỳnh vẫn được khai thác từ các lớp trầm tích bề mặt ở các quốc gia nghèo hơn có núi lửa, chẳng hạn như Indonesia, và điều kiện của người lao động không được cải thiện nhiều kể từ thời Booker T. Washington.
Lưu huỳnh nguyên tố được chiết xuất từ vòm muối (đôi khi nó xuất hiện ở dạng gần như tinh khiết) cho đến cuối thế kỷ 20. Hiện nay lưu huỳnh được sản xuất như một sản phẩm phụ của các quy trình công nghiệp khác như lọc dầu, trong đó lưu huỳnh không được ưa chuộng. Là một khoáng chất, lưu huỳnh tự nhiên dưới vòm muối được cho là nguồn tài nguyên khoáng sản hóa thạch, được tạo ra do hoạt động của vi khuẩn kỵ khí trên các mỏ sunfat. Nó đã được loại bỏ khỏi các mỏ muối dạng vòm chủ yếu bằng quy trình Frasch.Trong phương pháp này, nước quá nhiệt được bơm vào cặn lưu huỳnh tự nhiên để làm tan chảy lưu huỳnh, sau đó khí nén đưa sản phẩm tan chảy nguyên chất 99,5% trở lại bề mặt. Trong suốt thế kỷ 20, quy trình này đã tạo ra lưu huỳnh nguyên tố không cần tinh chế thêm. Do số lượng các mỏ lưu huỳnh như vậy có hạn và chi phí vận hành chúng cao, quy trình khai thác lưu huỳnh này đã không được sử dụng rộng rãi ở bất kỳ nơi nào trên thế giới kể từ năm 2002.
Ngày nay, lưu huỳnh được sản xuất từ dầu mỏ, khí tự nhiên và các tài nguyên hóa thạch liên quan, từ đó nó thu được chủ yếu dưới dạng hydro sunfua.[8] Các hợp chất lưu huỳnh hữu cơ, tạp chất không mong muốn trong dầu mỏ, có thể được nâng cấp bằng cách cho chúng trải qua quá trình hydrodesulfur hóa, làm đứt các liên kết C–S:[77][78]
R-S-R + 2 H2 → 2 RH + H2S
Hydro sunfua thu được từ quá trình này, cũng như nó xuất hiện trong khí tự nhiên, được chuyển thành lưu huỳnh nguyên tố theo quy trình Claus. Quá trình này đòi hỏi quá trình oxy hóa một số hydro sunfua thành lưu huỳnh đioxit và sau đó là sự cân đối của cả hai:[77] [78]
3 O2 + 2 H2S → 2 SO2 + 2 H2O
SO2 + 2 H2S → 3 S + 2 H2O
- Ngoài ra lưu huỳnh còn được điều chế bằng cách cho Axit sunfulric tác dụng với Natri thiosulfat
Na2S2O3 + H2SO4 → Na2SO4 + S ↓ + SO2 ↑ + H2O
Vai trò sinh học
[sửa | sửa mã nguồn]Các amino acid cystein và methionin chứa lưu huỳnh, cũng như mọi polypeptid, protein và enzym có chứa các amino acid này. Điều đó làm cho lưu huỳnh trở thành thành phần cần thiết cho mọi tế bào. Các liên kết disulfide giữa các polypeptid là rất quan trọng trong sự tạo thành và cấu trúc của protein. Homocystein và taurin cũng là các amino acid chứa lưu huỳnh nhưng không được mã hóa bởi DNA và chúng cũng không phải là một phần của cấu trúc sơ cấp của các protein. Một số dạng vi khuẩn sử dụng sulfide hydro (H2S) thay vào vị trí của nước như là chất cung cấp electron trong các tiến trình thô sơ tương tự như quang hợp. Thực vật cũng hấp thụ lưu huỳnh từ đất trong dạng các ion sulfat. Lưu huỳnh vô cơ tạo thành một phần của các cụm sắt-lưu huỳnh, và lưu huỳnh là chất cầu nối trong vị trí CuA của cytochrom c oxidaza. Lưu huỳnh là thành phần quan trọng của coenzym A
Ảnh hưởng môi trường
[sửa | sửa mã nguồn]Sự đốt cháy than và dầu mỏ trong công nghiệp và các nhà máy điện giải phóng ra một lượng lớn lưu huỳnh dioxide SO2, nó sẽ phản ứng với hơi nước và oxy có trong khí quyển để tạo ra acid sulfuric. Đây là nguyên nhân của các trận mưa acid và làm giảm pH của đất cũng như các khu vực chứa nước ngọt, tạo ra những tổn thất đáng kể cho môi trường tự nhiên và gây ra phong hóa hóa học đối với các công trình xây dựng và kiến trúc. Các tiêu chuẩn về nhiên liệu đã thắt chặt các chỉ tiêu về hàm lượng lưu huỳnh trong các nhiên liệu hóa thạch để giảm thiểu sự hình thành của mưa acid. Lưu huỳnh được tách ra từ các nhiên liệu này sau đó sẽ được làm tinh khiết và tạo ra một phần lớn của sản lượng lưu huỳnh được sản xuất.
Lịch sử
[sửa | sửa mã nguồn]
Lưu huỳnh (tiếng Phạn, sulvere; tiếng Latinh sulpur), (còn được gọi là lưu hoàng, sinh diêm vàng, diêm sinh) đã được biết đến từ thời cổ đại, và nó được nhắc đến trong Pentateuch của Kinh Thánh (Sáng thế ký). Các phiên dịch ra tiếng Anh của nó đều coi lưu huỳnh như là "brimstone", tạo ra tên gọi của các bài thuyết giáo "Fire and brimstone", trong đó địa ngục và sự quở trách của Thượng đế đối với những kẻ có tội được nhấn mạnh. Nó có từ phần của Kinh Thánh cho rằng địa ngục có mùi của lưu huỳnh.
Trong tiếng Ả Rập sufra có nghĩa là màu vàng, có từ màu sáng của dạng tự nhiên của lưu huỳnh và người ta cho rằng nó là nguyên từ của các tên gọi để chỉ lưu huỳnh trong ngôn ngữ của một số quốc gia châu Âu hiện nay.
Homer đã đề cập tới "lưu huỳnh ngăn ngừa các loài phá hoại" từ thế kỷ IX TCN và năm 424 TCN thì bộ tộc ở Boeotia đã tiêu hủy các bức tường của thành phố bằng cách đốt hỗn hợp than, lưu huỳnh và hắc ín dưới chân tường.
Vào khoảng thế kỷ XII, người Trung Quốc đã phát minh ra thuốc súng, nó là hỗn hợp của kali nitrat (KNO3), carbon và lưu huỳnh. Các nhà giả kim thuật ban đầu cho lưu huỳnh ký hiệu giả kim thuật là một tam giác ở đỉnh của chữ thập. Vào những năm cuối thập niên 1770, Antoine Lavoisier đã củng cố niềm tin của cộng đồng khoa học khi cho rằng lưu huỳnh là một nguyên tố chứ không phải hợp chất.
Năm 1867 lưu huỳnh đã được phát hiện trong các mỏ ở Louisiana và Texas. Lớp nằm trên của nó là cát chảy đã ngăn cản các hoạt động khai thác thông thường. Vì thế quy trình Frasch đã nảy sinh và được thực hiện.
Sự phổ biến
[sửa | sửa mã nguồn]

Lưu huỳnh dạng đơn chất có thể tìm thấy ở gần các suối nước nóng và các khu vực núi lửa tại nhiều nơi trên thế giới, đặc biệt là dọc theo vành đai lửa Thái Bình Dương. Các nguồn phổ biến này là cơ sở cho tên gọi truyền thống brimstone, do lưu huỳnh có thể tìm thấy gần các miệng núi lửa. Các trầm tích núi lửa hiện được khai thác tại Indonesia, Chile và Nhật Bản.
Các mỏ đáng kể của lưu huỳnh đơn chất cũng tồn tại trong các mỏ muối dọc theo bờ biển thuộc vịnh Mexico và trong các evaporit ở Đông Âu và Tây Á. Lưu huỳnh trong các mỏ này được cho là có được nhờ hoạt động của các vi khuẩn kỵ khí đối với các khoáng chất sulfat, đặc biệt là thạch cao. Các mỏ này là nền tảng của sản xuất lưu huỳnh công nghiệp tại Hoa Kỳ, Ba Lan, Nga, Turkmenistan và Ukraina.
Lưu huỳnh thu được từ dầu mỏ, khí đốt và cát dầu Athabasca đã trở thành nguồn cung cấp lớn trên thị trường, với các kho dự trữ lớn dọc theo Alberta.

Các hợp chất chứa lưu huỳnh nguồn gốc tự nhiên phổ biến nhất là các sulfide kim loại, như pyrit (sulfide sắt), cinnabar hay còn gọi là chu sa (sulfide thủy ngân), galen (sulfide chì), sphalerit (sulfide kẽm) và stibnit (sulfide antimon) cũng như các sulfat kim loại, như thạch cao (calci sulfat), alunit (nhôm kali sulfat) và barit (bari sulfat). Hydro sulfide là một chất khí tạo ra mùi đặc trưng của trứng thối. Trong tự nhiên, nó có trong các sản phẩm phun trào từ núi lửa, chẳng hạn từ các miệng phun thủy nhiệt, và do tác động của vi khuẩn với các hợp chất hữu cơ chứa lưu huỳnh khi bị phân hủy.
Các màu đặc trưng của các vệ tinh núi lửa của Sao Mộc, như Io, là do các dạng khác nhau của lưu huỳnh gây ra (nóng chảy, rắn hay khí). Các khu vực sẫm màu trên Mặt Trăng gần hố Aristarchus có thể là mỏ lưu huỳnh. Lưu huỳnh cũng tồn tại trong nhiều loại thiên thạch.
Hợp chất
[sửa | sửa mã nguồn]Hydro sulfide có mùi đặc trưng của trứng thối. Khi hòa tan trong nước nó có tính acid và phản ứng với nhiều kim loại để tạo ra các sulfide kim loại. Các sulfide kim loại khá phổ biến, đặc biệt là của sắt. Sulfide sắt còn được gọi là pyrit cũng như khoáng sản màu vàng. Một điều thú vị là pyrit có các tính chất bán dẫn [1] Lưu trữ ngày 20 tháng 12 năm 2004 tại Wayback Machine. Galen là sulfide chì tự nhiên, là chất bán dẫn đầu tiên được phát hiện và nó đã từng được dùng làm bộ chỉnh lưu tín hiệu trong các "râu mèo" của các radio tinh thể đầu tiên.
Nhiều hợp chất hữu cơ của lưu huỳnh với mùi khó ngửi như các êtyl và mêtyl mecaptan được dùng làm chất tạo mùi cho khí đốt nhằm dễ dàng phát hiện rò rỉ. Mùi của tỏi và "mùi hôi như chồn hôi" cũng do các hợp chất hữu cơ chứa lưu huỳnh gây ra. Tuy nhiên, không phải mọi hợp chất hữu cơ chứa lưu huỳnh đều có mùi khó ngửi, chẳng hạn, terpen-một hợp chất chứa lưu huỳnh là tác nhân tạo ra mùi thơm đặc trưng của quả bưởi chùm.
Nitride lưu huỳnh polyme hóa có các tính chất của kim loại mặc dù nó không chứa bất kỳ một nguyên tử kim loại nào. Hợp chất này cũng có các tính chất điện và quang học bất thường. Polyme này có thể tạo ra từ Tetra lưu huỳnh tetranitride S4N4.
Các hợp chất quan trọng khác của lưu huỳnh còn có:
Vô cơ:
- Các sulfide (S2-) là các hợp chất đơn giản nhất của lưu huỳnh với các nguyên tố hóa học khác.
- Các sulfit (SO32-), các muối của acid sulfurơ, H2SO3, được tạo ra bằng cách hòa tan SO2 trong nước. acid sulfurơ và các sulfit tương ứng là các chất khử tương đối mạnh. Các hợp chất dẫn xuất khác từ SO2 còn có các ion pyrosulfit hay mêtabisulfit (S2O52−).
- Các sulfat (SO42-), các muối của acid sulfuric. acid sulfuric cũng phản ứng với SO3 trong các tỷ lệ đẳng phân tử gam để tạo ra acid pyrosulfuric (H2S2O7).
- Các thiosulfat (đôi khi được gọi là thiosulfit hay "hyposulfit") (S2O32−)- như thiosulfat natri được dùng như các chất cố định trong nhiếp ảnh (trong vai trò của các chất khử) và amoni thiosulfat đã được phát hiện như là chất thay thế cho các cyanide trong lọc quặng vàng [2].
- Natri dithionit, Na2S2O4 tạo ra từ acid hyposulfurơ/đithionơ - là một chất khử mạnh.
- Natri dithionat (Na2S2O6)
- Các acid polythionic (H2SnO6), trong đó n dao động từ 3 đến 80.
- acid peroxymonosulfuric (H2SO5) và acid peroxydisulfuric (H2S2O8)-được điều chế từ phản ứng của SO3 hay H2SO4 với H2O2 đậm đặc một cách tương ứng.
- Các natri polysulfide (Na2Sx)
- lưu huỳnh hexafluoride, SF6, một tác nhân đẩy nặng, dạng khí, không phản ứng và không độc
- Tetra lưu huỳnh tetranitride S4N4.
- Các thiocyanat là các hợp chất chứa ion thiocyanat, SCN-. Liên quan đến các ion này là thiocyanogen, (SCN)2.
Hữu cơ:
- dimethylsulfoniopropionat (DMSP; (CH3)2S+CH2CH2COO-) là thành phần trung tâm của chu trình lưu huỳnh hữu cơ trong đại dương.
- Các thioether là các phân tử với công thức tổng quát dạng R-S-R′, trong đó R và R′ là các nhóm hữu cơ. Các chất này là sự tương đương của các ether (lưu huỳnh thay thế oxy).
- Các thiol (hay mecaptan) là các phân tử với nhóm chức -SH. Chúng là các chất tương đương với rượu (lưu huỳnh thay thế oxy).
- Các thiolat có nhóm chức -S- gắn vào. Chúng là các chất tương đương của các ankoxide (lưu huỳnh thay thế oxy).
- Sulfoxide là các phân tử với nhóm chức R-S(=O)-R′, trong đó R và R′ là các nhóm hữu cơ. Một chất phổ biến trong số các sulfoxide là DMSO.
- Sulfon là các phân tử với nhóm chức R-S(=O)-R′, trong đó R và R′ là các nhóm hữu cơ.
- Thuốc thử Lawesson là thuốc thử hóa học có thể lấy oxy từ các chất hữu cơ khác và thay nó bằng lưu huỳnh.
- Naphthalen-1,8-diyl 1,3,2,4-dithiadiphosphetane 2,4-disulfide
Đồng vị
[sửa | sửa mã nguồn]Lưu huỳnh có 18 đồng vị, trong đó 4 đồng vị ổn định: S32 (95,02%), S33 (0,75%), S34 (4,21%) và S36 (0,02%). Các đồng vị khác và S35 là các đồng vị phóng xạ và có chu kỳ bán rã ngắn. S35 được tạo ra từ sự bắn phá của các tia vũ trụ với Ar40 trong khí quyển Trái Đất. Nó có chu kỳ bán rã là 87 ngày.
Khi các khoáng chất sulfide theo nước mưa xuống đất thì cân bằng đồng vị giữa các thể rắn và các thể lỏng có thể sinh ra sự sai biệt nhỏ trong các giá trị của dS34 của các khoáng chất cùng nguồn gốc. Sự khác biệt trong các khoáng chất có thể sử dụng để ước tính nhiệt độ của cân bằng. dC13 và dS34 của các carbonat cùng tồn tại và các sulfide có thể sử dụng để xác định pH và độ khó giữ oxy của các chất lỏng mang theo quặng trong quá trình hình thành quặng.
Trong phần lớn các hệ sinh thái rừng, sulfat chủ yếu thu được từ khí quyển hay sự phong hóa của các quặng khoáng sản và các chất đã thoát hơi nước cũng cung cấp một lượng lưu huỳnh nhỏ. Lưu huỳnh với thành phần đồng vị đặc biệt được sử dụng để xác định các nguồn ô nhiễm, và lưu huỳnh được làm giàu được thêm vào dưới dạng dấu vết trong các nghiên cứu thủy học. Các khác biệt trong độ phổ biến tự nhiên cũng được sử dụng trong các hệ thống mà trong đó có các biến đổi đủ lớn của S34 trong thành phần của hệ sinh thái.
Phòng ngừa
[sửa | sửa mã nguồn]Các chất như carbon disulfide, carbonyl sulfide, hydro sulfide và lưu huỳnh dioxide cần phải rất cẩn thận khi tiếp xúc.
Mặc dù lưu huỳnh dioxide là khá an toàn để sử dụng như là phụ gia thực phẩm với một lượng nhỏ, nhưng khi ở nồng độ cao nó phản ứng với hơi ẩm để tạo ra acid sulfurơ mà với một lượng đủ lớn có thể gây tổn thương cho phổi, mắt hay các cơ quan khác. Trong các sinh vật không có phổi như côn trùng hay thực vật thì nó ngăn cản sự hô hấp.
Hydro sulfide là rất nhẹ (nó độc hơn nhiều so với cyanide). Mặc dù ban đầu nó có mùi, nhưng nó nhanh chóng làm mất cảm giác mùi, vì thế các nạn nhân có thể không biết được sự hiện diện của nó cho đến khi đã quá muộn.
Xem thêm
[sửa | sửa mã nguồn]- Chu trình lưu huỳnh
- Liên kết disulfide
- Sulfoni S+, S+R3
Chú thích
[sửa | sửa mã nguồn]- ^ Magnetic susceptibility of the elements and inorganic compounds, in Handbook of Chemistry and Physics (PDF). CRC press. 2000. ISBN 0849304814. Bản gốc (PDF) lưu trữ ngày 12 tháng 1 năm 2012. Truy cập ngày 18 tháng 7 năm 2011.
- ^ "Xử lý thủy ngân rơi vãi". hanoimoi.com.vn. Truy cập ngày 24 tháng 6 năm 2022.
Tham khảo
[sửa | sửa mã nguồn]- Phòng thí nghiệm quốc gia Los Alamos, Hoa Kỳ-Lưu huỳnh Lưu trữ ngày 16 tháng 10 năm 2004 tại Wayback Machine
- R. Steudel (ed.): Elemental Sulfur and Sulfur-Rich Compounds (phần I & II), Topics in Current Chemistry Vol. 230 & 231, Springer, Berlin 2003.
Liên kết ngoài
[sửa | sửa mã nguồn]- Biểu đồ pha của lưu huỳnh. Lưu trữ ngày 23 tháng 2 năm 2010 tại Wayback Machine
- WebElements.com-Lưu huỳnh
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Từ khóa » Tính Chất Của Lưu Huỳnh Kết Tủa
-
TÍNH CHẤT HÓA HỌC, ĐIỀU CHẾ VÀ ỨNG DỤNG CỦA LƯU ...
-
Lưu Huỳnh Là Gì? Tính Chất Vật Lí, Tính Chất Hóa Học - Tác Dụng, ứng ...
-
Tính Chất Hoá Học Của Lưu Huỳnh (S), Bài Tập Về Lưu ... - Hayhochoi
-
Tính Chất Của Lưu Huỳnh Kết Tủa | Leo-đè
-
Lưu Huỳnh Và Những điều Có Thể Bạn Chưa Biết Về Phi Kim Này
-
Hidro Sunfua (H2S), Lưu Huỳnh Dioxit (SO2), Lưu Huỳnh Trioxit (SO3 ...
-
Tính Chất Hóa Học Của Lưu Huỳnh, Cách Điều Chế Và Các Ứng ...
-
Lý Thuyết Hợp Chất Của Lưu Huỳnh Hay, Chi Tiết Nhất
-
Tính Chất Hóa Học Của Các Hợp Chất Của Lưu Huỳnh - 123doc
-
Bài 35. Bài Thực Hành Số 5. Tính Chất Các Hợp Chất Của Lưu Huỳnh
-
Tính Chất Hóa Học Của Hidro Sunfua H2S, Lưu Huỳnh Dioxit SO2 ...
-
Hoá Học 10 Bài 30: Lưu Huỳnh - HOC247
-
Tính Chất Hóa Học Của Các Hợp Chất Của Lưu Huỳnh - Tài Liệu Text